
- •Модуль 4
- •2.8. Молекулярная физика
- •Примеры решения задач по молекулярной физике
- •4. Использовать уравнения кинетической теории газов и закон Дальтона:
- •2.7. Термодинамика
- •Укажите, какие ответы могут быть окончанием фразы:
- •Какое из приведенных выражений соответствует молярной теплоемкости идеального газа при постоянном объеме?
- •Примеры решения задач по термодинамике
Какое из приведенных выражений соответствует молярной теплоемкости идеального газа при постоянном объеме?
. 2. . 3. . 4. . 5. .
Какие из формул определяют первый закон термодинамики для адиабатического процесса?
. 2. . 3. . 4.
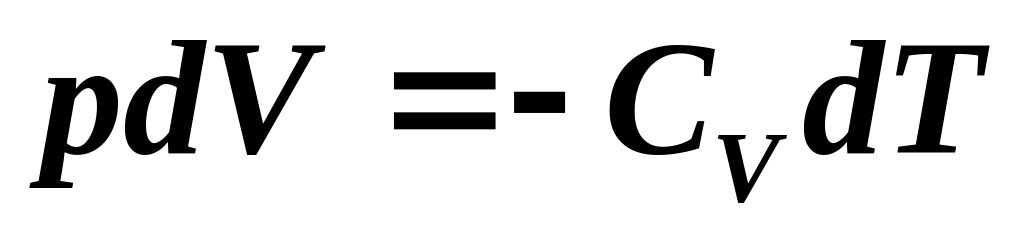 .
.
Какой из перечисленных процессов называется адиабатическим?
Перенос теплоты потоком жидкости или газа.
Процесс, при котором теплоемкость постоянна.
Передача теплоты от одного тела к другому при их контакте.
Процесс, происходящий без теплообмена с окружающей средой.
Перенос теплоты с помощью электромагнитных волн.
Какое из уравнений первого закона термодинамики справедливо для изобарического процесса?
. 2. . 3. .
4.
![]() .
5.
.
.
5.
.
Укажите, на какую величину молярная теплоемкость идеального газа при постоянном давлении больше, чем при постоянном объеме.
. 2. . 3.
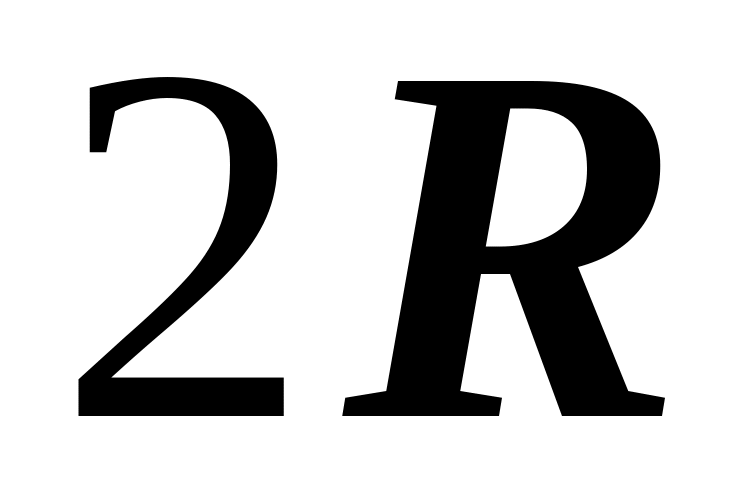 .
4.
.
4.
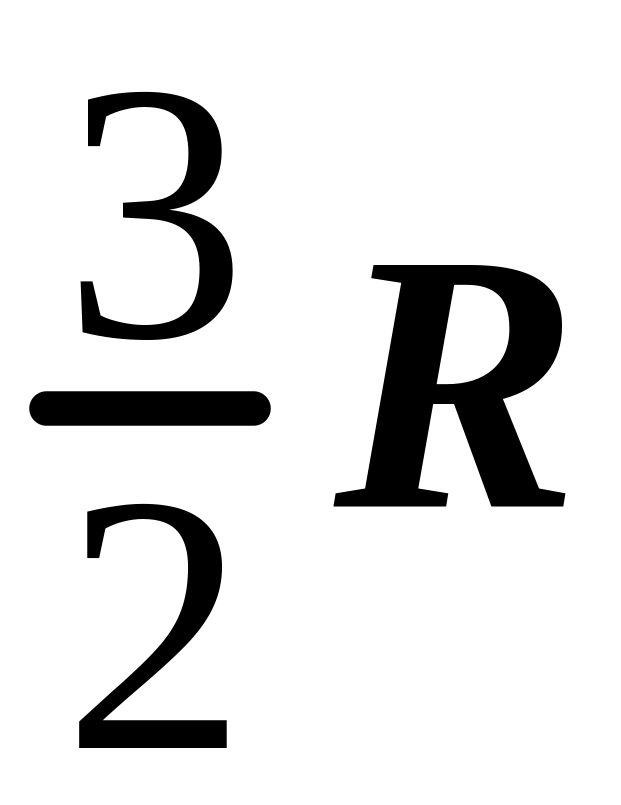 .
5.
.
5.
 .
.
Какое из выражений определяет обратимый термодинамический процесс?
В системе происходят процессы, в результате которых изменяется состояние.
Циклический процесс, в результате которого система возвращается в исходное состояние.
Такое изменение состояния системы, при котором она может возвращаться в начальное состояние без остаточных изменений в системе и окружающей среде.
Процесс превращения всего количества теплоты, получаемой системой от внешней среды, в работу.
Циклический процесс, происходящий по часовой стрелке.
Какая из кривых прямого цикла Карно (рис. 2.30.) соответствует адиабатическому расширению?
Какая из кривых прямого цикла Карно (см. рис. 2.30.) соответствует изотермическому расширению?
Чему численно равно количество теплоты, полученной от нагревателя за один прямой цикл Карно (см. рис. 2.30.)?
1
Рис.
2.30.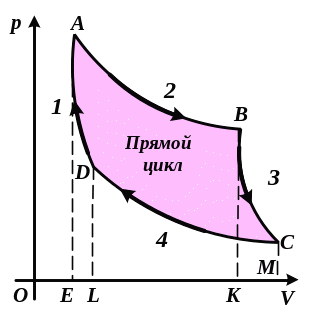
2. Площади EABK.
3. Площади EADL.
4. Площади ABCD.
5. Площади KBCM.
Чему численно равна полез- ная работа прямого цикла Карно (см. рис. 2.30.)?
1. Площади EABCM.
2. Площади EABK.
3. Площади EADL.
4. Площади ABCD.
5. Площади KBCM.
Какая из кривых обратного цикла Карно (рис. 2.34.) соответствует адиабатическому сжатию?
Какая из кривых обратного цикла Карно (см. рис. 2.34.) соответствует изотермическому сжатию?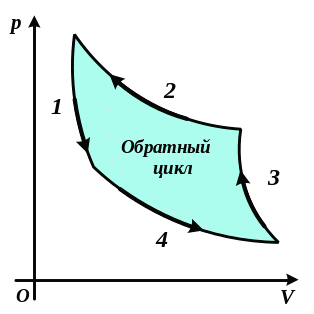 Рис.
2.34.
Рис.
2.34.Укажите определение КПД цикла Карно.
1. Невозможен такой периоди- чески действующий двигатель, который совершал бы работу в большем количестве, чем получаемая им энергия.
2.
![]() ,
где А
– работа, совершенная за цикл;
,
где А
– работа, совершенная за цикл;
![]() – количество теплоты, переданное от
нагревателя.
– количество теплоты, переданное от
нагревателя.
3. КПД обратимых машин, работающих с одним и тем же нагревателем и холодильником, должен быть одинаков.
4. Отношение разности температур нагревателя и холодильника к температуре нагревателя, т. е.
![]() .
.
Какие характеристики являются функциями состояния вещества?
1. Внутренняя энергия. 2. Выполненная работа.
3. Количество теплоты. 4. Энтропия. 5. Правильного ответа нет.
Какие свойства вещества характеризует энтропия?
1. Степень превращаемости теплоты в работу.
2. Температуру тела.
3. Степень неупорядоченности движения молекул.
4. Внутреннюю энергию. 5. Правильного ответа нет.
Укажите формулировки второго закона термодинамики.
Внутренняя энергия непосредственно и полностью не превращается в механическую работу.
2. Теплота не может переходить сама по себе от тела с низкой температурой к телу с более высокой температурой.
3. Невозможен процесс, единственным результатом которого является превращение всей теплоты в эквивалентную ей работу.
4. ”Perpetum mobile” второго рода создать невозможно.
5. При самопроизвольном процессе тепло переходит от более нагретого тела к менее нагретому телу.
Укажите математическое выражение записи второго закона термодинамики.
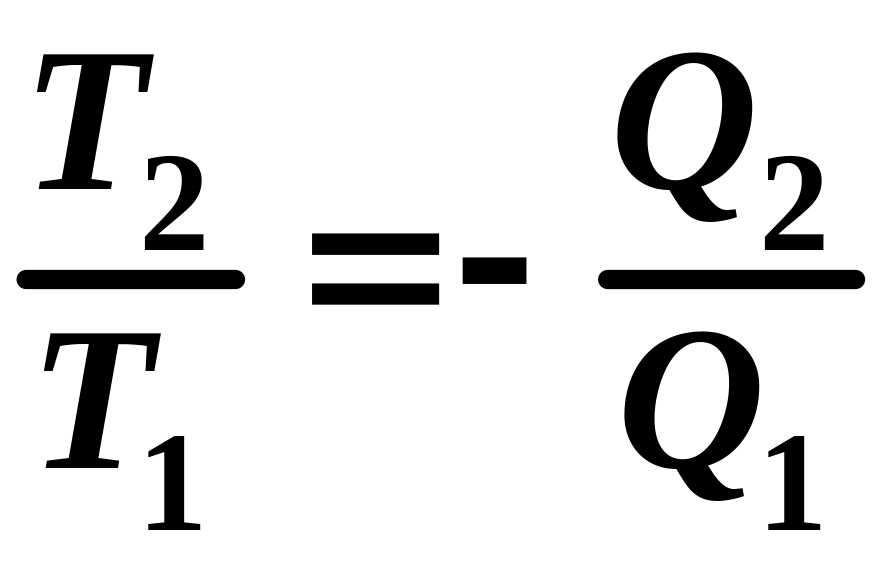 .
2.
.
2.
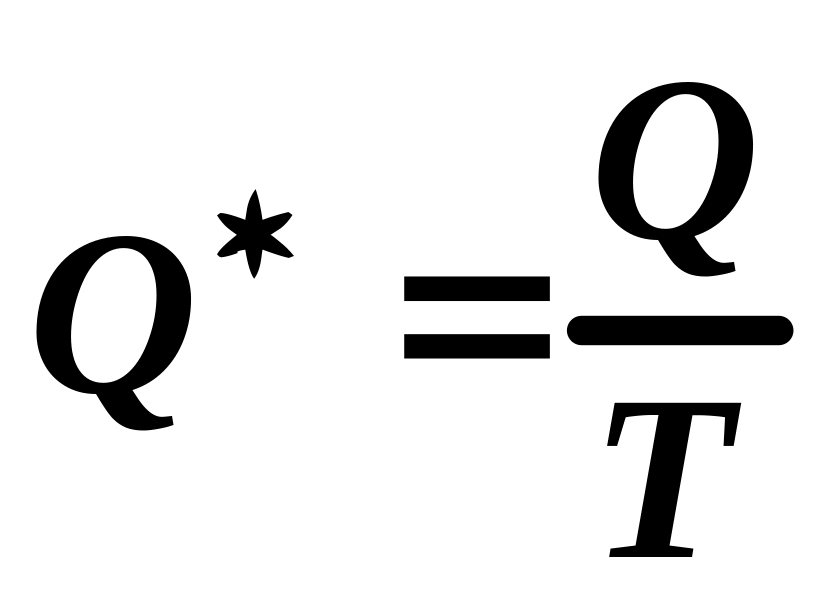 .
3.
.
3.
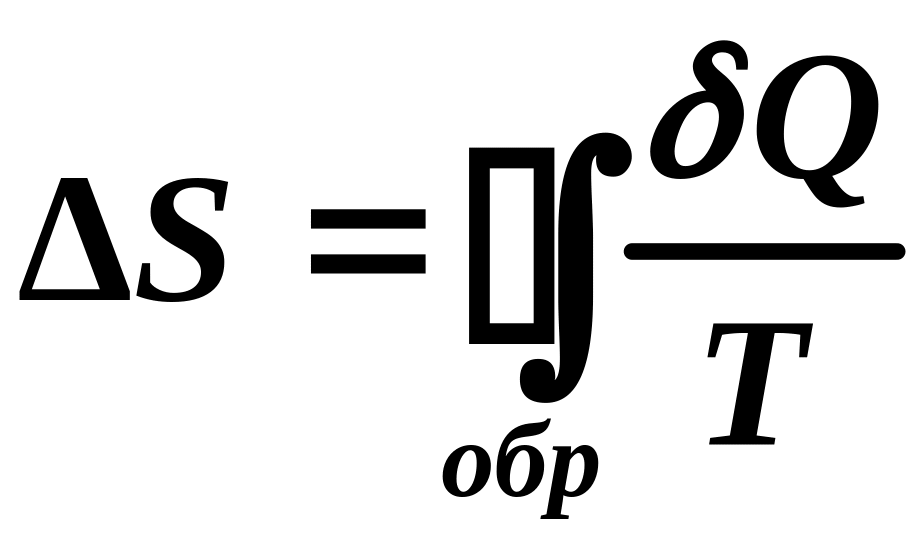 .
.
4.
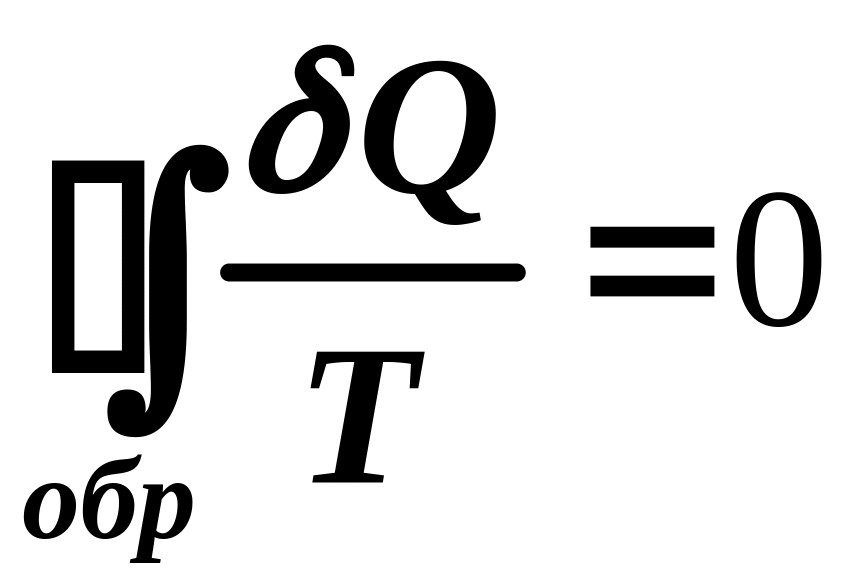 .
5.
.
5.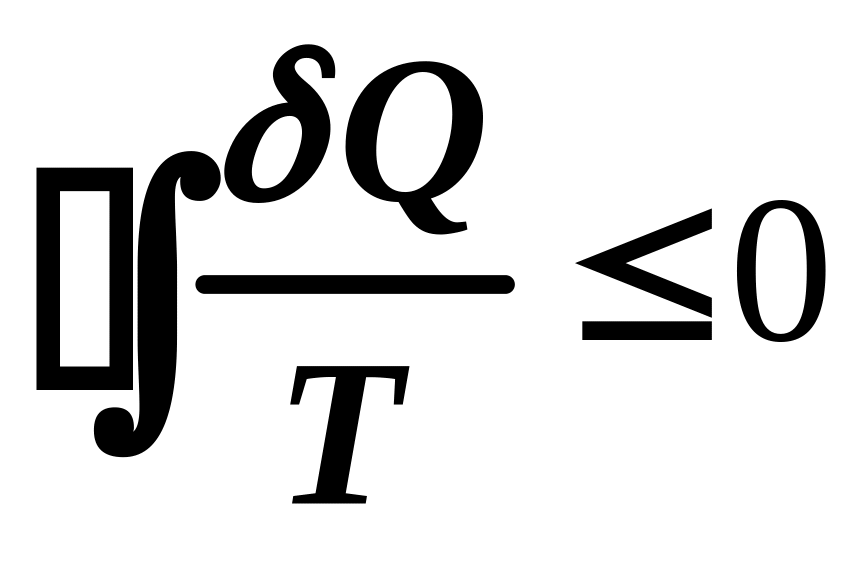 .
.
Какая формула связывает энтропию с термодинамической вероятностью состояния?
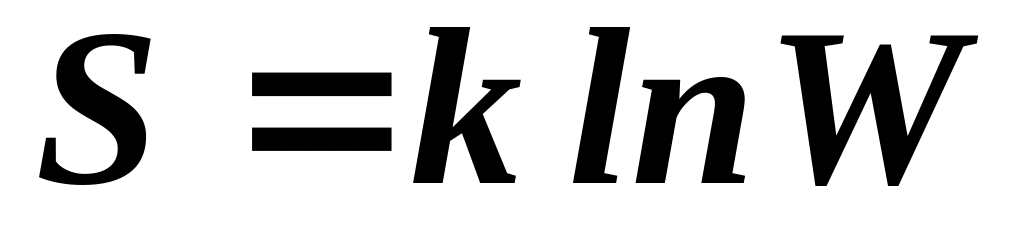 .
2.
.
2.
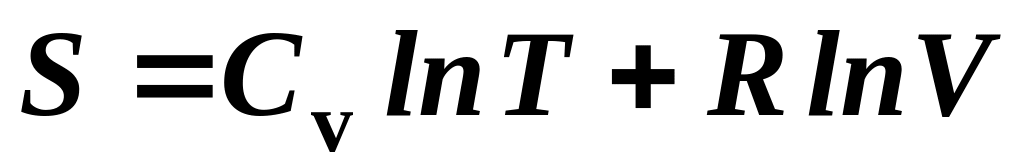 .
3.
.
3.
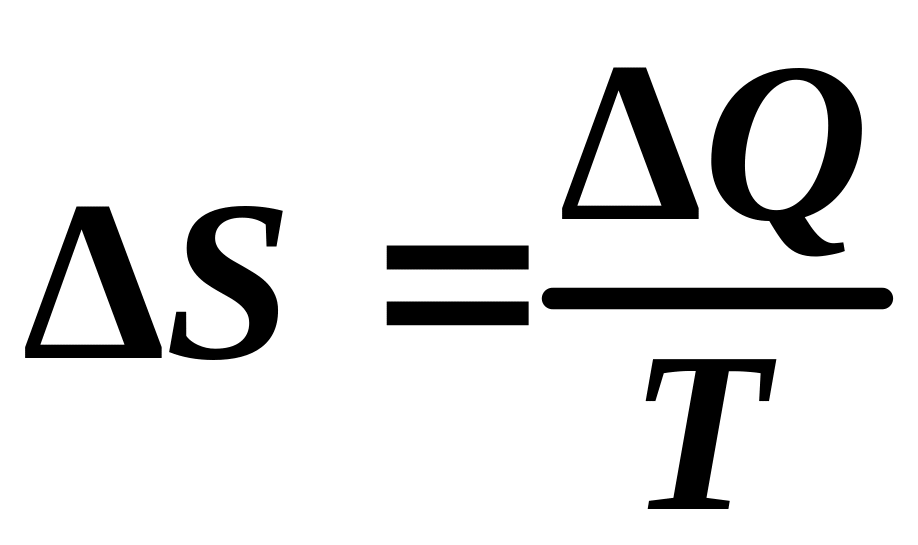 .
.
4.
![]() .
5.
.
5.
![]() .
.
Какому из перечисленных условий удовлетворяет обратимый процесс в изолированной системе?
1. Энтропия системы остается неизменной.
2. Энтропия системы уменьшается.
3. Энтропия системы увеличивается.
4. Энтропия системы увеличивается, а затем уменьшается.
5. Энтропия системы уменьшается, а затем увеличивается.
Укажите основные задачи термодинамики.
Определение изменения внутренней энергии системы, если известны начальное и конечное ее состояния.
Вычисление работы, совершаемой системой, и количества теплоты, полученной (или отданной) ею, если известны промежуточные состояния (т.е. известен процесс).
Нахождение макроскопических параметров состояния системы при переходе ее из одного состояния в другое.
Применение закона сохранения энергии для изолированных термодинамических систем.
Определение небольшим количеством макроскопических параметров (давление p, объем V, температура T и некоторые другие) равновесного состояния системы, состоящей из большого числа частиц.
