
- •Оглавление
- •Перечень сокращений
- •Введение
- •Общая характеристика производных азепина и диазепина
- •Производные дибензоазепина
- •Производные бензодиазепина
- •Общие физические свойства
- •Общие химические свойства
- •Взаимосвязь между физико-химическими свойствами и фармакокинетическими параметрами производных 1,4-бензодиазепина
- •Производные триазолобензодиазепина
- •Производные 1,5-бензотиазепина
- •Определение примесей
- •Выводы.
- •Методы идентификации
- •Производные дибензоазепина
- •Производные бензодиазепина
- •Производные 1,5-бензотиазепина
- •Производные триазолобензодиазепина
- •Методы количественного определения
- •Производные дибензоазепина
- •Производные бензодиазепина
- •Производные 1,5-бензотиазепина
- •Производные триазолобензодиазепина
- •Заключение
- •Список использованных источников
Производные триазолобензодиазепина
Одним из представителей этих производных является алпразолам.
Алпразолам (Alprazolam)
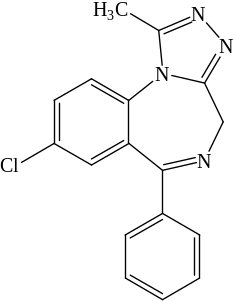
Белый или белый со слабым желтоватым оттенком мелкокристаллический порошок без запаха. Т.пл. 225-230 °С практически нерастворимый в воде и эфире, умеренно растворимый в этаноле и легко растворимый в хлороформе, мало растворим в ацетоне и этилацетате. Наряду с транквилизирующими, обладает умеренными антидепрссивными свойствами. Оказывает противосудорожное и слабое снотворное действие [5].
Производные 1,5-бензотиазепина
Бензотиазепин отличается от 1,4-бензодиазепина наличием в положении 1 атома серы вместо азота и расположением гетероатомов:

1,4-бензодиазепина 1,5-бензотиазепина
Применяют лекарственное вещество дилтиазема гидрохлорид
Дилтиазема гидрохлорид (Diltiazem Hydrochloride)

Белый кристаллический порошок или тонкие кристаллы без запаха. Т.пл. 210 °С (с разложением). Удельное вращение от + 110 до + 116° (1%-ный водный раствор), растворим в воде, метаноле, хлороформе, муравьиной кислоте, нерастворим в эфире. Относится к вазодилататорам непрямого действия. Под его влиянием снижается тонус периферических артериальных сосудов. Дилтиазем вызывает расширение коронарных сосудов сердца и улучшает кровоснабжение миокарда [5].
Определение примесей
К лекарственным веществам предъявляют многочисленные жесткие требования. Прежде всего, лекарственное вещество должно обладать высокой активностью, избирательностью и продолжительностью лечебного действия. Себестоимость его производства не должна быть слишком высокой. Наконец, оно должно быть доступным, а доходность при его реализации на фармацевтическом рынке - достаточно высокой. Оно должно быть нетоксичным и не должно вызывать нежелательных побочных эффектов. Кроме того, лекарственное вещество должно иметь высокую стабильность при хранении и быть высокочистым [8]. Поэтому в контроле качества ЛС обязательно проводят исследования на чистоту. Основными источниками примесей являются: исходные и промежуточные продукты синтеза, сопутствующие вещества (в растительном и животном сырье), растворители, остатки кислот и щелочей, в том числе за счет выщелачивания стекла, металл, из которого изготовлена аппаратура, песок, асбест, волокна тканей и фильтровальной бумаги и т.д. Примеси можно разделить на две группы: технологические (внесенные исходным сырьем или образовавшиеся в процессе производства) и примеси, приобретенные в процессе хранения, транспортировки, под воздействием различных факторов (тепла, света, кислорода воздуха, влаги и др.).
Примеси могут быть токсичные (недопустимые), оказывающие влияние на фармакологический эффект, и примеси, указывающие на степень очистки ЛВ. Последние, присутствуя в больших количествах, снижают содержание биологически активных веществ и, соответственно, уменьшают активность ЛС. Поэтому в ФС (ФСП) указываются допустимые пределы содержания таких примесей и приводятся испытания, подтверждающие отсутствие токсичных примесей [3]. По фармакопее США примеси определяются методом ВЭЖХ. Проверяют содержание тяжелых металлов, исследуют на сульфатную залу. Определяют потерю в массе при высушивании и при сжигании. По британской фармакопее примеси определяют методом ТСХ и методом ВЭЖХ. По Международной фармакопее исследования на чистоту проводят методом ТСХ и методом ВЭЖХ. Проверяют содержание тяжелых металлов, исследуют на сульфатную залу. Определяют потерю в массе при высушивании.
