
- •МЕТАБОЛИЗМ ЛИПИДОВ
- •РОЛЬ ЛИПИДОВ В ПИТАНИИ
- •ПЕРЕВАРИВАНИЕ И ВСАСЫВАНИЕ ЛИПИДОВ
- •ЖИРОВАЯ ТКАНЬ И ЕЕ УЧАСТИЕ В ОБМЕНЕ ЛИПИДОВ
- •ОКИСЛЕНИЕ ЖИРНЫХ КИСЛОТ
- •Окисление ненасыщенных жирных кислот
- •Окисление жирных кислот с нечетным числом углеродных атомов
- •МЕТАБОЛИЗМ КЕТОНОВЫХ ТЕЛ
- •БИОСИНТЕЗ НАСЫЩЕННЫХ ЖИРНЫХ КИСЛОТ
- •НЕЗАМЕНИМЫЕ ЖИРНЫЕ КИСЛОТЫ
- •ЭЙКОЗАНОИДЫ
- •БИОСИНТЕЗ ТРИГЛИЦЕРИДОВ
- •МЕТАБОЛИЗМ ФОСФОЛИПИДОВ
- •Распад и обновление фосфолипидов
- •БИОСИНТЕЗ ХОЛЕСТЕРИНА
- •РЕГУЛЯЦИЯ ЛИПИДНОГО ОБМЕНА
- •НАРУШЕНИЯ ЛИПИДНОГО ОБМЕНА
- •Липосомы
факторов. В частности, скорость синтеза редуктазы в печени подвержена четким суточным колебаниям: максимум ее приходится на полночь, а минимум – на утренние часы.
Активность ГМГ-редуктазы возрастает при введении инсулина и тиреоидных гормонов. Это приводит к усилению синтеза холестерина и повышению его уровня в крови.
При голодании, тиреоидэктомии, введение глюкагона и глюкокортикоидов, напротив, отмечается угнетение синтеза холестерина, что прежде всего связано со снижением активности ГМГ-КоА-редуктазы.
РЕГУЛЯЦИЯ ЛИПИДНОГО ОБМЕНА
Обмен липидов регулируется ЦНС. Кора большого мозга оказывает трофическое влияние на жировую ткань либо через нижележащие отделы ЦНС – симпатическую и парасимпатическую системы, либо через эндокринные железы. В настоящее время установлен ряд биохимических механизмов, лежащих в основе действия гормонов на липидный обмен.
Известно, что длительный отрицательный эмоциональный стресс, сопровождающийся увеличением выброса катехоламинов в кровяное русло, может вызвать заметное похудание. Уместно напомнить, что жировая ткань обильно иннервируется волокнами симпатической нервной системы, возбуждение этих волокон сопровождается выделением норадреналина непосредственно в жировую ткань. Адреналин и норадреналин увеличивают скорость липолиза в жировой ткани; в результате усиливается мобилизация жирных кислот из жировых депо и повышается содержание неэстерифицированных жирных кислот в плазме крови. Как отмечалось, тканевые липазы (триглицеридлипаза) существуют в двух взаимопревращающихся формах, одна из которых фосфорилирована и каталитически активна, а другая – нефосфорилирована и неактивна. Адреналин стимулирует через аденилатциклазу синтез цАМФ. В свою очередь цАМФ активирует соответствующую протеинкиназу, которая способствует фосфорилированию липазы, т.е. образованию ее активной формы. Следует заметить, что действие глюкагона на липолитическую систему сходно с действием кате-холаминов.
Не подлежит сомнению, что секрет передней доли гипофиза, в частности соматотропный гормон, оказывает влияние на липидный обмен. Гипофункция железы приводит к отложению жира в организме, наступает гипофизарное ожирение. Напротив, повышенная продукция СТГ стимулирует липолиз, и содержание жирных кислот в плазме крови увеличивается. Доказано, что стимуляция липолиза СТГ блокируется
ингибиторами синтеза мРНК. Кроме того, известно, что действие СТГ на липолиз характеризуется наличием лаг-фазы продолжительностью около 1 ч, тогда как адреналин стимулирует липолиз почти мгновенно. Иными словами, можно считать, что первичное действие этих двух типов гормонов на липолиз проявляется различными путями. Адреналин стимулирует активность аденилатциклазы, а СТГ индуцирует синтез данного фермента. Конкретный механизм, с помощью которого СТГ избирательно увеличивает синтез аденилатциклазы, пока неизвестен.
Инсулин оказывает противоположное адреналину и глюкагону действие на липолиз и мобилизацию жирных кислот. Недавно было показано, что инсулин стимулирует фосфодиэстеразную активность в жировой ткани. Фосфодиэстераза играет важную роль в поддержании постоянного уровня цАМФ в тканях, поэтому увеличение содержания инсулина должно повышать активность фосфодиэстеразы, что в свою очередь приводит к уменьшению концентрации цАМФ в клетке, а следовательно, и к образованию активной формы липазы.
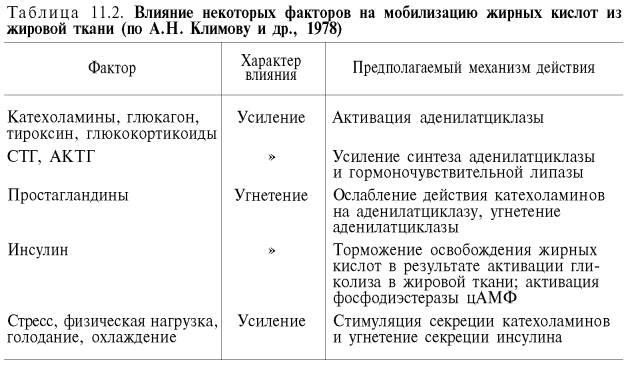
Несомненно, и другие гормоны, в частности тироксин, половые гормоны, также оказывают влияние на липидный обмен. Например, известно, что удаление половых желез (кастрация) вызывает у животных избыточное отложение жира. Однако сведения, которыми мы располагаем, не дают пока основания с уверенностью говорить о конкретном механизме их действия на обмен липидов. В табл. 11.2 приведены сводные данные о влиянии ряда факторов на мобилизацию жирных кислот из жировых депо.
НАРУШЕНИЯ ЛИПИДНОГО ОБМЕНА
Нарушение процессов всасывания жиров. Нарушения липидного обмена возможны уже в процессе переваривания и всасывания жиров. Одна группа расстройств связана с недостаточным поступлением панкреатической липазы в кишечник, вторая обусловлена нарушением поступления в кишечник желчи. Кроме того, нарушения процессов переваривания и всасывания липидов могут быть связаны с заболеваниями пищеварительного тракта (при энтеритах, гиповитаминозах и некоторых других патологических состояниях). Образовавшиеся в полости кишечника моноглицериды и жирные кислоты не могут нормально всасываться вследствие повреждения эпителиального покрова кишечника. Во всех этих случаях кал содержит много нерасщепленного жира или невсосавшихся высших жирных кислот и имеет характерный серовато-белый цвет.
Нарушение процессов перехода жира из крови в ткань. При недостаточной активности липопротеинлипазы крови нарушается переход жирных кислот из хиломикронов (ХМ) плазмы крови в жировые депо (не расщепляются триглицериды). Чаще это наследственное заболевание, обусловленное полным отсутствием активности липопротеинлипазы. Плазма крови при этом
имеет молочный цвет в результате чрезвычайно высокого содержания ХМ. Наиболее эффективным лечением этого заболевания является замена природных жиров, содержащих жирные кислоты с 16–18 углеродными атомами, синтетическими, в состав которых входят короткоцепочечные жирные кислоты с 8–10 углеродными атомами. Эти жирные кислоты способны всасываться из кишечника непосредственно в кровь без предварительного образования ХМ.
Кетонемия и кетонурия. В крови здорового человека кетоновые (ацетоновые) тела содержатся в очень небольших концентрациях. Однако при голодании, а также у лиц с тяжелой формой сахарного диабета содержание кетоновых тел в крови может повышаться до 20 ммоль/л. Это состояние носит название кетонемии; оно обычно сопровождается резким увеличением содержания кетоновых тел в моче (кетонурия). Например, если в норме за сутки с мочой выводится около 40 мг кетоновых тел, то при сахарном диабете содержание их в суточной порции мочи может доходить до
50г и более.
Внастоящее время явления кетонемии и кетонурии при сахарном диабете или голодании можно объяснить следующим образом. И диабет, и голодание сопровождаются резким сокращением запасов гликогена в печени. Многие ткани и органы, в частности мышечная ткань, находятся в состоянии энергетического голода (при недостатке инсулина глюкоза не может с
достаточной скоростью поступать в клетку). В этой ситуации благодаря возбуждению метаболических центров в ЦНС импульсами с хеморецепторов клеток, испытывающих энергетический голод, резко усиливаются липолиз и мобилизация большого количества жирных кислот из жировых депо в печень. В печени происходит интенсивное образование кетоновых тел. Образующиеся в необычно большом количестве кетоновые тела (ацетоуксусная и β-гидроксимасляная кислоты) с током крови транспортируются из печени к периферическим тканям. Периферические ткани при диабете и голодании сохраняют способность использовать кетоновые тела в качестве энергетического материала, однако ввиду необычно высокой концентрации кетоновых тел в притекающей крови мышцы и другие органы не справляются с их окислением и как следствие возникает кетонемия.
Атеросклероз и липопротеины. В настоящее время доказана ведущая роль определенных классов липопротеинов в патогенезе атеросклероза. Известное положение акад. Н.Н. Аничкова «без холестерина нет атеросклероза» с учетом современных знаний можно выразить иначе: «без атерогенных липопротеинов не может быть атеросклероза».
Напомним, что плазменные липопротеины – это сложные комплексные соединения, в состав которых, кроме белка, входит липидный компонент. Плазменные липопротеины имеют характерное строение: внутри липопротеиновой частицы находится жировая капля (ядро), содержащая неполярные липиды (триглицериды, этерифицированный холестерин). Жировая капля окружена оболочкой, в состав которой входят фосфолипиды, белок и свободный холестерин. Толщина этой оболочки составляет 2,0–2,5 нм, что соответствует половине толщины фосфолипидного бислоя клеточной мембраны.
Различают несколько классов липопротеинов: α-липопротеины, или липопротеины высокой плотности (ЛПВП); β-липопротеины, или липопротеины низкой плотности (ЛПНП); пре-β-липопротеины, или липопро-теины очень низкой плотности (ЛПОНП); хиломикроны (ХМ).
Установлено, что атеросклероз и связанные с ним заболевания протекают при значительном повышении содержания в плазме крови фракции ЛПНП, а во многих случаях и фракции ЛПОНП (подробнее см. главу 17).
Исследования последних 5 лет показали, что сами по себе нативные ЛПНП и ЛПОНП аллергенностью не обладают. Атерогенность у этих классов липопротеинов появляется только тогда, когда их частицы подвергнутся химическому изменению и прежде всего перекисному окислению. При этом сначала в их составе образуются такие продукты
