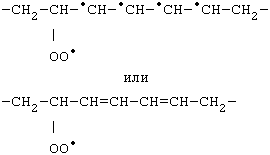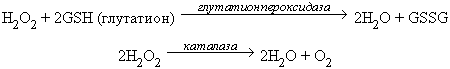Радикал коэнзима q
Биологическое окисление субстратов клеточного дыхания, таких как глюкоза, пировиноградная и янтарная кислота и другие, осуществляется, как известно, в два этапа. На первом этапе в цикле трикарбоновых кислот происходит последовательный отрыв атомов водорода от субстрата и образование восстановленных форм пиридиннуклеотидов НАДН и НАДФН. На втором этапе электроны от НАДН и НАДФН переносятся по так называемой дыхательной цепи на кислород. В состав дыхательной цепи входят флавопротеиды, комплексы негемового железа, убихинон и гемопротеиды (цитохромы a,b и c и цитохром-оксидаза).
 Важным
звеном цепи переноса электронов служит
убихинол (коэнзим Q) радикал которого
(семихинон, ·QH) образуется либо при
одноэлектронном окислении убихинола
(QH2,
гидрохинон-форма) , либо при одноэлектронном
восстановлении убихинона (Q). В норме
радикал этот – не более как рядовой
Важным
звеном цепи переноса электронов служит
убихинол (коэнзим Q) радикал которого
(семихинон, ·QH) образуется либо при
одноэлектронном окислении убихинола
(QH2,
гидрохинон-форма) , либо при одноэлектронном
восстановлении убихинона (Q). В норме
радикал этот – не более как рядовой
Убихинол (коэнзим Q)

участник процесса переноса электронов; но при нарушении работы дыхательной цепи он может стать источником других, менее безобидных радикалов, в первую очередь, радикалов кислорода.
Образование семихинона при
одноэлектронном окислении убихинола
КИНЕТИКА РЕАКЦИЙ ЦЕПНОГО ОКИСЛЕНИЯ ЛИПИДОВ
Общая схема реакций
Примером сложной системы
химических реакций может служить цепное
окисление липидов. Кинетика процесса
перекисного окисления обладает большой
сложностью, иллюстрацией чего могут
служить экспериментальные кривые,
приведенные на рисунке.

К суспензии митохондрий, выделенных из печени крысы, добавляли
FeSO4 и наблюдали за изменением
концентрации ионов Fe2+, продукта перекисного окисления липидов - малонового диальдегида, а также за интенсивностью хемилюминесценции, сопровождающей процесс перекисного окисления липидов. Можно видеть сложность кинетических кривых, что отражает сложность самой Кинетика окисления ионов Fe2+, образования реакции цепного окисления липидов. Эта продуктов перекисного окисления липидов реакция включает в себя несколько стадий
(MDA) и хемилюминесценции (CL) в
суспензии митохондрий, к которой добавлены
ионы двухвалентного железа
.
Инициирование цепи
При взаимодействии сильного окислителя с ненасыщенной жирной кислотой, точнее с -CH2- группой в a-положении по отношению к двойной связи происходит отрыв атома водорода от этой связи и образуется свободный радикал (алкил-радикал) жирной кислоты (L·). В качестве реагента, способного отрывать атом водорода чаще всего служит свободный радикал, например, радикал гидроксила HO·:
|
HO· + –CH2–CH=CH–CH2–CH=CH–CH2– H2O + –CH2–CH=CH–•CH–CH=CH–CH2– |
Реакция инициирования может быть записана в виде простого химического уравнения:
|
HO· + LH -> H2O + L· |
(1) |
Двойная связь, как известно, образуется одной парой s-электронов и двумя p-электронами. В молекуле полиненасыщенных жирных кислот имеется не одна, а две или более двойных связей, но они разделены группой -CH2- (метиленовым мостиком). Двойные связи и p-электроны локализованы. В радикале L· имеется не один, а пять одинаковых p-электронов, расположенных у соседних углеродных атомов, как это изображено ниже:
|
–CH2–•CH–•CH–•CH–•CH–•CH–CH2– |
Нельзя определить, какие же из этих электронов образуют двойные связи. Все они находятся в равном положении, и присоединение какой-либо химической группы к любому из этих пяти углеродных атомов примерно равновероятно. Можно сказать, что свободная валентность принадлежит не конкретному атому углерода, а делокализована.
Продолжение цепи
В кислородсодержащей среде происходит быстрое присоединение молекулы кислорода к одному из атомов углерода с неспаренным электроном, обычно к крайнему. Образуется радикал перекиси липида:
|
|
В дальнейшем мы будем обозначать такой радикал знаком LO2· и называть его липидным диоксиалкил-радикалом. Реакция образования диоксил-радикала может быть теперь описана таким химическим уравнением:
|
L· + O2 -> LO2· |
(2) |
Радикал LO2· легко отнимает атом водорода от одной из соседних ненасыщенных жирных кислот (LH):
|
LO2· + LH -> LOOH + L· |
(3) |

Образуется новый липидный алкил-радикал, а затем реакции 2 и 3 повторяются. Перекисное окисление липидов - это цепная реакция, и её можно наглядно изобразить следующим образом: см. рисунок. В реакцию продолжения цепи
Цепная ракция перекисного вовлекаются всё новые и новые окисления липидов молекулы субстратов, т.е. молекулярный кислород O2 и полиненасыщенные жирные кислоты LH, и в каждом звене этой цепной реакции образуется молекула продукта - гидроперекиси липида LOOH. В каждый данный момент протекает какая-то одна частная реакция цепного окисления, так что цепи разворачиваются во времени, а не в пространстве.
Обрыв цепей
В конце концов цепи обрываются, поскольку свободные радикалы L·и LO2·, "ведущие" цепи окисления, исчезают из-за одной из возможных реакций обрыва цепей. Это могут быть следующие реакции:
|
L· + L· -> LL |
(4) |
|
L· + LO2· -> LOOL |
(5) |
|
LO2· + LO2· -> L=O + LOH + фотон |
(6) |
Последняя реакция диспропорционирования радикалов LO2· интересна тем, что она сопровождается свечением - хемилюминесценцией. В липид-содержащих системах длина цепей может составлять десятки и сотни звеньев. Для организма цепное окисление липидов - весьма нежелательное явление не только потому, что оно приводит к бесполезному сжиганию ценных компонентов клетки, но ещё и потому, что некоторые продукты цепного окисления липидов чрезвычайно токсичны. В связи с этим имеется целая система защиты от перекисного окисления, в частности, имеются вещества, "перехватчики" свободных радикалов, которые тормозят цепное окисление за счёт ещё одной реакции обрыва цепей:
|
L· + InH -> LH + In· |
(7) |
где In· - свободный радикал ингибитора цепного окисления. К числу молекул - перехватчиков радикалов относятся токоферол (витамин Е), женские половые (стероидные) гормоны, коэнзим Q (убихинон), многие другие соединения. Хотя в реакции 7 образуются радикалы этих соединений, эти радикалы недостаточно активны, чтобы оторвать атом водорода от молекул жирных кислот, и поэтому не инициируют новых цепей окисления. Обычно они быстро исчезают, например, вследствие взаимодействия друг с другом:
|
In· + In· -> In-In |
(8) |
Все соединения, тормозящие процессы цепного окисления липидов, называются антиоксидантами. К числу антиоксидантов относятся и перехватчики свободных радикалов. Антиоксидантными свойствами в определённых условиях обладают ионы металлов переменной валентности в восстановленной форме, в частности, ионы Fe2+. Они также способны перехватывать свободные радикалы в одной из следующих реакций:
|
Fe2+ + L· + H+ -> Fe3+ + LH |
(9) |
|
Fe2+ + LO2· + H+ -> Fe3+ + LOOH |
(9a) |
Разветвление цепей
В большинстве случаев ионы Fe2+ обладают однако не анти-, а прооксидантным действием, т.е. они не подавляют, а наоборот, резко усиливают процессы перекисного окисления. Это происходит потому, что ионы двухвалентного железа вступают в реакцию с продуктом перекисного окисления - гидроперекисями липидов:
|
Fe2+ + LOOH -> Fe3+ + LO· + OH- |
(10) |
В результате появляется новый свободный радикал (алкоксильный радикал липида) LO·, который инициирует образование новой цепи окисления:
|
LO· + LH -> LOH + L· |
(11) |
|
L· + O2 -> LO2· |
(2) |
|
LO2· + LH -> LOOH + L· |
(3) |
и далее реакции 2-3, 2-3, 2-3 и т.д. Разветвление цепей более наглядно видно на следующем рисунке.

Разветвление цепи перекисного
окисления липидов ионами железа
ПОВРЕЖДЕНИЯ СПОСОБНЫЕ НАНЕСТИ СРО
ПОВРЕЖДЕНИЕ КОМПОНЕНТОВ БИОЛОГИЧЕСКИХ МЕМБРАН ПРИ ПАТОЛОГИЧЕСКИХ ПРОЦЕССАХ
Биологические мембраны наряду с элементами цитоскелета формируют ультраструктуру протоплазмы. Кроме того, они выполняют множество функций, нарушение любой из которых может привести к изменению жизнедеятельности клетки в целом и даже к ее гибели. Наиболее тяжелые последствия вызывает повреждение липидного слоя (или бислоя) мембран. Липидный слой клеточной и внутриклеточных мембран выполняет две основные функции - барьерную и матричную (структурную). Повреждение барьера приводит к нарушению регуляции внутриклеточных процессов и тяжелым расстройствам клеточных функций. С другой стороны, липидный слой мембран формирует в клетке особую жидкую фазу. На поверхности раздела водной и липидной фаз, а также внутри липидной фазы "плавают" многочисленные ферменты, многие субстраты биохимических реакций, белковые клеточные рецепторы, гликолипиды и гликолипопротеиды, образующие гликокаликс. Во многих клетках до 80% белков встроены в мембраны или связаны с их поверхностью. Липидный бислой выполняет, таким образом, роль структурной основы или матрицы для всех этих белковых, липопротеидных, гликопротеидных и гликолипидных компонентов мембран. От свойств липидной фазы мембран, таких, как вязкость, поверхностный заряд, полярность, зависит работа мембранных ферментов и рецепторов. Наличие гликокаликса характерно для наружных клеточных мембран. Он выполняет ряд функций, в частности, от него зависят свойства клеточной поверхности, способность клеток к фагоцитозу и адгезии с другими клетками. Гликокаликс эритроцитов препятствует их агглютинации. Повреждение гликокаликса приводит к тяжелым последствиям, помимо прочего еще и потому, что это приводит к изменению иммунных свойств клеточной поверхности. Действие многих токсических соединений направлено на белковые компоненты клеточной мембраны. Например, цианистый калий блокирует цитохромоксидазу - фермент, входящий в состав внутренних мембран митохондрий. Ионы тяжелых металлов (ртуть, серебро, свинец) связывают SH-группы белков, в том числе мембранных ферментов и ионных каналов, вызывая их инактивацию. На белки плазматических мембран или элементы цитоскелета направлено действие многих бактериальных токсинов. Изменения в активности мембранных ферментов, каналов и рецепторных белков, вызванные неблагоприятными факторами, также приводят к нарушению функции клеток и развитию заболеваний.
Основные механизмы нарушения барьерных свойств липидного слоя
Изучение воздействия разного рода повреждающих агентов на изолированные клетки (например, эритроциты), митохондрии, фосфолипидные везикулы (липосомы), плоские бислойные липидные мембраны (БЛМ) и другие модельные объекты показало, что, в конечном счете, существует всего четыре основных процесса, которые непосредственно обусловливают нарушение целостного липидного бислоя в патологии [Владимиров Ю. А., 1973]:
перекисное окисление липидов;
действие мембранных фосфолипаз;
механическое (осмотическое) растяжение мембраны;
адсорбция на бислое полиэлектролитов, включая некоторые белки и пептиды.
Чтобы понять роль этих процессов в развитии патологического состояния, надо знать химические и физические условия протекания каждого из них, пути их регуляции в живой клетке и причины ее нарушения, характер повреждения свойств мембран под действием данного процесса, биологические последствия такого повреждения мембран для жизнедеятельности клетки и организма в целом. Рассмотрим эти вопросы на примере наиболее изученного процесса – перекисного окисления (пероксидации) липидов.
Свободнорадикальное (перекисное) окисление липидов
Перекисное окисление (пероксидация) липидов - пример процесса, идущего с участием свободных радикалов. Свободные радикалы - это молекулярные частицы, имеющие непарный электрон на внешней орбитали и обладающие высокой реакционной способностью. Их изучение ведется методом ЭПР (спиновые ловушки), хемилюминесценции и путем применения ингибиторов реакций, в которых участвуют радикалы определенного типа.
Первичные радикалы
Основные радикалы, образующиеся в клетках - это радикалы кислорода (супероксид и гидроксильный радикал), монооксид азота, радикалы ненасыщенных жирных кислот, радикалы, образующиеся в окислительно-восстановительных реакциях (например, убихинол). Радикалы образуются также при действии ультрафиолетовых лучей и в ходе метаболизма некоторых чужеродных соединений (ксенобиотиков), в том числе некоторых препаратов, одно время применявшихся в качестве лекарств.
Активные формы кислорода
Основная масса молекулярного кислорода, потребляемого клетками нашего организма, непосредственно восстанавливается до воды, окисляя органические субстраты в цепях переноса электронов. Меньшая часть кислорода расходуется на неполное окисление органических соединений. Наконец, заметная часть кислорода восстанавливается клетками нашего организма до супероксидного радикала. Так клетки – фагоциты (моноциты и гранулоциты крови и тканевые макрофаги) выделяют супероксид в реакции, катализируемой ферментным комплексом – НАДФН-оксидазой:
|
НАДФН + 2O2 -> НАДФ+ + 2O•- (супероксид) |
Дальнейшая судьба супероксидных радикалов может быть разной В норме и при отсутствие ионов металлов переменной валентности супероксидные радикалы превращаются в перекись водорода; эта реакция катализируется ферментом супероксиддисмутазой (СОД)
|
2O•- -> H2O2 + O2 |
Клетки-фагоциты используют перекись водорода, превращая ее в гипохлорит – соединение, разрушающее стенки бактериальных клеток; эта реакция катализируется ферментом миелопероксидазой
|
H2O2 + Cl- -> H2O + ClO- |
Избыток перекиси водорода удаляется под действием двух ферментов: глутатионпероксидазы или каталазы
|
|
В условиях патологии могут произойти нарушения либо системы защитных ферментов (в частности, снижение активности СОД), либо ферментных систем, связывающих ионы железа в плазме крови (церулоплазмин и трансферрин) и в клетках (ферритин). В этом случае супероксидные радикалы и перекись водорода вступают в альтернативные реакции: Образование двухвалентного железа из трехвалентного
|
Fe3+ + O•- -> Fe2++ O2 |
Реакция перекиси водорода и гипохлорита с ионами двухвалентного железа
|
Fe2+ + H2O2 -> Fe3+ + HO- + HO· (радикал гидроксила) |
|
Fe2+ + ClO- + H+ -> Fe3+ + Cl- + HO· (радикал гидроксила) |
Совокупность продуктов, образуемых активированными клетками-фагоцитами (радикалы супероксида и гидроксила, перекись водорода и гипохлорит) называют активными формами кислорода; некоторые авторы называют гипохлорит и продукты его метаболизма в тканях (такие как хлорамины R-NHCl) называют активными формами хлора. Радикалы гидроксила химически исключительно активны и вызывают повреждение белков, нуклеиновых кислот и липидов биологических мембран. Особенно тяжелые последствия имеют две последние реакции. Радикалы ·OH вызывают разрыв нитей ДНК, обладая, в зависимости от ситуации, мутагенным, канцерогенным или цитостатическим действием. С другой стороны, реагируя с ненасыщенными жирными кислотами, входящими в состав мембранных липидов, радикалы гидроксила инициируют цепную реакцию их пероксидации (перекисного окисления).
БИОЛОГИЧЕСКИЕ ПОСЛЕДСТВИЯ ПЕРОКСИДАЦИИ ЛИПИДОВ
Увеличенное образование свободных радикалов в организме и связанное с этим усиление процессов пероксидации липидов (которое иногда называют "оксидативным стрессом") сопровождается рядом нарушений в свойствах биологических мембран и функционировании клеток. В таблице приведены наиболее важные изменения в мембранных структурах при перекисном окислении липидов.
Таблица Наиболее важные изменения в мембранных структурах при перекисном окислении липидов
|
Действие перекисного окисления на мембранные белки |
Действие перекисного окисления на липидный слой мембран |
|
Окисление тиоловых соединений Повреждение переносчиков Появление проницаемости для ионов Повреждение транспортных АТФаз |
Увеличение микровязкости мембран Изменение поверхностного заряда мембран и липопротеинов Уменьшение гидрофобного объема Увеличение полярности липидной фазы Увеличение проницаемости для ионов водорода Увеличение проницаемости для ионов кальция |
Окисление тиоловых групп мембранных белков
Этот процесс может приводить в результате к неферментативной реакции SH-групп со свободными радикалами липидов; при этом образуются сульфгидрильные радикалы, которые затем взаимодействуют с образованием дисульфидов либо окисляются кислородом с образованием производных сульфоновой кислоты:
|
Pr-SH + L· -> LH + Pr-S· |
|
Pr1-S· + Pr2-S· -> Pr1-SS- Pr2 |
|
Pr-S· + O2 -> Pr-SO2· -> производные сульфоновой кислоты |
Связанное с перекисным окислением липидов окисление белков и образование белковых агрегатов в хрусталике глаза заканчивается его помутнением; этот процесс играет важную роль в развитии старческой и других видов катаракты у человека. Большую роль в патологии клетки играет также инактивация ион-транспортных ферментов, в активный центр которых входят тиоловые группы, в первую очередь Ca2+-АТФазы. Инактивация этого фермента приводит к замедлению "откачивания" ионов кальция из клетки и, наоборот, к входу кальция в клетку, увеличению внутриклеточной концентрации ионов кальция и повреждению клетки. Наконец, окисление тиоловых групп мембранных белков приводит к появлению дефектов в липидном слое мембран клеток и митохондрий. Под действием разности электрических потенциалов на мембранах через такие поры в клетки входят ионы натрия, а в митохондрий - ионы калия. В результате происходит увеличение осмотического давления внутри клеток и митохондрий и их набухание. Это приводит к еще большему повреждению мембран.
Изменение свойств липидного слоя
Увеличение микровязкости мембран
Изменение поверхностного заряда мембран и липопротеинов
Уменьшение гидрофобного объема
Увеличение полярности липидной фазы
Увеличение проницаемости для ионов водорода
Увеличение проницаемости для ионов кальция
Увеличение проницаемости для ионов кальция – второй результат перекисного окисления липидов – связано с тем, что продукты пероксидации обладают способностью непосредственно увеличивать ионную проницаемость липидного бислоя. Так показано, что продукты перекисного окисления липидов делают липидную фазу мембран проницаемой для ионов водорода и кальция. Это приводит к тому, что в митохондриях окисление и фосфорилирование разобщаются, а клетка оказывается в условиях энергетического голода (т.е. недостатка АТФ). Одновременно в цитоплазму выходят ионы кальция, которые повреждают клеточные структуры. Третий (и быть может, самый важный) результат пероксидации – это уменьшение стабильности липидного слоя, что может привести к электрическому пробою мембраны собственным мембранным потенциалом, т.е. под действием разности электрических потенциалов, существующей на мембранах живой клетки. Электрический пробой приводит к полной потере мембраной ее барьерных функций.
КЛЕТОЧНЫЕ СИСТЕМЫ АНТИРАДИКАЛЬНОЙ ЗАЩИТЫ
В нормальных условиях процесс перекисного окисления липидов находится под строгим контролем ферментативных и неферментативных систем клетки, от чего скорость его невелика. Принято делить химические соединения и физические воздействия, влияющие на скорость перекисного окисления липидов, на прооксиданты (усиливают процессы перекисного окисления) и антиоксиданты (тормозят перекисное окисление липидов). К прооксидантам в живой клетке относятся высокие концентрации кислорода (например, при длительной гипербарической оксигенации больного), ферментные системы, генерирующие супероксидные радикалы (например, ксантиноксидаза, ферменты плазматической мембраны фагоцитов и др.), ионы двухвалентного железа. Хотя сам процесс перекисного окисления развивается в виде цепных реакций в липидной фазе мембран и липопротеинов, начальные (а возможно, и промежуточные) стадии этой сложной системы реакций протекают в водной фазе. Часть защитных систем клетки также локализуется в липидной фазе, а часть - в водной фазе. В зависимости от этого можно говорить о водорастворимых и гидрофобных антиоксидантах. В таблице приведены наиболее известные антиоксиданты.
Таблица . Наиболее известные антиоксиданты
|
Антиоксидант |
Действие |
|
Церулоплазмин (плазма крови) |
Окисляет Fe2+ до Fe3+ молекулярным кислородом |
|
Апо-белок трансферрина (плазма крови) |
Связывает Fe3+ |
|
Ферритин (цитоплазма) |
Окисляет Fe2+ и депонирует Fe3+ |
|
Карнозин |
Связывает Fe2+ |
|
Супероксиддисмутазы (повсеместно) |
Удаляет супероксид с образованием пероксида водорода |
|
Каталаза (внутри клеток) |
Разлагает пероксид водорода с выделением кислорода |
|
Глутатион-пероксидазы (в цитоплазме) |
Удаляет пероксид водорода за счет окисления глутатиона Удаляет гидроперекиси липидов |
|
Глутатионредуктаза |
Восстанавливает окисленный глутатион |
|
Токоферол, тироксин, стероиды |
Перехватывают радикалы липидов |
|
Аскорбиновая кислота |
Регенерирует окисляющиеся токоферол и убихинон |
|
Глутатион |
Используется для восстановления пероксидов |
Антиоксиданты водной фазы
Основные реакции в водной фазе, предшествующие цепному окислению, и роль антиоксидантов в ограничении скорости этих процессов можно представить в виде схемы, приведенной на рисунке.

Роль антиоксидантов водной фазы
Непосредственными предшественниками гидроксильного радикала, инициирующего цепное окисление липидов, служат ионы двухвалентного железа и перекись водорода (или образующийся из нее гипохлорит). По этой причине образование радикала гидроксила и пероксидация липидов тормозится веществами, снижающими концентрацию одного из этих двух соединений. К ним относятся:
Фермент супероксиддисмутаза, который снижает концентрацию супероксидных радикалов и тем самым препятствует восстановлению ими ионов трехвалентного железа до двухвалентного. В клетке ионы железа хранятся в трехвалентном состоянии в специальных депо, образованных субъединицами белка ферритина.
Ферменты каталаза и глутатион-пероксидаза, которые удаляют перекись водорода. Эффективность работы глутатион-пероксидазы зависит от концентрации свободного глутатиона, при снижении которой может возрастать концентрация цитотоксических гидроксильных радикалов. Регенерация восстановленного глутатиона (GSH) из окисленного (GSSG) осуществляется за счёт НАДФН; этот процесс катализируется ферментом глутатионредуктазой. Недостаток глутатиона в клетках, например эритроцитах, который может быть обусловлен действием токсических веществ, например ионами тяжелых металлов или наследственным недостатком глутатионредуктазы приводит к активации перекисного окисления; это, в частности, наблюдается при некоторых видах гемолитических анемий.
Соединения, связывающие ионы железа (комплексоны). Надо, правда, оговориться, что в водной фазе некоторые комплексы ионов железа вступают в реакции с супероксидным радикалом и перекисью водорода наряду со свободными ионами железа в растворе.
Антиоксиданты, тормозящие развитие цепных реакций в липидной фазе
Основные реакции в липидной фазе биологических мембран и липопротеинов крови, а также место действия антиоксидантов в ограничении скорости этих процессов можно продемонстрировать с помощью схемы, приведенной на рисунке.:

Антиоксиданты, тормозящие развитие цепных реакций в липидной фазе
Цепные реакции "ведут" свободные радикалы липидов (L· и LOO·), разветвление цепей происходит при взаимодействии продукта пероксидации – гидроперекиси липидов (LOOH) с ионами Fe2+. Все соединения, снижающие концентрацию перечисленных веществ, выполняют функцию антиоксидантов. Сюда относятся:
Ферменты фосфолипаза и глутатионпероксидаза, которые разрушают гидроперекиси липидов, предотвращая разветвление цепей окисления липидов в мембранах. При этом действие фосфолипазы заключается в отщеплении от фосфолипидов окисленной жирной кислоты, содержащей гидроперекисную группу (LOOH), а действие глутатионпероксидазы сводится к восстановлению этой группы до спиртовой с одновременным окислением глутатиона (GSH) до дисульфида (GSSG):
-
LOOH + 2GSH -> LOH + GSSG + H2O
Ловушки радикалов, которые называют иногда "липидными антиоксидантами". По своей химической природе липидные антиоксиданты - это производные фенола. К ним относится a-токоферол (витамин Е), убихинон (коэнзим Q), тироксин и синтетические соединения, например ионол (бутилированный гидрокситолуол) (см. рисунке).