
- •Химическая посуда
- •Приготовление растворов. Титриметрический анализ
- •1. Общие понятия
- •2. Способы выражения концентрации растворов
- •3. Титриметрический анализ
- •3.1. Сущность титриметрического метода анализа
- •3.2. Классификация титриметрических методов
- •3.3. Вычисления в титриметрии
- •3.4. Растворы, применяемые в титриметрии. Приготовление стандартных растворов
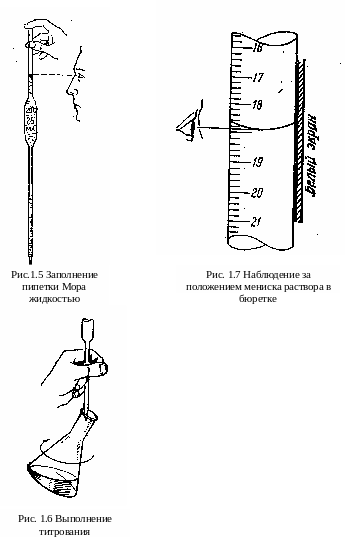
- •3.5. Аппаратура и техника выполнения титриметрического анализа
- •Выполнение работы. Опыт №1. Приготовление раствора заданной процентной концентрации.
- •Требуется приготовить 100 г раствора заданной процентной концентрации определенного вещества и воды (концентрацию и вещество указывает преподаватель).
- •Рассчитывают, какая масса вещества требуется для приготовления 250 мл раствора указанной концентрации. При расчетах учитывают, что щелочи, как правило, содержат 96–98% основного вещества.
- •3.2. Определение концентрации раствора щелочи
Рассчитывают, какая масса вещества требуется для приготовления 250 мл раствора указанной концентрации. При расчетах учитывают, что щелочи, как правило, содержат 96–98% основного вещества.
Пользуясь шпателем, отвешивают в предварительно взвешенном стаканчике расчетное количество щелочи на технохимических весах с точностью до 0,01 г. Осторожно! При попадании на кожу щелочи вызывают ожоги!
Всыпают через воронку взятую навеску в мерную колбу емкостью 250 мл, тщательно смывают оставшиеся кристаллы щелочи дистиллированной водой, не вынимая воронку из горлышка колбы. Навеску в колбе растворяют в малом количестве воды, доливают водой до метки, закрывают пробкой и хорошо перемешивают.
3.2. Определение концентрации раствора щелочи
В чистую коническую колбу пипеткой отбирают 10 мл приготовленного раствора щелочи. Добавляют 2-3 капли раствора метилоранжа и титруют стандартным раствором соляной кислоты до перехода окраски, как описано выше (см. опыт 2). Рассчитывают нормальность раствора и титр.
Контрольные вопросы и задачи.
Дайте определение следующих понятий: раствор, растворитель, насыщенный, ненасыщенный, пересыщенный раствор.
Перечислите способы выражения концентрации растворов. Как вычисляется молярная концентрация и молярная концентрация эквивалента (нормальность)?
Что такое титриметрический анализ? Назовите его достоинства.
Дайте классификацию титриметрических методов: по типу реакций, по приемам титрования.
В чем заключается сущность кислотно-основного титрования?
Как проводятся вычисления в титриметрическом анализе?
О
 пределите
молярную концентрацию эквивалента и
титр раствора HCl,
если на титрование 20 мл 0,5 н раствора
NaOH
было израсходовано 2 мл этого раствора
кислоты.
пределите
молярную концентрацию эквивалента и
титр раствора HCl,
если на титрование 20 мл 0,5 н раствора
NaOH
было израсходовано 2 мл этого раствора
кислоты.

Рис. 1.1. Приготовление
стандартного раствора из фиксанала
Рис. 1.2 Мерные
колбы


Рис. 1.4. Градуированные
пипетки
Рис. 1.3. Пипетки
Мора
Глухарева Н.А., Перистая Л.Ф., Колесникова Е.Н.
РУКОВОДСТВО К ПРАКТИЧЕСКИМ ЗАНЯТИЯМ ПО ОБЩЕЙ ХИМИИ, для студентов медицинского факультета
