
- •Лекция №1. Химия нефти и газа.
- •Лекция №2. Стабилизация нефтяного и газового конденсата.
- •Средние составы потоков установки стабилизации конденсата одного из гпз приведены в табл. 6.2.
- •Лекция №3. Ректификационная колонна.
- •Лекция №4. Вакуумная перегонка нефти.
- •Лекция №5. Каталитический крекинг.
- •Реактор.
- •Регенератор
- •Лекция №6 Газофракционирующие установки.
- •Лекция №7. Термический крекинг.
Лекция №1. Химия нефти и газа.
В основе процессов нефтепереработки лежат законы органической химии. Поэтому, для того, чтобы разобраться в технологии нефтепереработки необходимо вспомнить основные правила и определения химии.
Атом – химически неделимая частица вещества. Атом – электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
Химический элемент – определенный вид атомов с одинаковым зарядом ядра.
Валентность – это способность атома химического элемента (или атомной группы) образовывать определенное число химических связей с другими атомами (или атомными группами). Валентность атома некоторого элемента равна числу атомов водорода (или их эквивалента), с которым этот атом может соединиться.
Вид соединения между двумя атомами называется химической связью. Упрощенно можно считать, что это сила электростатического взаимодействия.
Углеводороды – органические соединения, молекулы которых построены только из атомов углерода и водорода.
Примером, иллюстрирующим три последних определения, может быть метан, который состоит из одного атома углерода и четырех атомов водорода. Валентность метана равна 4.

Метан относится к предельным
углеводородам (алканы) или парафинам
общей формулы
![]() .
Примеры таких углеводородов – пропан,
нормальный бутан (n-бутан)
и нормальный пентан (n-пентан).
.
Примеры таких углеводородов – пропан,
нормальный бутан (n-бутан)
и нормальный пентан (n-пентан).

Рис. 14
Атомы в углеводородах С4Н10 и С5Н12 могут располагаться несколькими способами. Один из способов показан на рисунке 14.
Другой способ - с ответвлением от одного из внутренних атомов углерода, изображен на рисунке 15.

Рис.15
Соединения С4Н10 и С5Н12, которые при этом получаются, являются парафиновыми углеводородами изостроения и называются изобутан и изопентан. Хотя n-бутан и изобутан имеют одинаковые брутто-формулы, их свойства различны. Они кипят при разной температуре, имеют разные плотности, вступают в различные химические реакции.
Другой класс углеводородов – это циклические соединения, содержащие, как правило, больше четырех атомов углерода. Ели цепочку из пяти атомов углерода свернуть в кольцо, получается циклопентан (рисунок 16). Существуют циклы и большего размера, например циклогексан. Этот класс соединений называется нафтенами или нафтеновыми углеводородами.
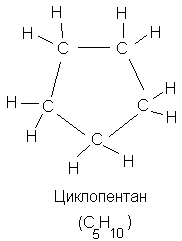
Рис. 16
Существует молекула, в которой есть два атома углерода, связанных двойной связью и четыре атома водорода. Это этилен, химическая формула С2Н4. Двойная связь, удерживающая вместе два атома углерода, менее прочная, чем одинарная. Поэтому этилен – химически неустойчив, и довольно легко вступает в реакцию с другими веществами, превращаясь при этом в соединение, в котором нет двойных связей.

Рис. 17
Этилен принадлежит классу
органических соединений, которые
называются олефины.
Представители олефиновых углеводородов
изображены на рисунке 17. Общая формула
для олефинов
![]() .
Этого вида углеводородов в природе не
существует. Их нет и в сырой нефти, а
появляются они в результате процесса
крекинга.
.
Этого вида углеводородов в природе не
существует. Их нет и в сырой нефти, а
появляются они в результате процесса
крекинга.
Следующий вид органических соединений, используемых в нефтяной промышленности, - это ароматические углеводороды.
Ароматические соединения – это органические соединения, молекулы которых содержат циклы (так называемые бензольные ядра) из шести атомов углерода, участвующих в образовании единой системы сопряженных связей.
Название связано с тем, что первые открытые представители ароматических соединений обладают приятным запахом.
Общая формула ароматических
углеводородов
![]() ,
простейшими представителями являются
бензол, толуол, ксилол (рисунок 18).
,
простейшими представителями являются
бензол, толуол, ксилол (рисунок 18).

Рис. 18
В органической химии наблюдается тенденция: как только число атомов углерода в соединении становится больше шести, число различных комбинаций в структуре возрастает лавинообразно. Поэтому индивидуальным соединениям уделяется очень мало внимания. Чтобы описать состав нефти или нефтепродукта, иногда указывают процентное содержание парафинов, нафтенов и ароматики; эти группы веществ обычно характеризуются соответствующими свойствами (плотность, вязкость, температура кипения и т.д.).
