
- •Инструкция по технике безопасности
- •Порядок проведения работы о составления отчета
- •Погрешности измерений
- •Лабораторная работа №1 Измерение атмосферного давления
- •Общие положения
- •Проведение эксперимента и обработка результатов
- •Порядок выполнения работы и обработка результатов
- •Контрольные вопросы и задания
- •Лабораторная работа № 4 Измерение удельной теплоты плавления льда
- •Лабораторная работа № 5 Измерение удельной теплоемкости и удельной теплоты плавления парафина.
- •Порядок выполнения работы
- •3 Предохранительный клапан; 4 манометр; 5,8 термометры; 6,7 вентили; 9 калориметр; 10 весы
- •Контрольные вопросы
- •Библиографический список
Проведение эксперимента и обработка результатов
После ознакомления с опытной установкой необходимо заготовить форму журнала наблюдений, записать температуру и давление окружающей среды, измеренное по барометру, а затем приступить к проведению измерений. При этом необходимо иметь в виду, что плотность системы следует считать удовлетворительной только в том случае, когда нет заметного изменения вакуума или избыточного давления в сосуде 5 при закрытых кранах 3, 4, 6 и скорость изменения давления не превышает 3-5 мм вод. ст. в минуту.
Результаты измерений заносим в таблицы 1.1 и 1.2
Таблица 1.1
Дата испытания |
Барометрическое давление Рб,Па |
Температура окружающего воздуха tB,°C |
|
|
|
Таблица 1.2
№ измерения
|
Показания Uобразного манометра, мм вод. ст. |
|||||
Измерение разряжения |
Измерение избыточного давления |
|||||
Левое колено |
Правое колено |
h вид |
Левое колено |
Правое колено |
h вид |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Обработка результатов опыта включает определение значений абсолютных давлений в сосуде 5 при различных заполнениях его водой и перевод этих значений во все, встречающиеся в практике единицы измерения давления.
Результаты расчетов сводятся в таблицу
№ измерения |
мм.вод.ст |
Па |
мм.рт.ст. |
бар |
1 атм. (физ) |
1 атм. (техн) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Контрольные вопросы
Какое влияние на показания барометра оказывает температура окружающей среды (при постоянном давлении)?
Является ли избыточное давление и давление разряжения параметрами состояния?
Какая связь между единицами измерения давления?
Лабораторная работа № 3
Определение отношения теплоемкостей газа методом Клемана и Дезорма
Цель работы
Определить экспериментально отношение молярных теплоемкостей газа при постоянном давлении и постоянном объеме и сравнить с теоретическим значением данного отношения, найденным из молекулярно-кинетической теории.
Теоретическое введение и описание лабораторной установки
В стеклянном сосуде 1 (рис.3.1) находится воздух под давлением РА. Заполнение сосуда воздухом производят через трубку от источника сжатого воздуха, в качестве которого используется груша. С помощью кранов З и 4 сосуд попеременно заполняют либо с атмосферой, либо с источником сжатого воздуха, либо U-образным водяным манометром. Атмосферное давление определяется по барометру. Избыточное давление в сосуде замеряют U-образным водяным манометром 2 (ни масса, ни объем газа не меняются).
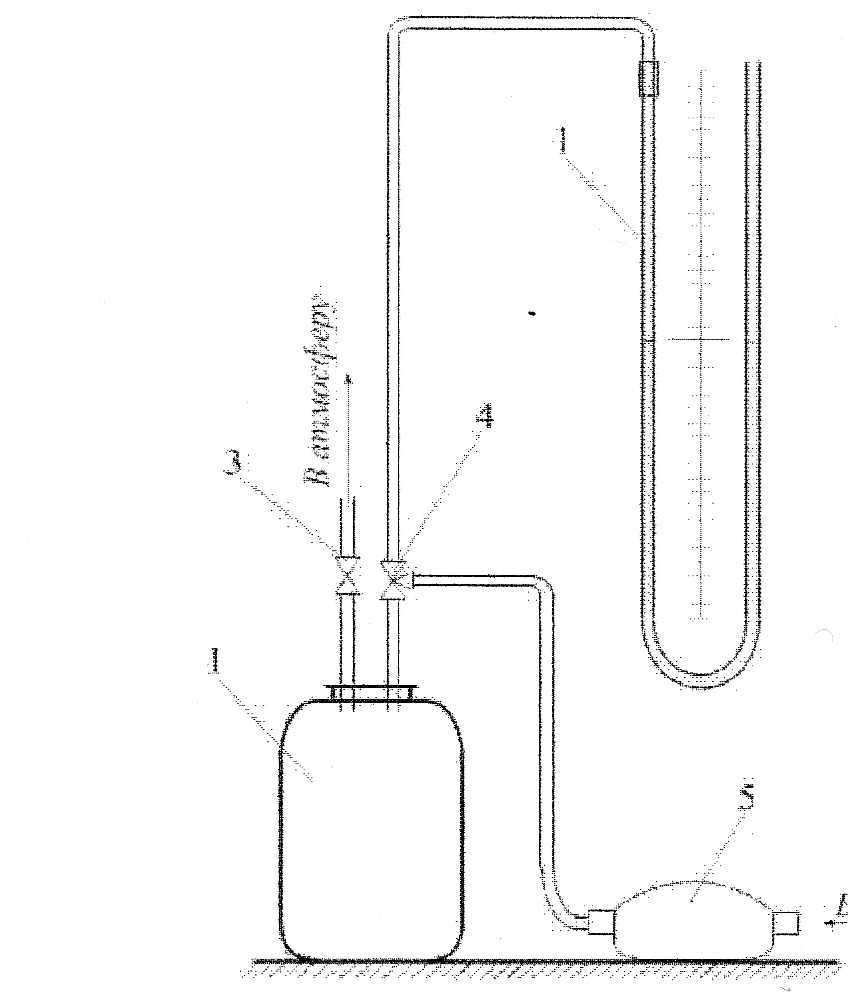
Рис.3.1.Схема экспериментальной установки:
1- стеклянный сосуд; 2 – U образный манометр; 3,4 – краны; 5 – насос.
Переход из первого, состояния во второе (адиабатический процесс) описывается уравнением Пуассона:
![]() где
где
![]()
показатель адиабаты.
показатель адиабаты.
Сравнивая конечное, третье состояние газа с первым, видим, что температура газа в этих состояниях одинакова, следовательно, к этому переходу применим закон Бойля-Мариотта
P1V1=P2V2.
Решая систему двух уравнений Пуассона и БойляМариотта, можно определить γ. Для этого возведем второе уравнение в степень γ разделим его на первое уравнение:

Так
как V2=V3,
то
![]() или
или
 Логарифмируя последнее выражение,
получим
Логарифмируя последнее выражение,
получим
![]()
![]() .
Обозначим разность уровней жидкости в
манометре в первом состоянии h1,
а в третьем состоянии - h3.
Тогда P1=P0+h1,
P3=P0+h3,
(P2=P0)
и
.
Обозначим разность уровней жидкости в
манометре в первом состоянии h1,
а в третьем состоянии - h3.
Тогда P1=P0+h1,
P3=P0+h3,
(P2=P0)
и
![]() .
.
В
данном случае h1
и h3
намного меньше Р0,
поэтому отношение разности логарифмов
можно заменить отношением разности
чисел, т.е.
![]() Это дает расчетную формулу для нашего
опыта
Это дает расчетную формулу для нашего
опыта
![]() .
.
В
молекулярно-кинетической теории молярные
теплоемкости газа Сp
и Сv
определяются
через число степеней свобода молекулы
i и универсальную газовую постоянную
R:
![]() Найдем их отношение
Найдем их отношение
![]() .
.
В данном случае воздух не очищается от влаги и содержит большое количество паров воды, поэтому число степеней свободы будет соответствовать трехатомным молекулам, т.е. i = 6.
