
- •Введение
- •Основные признаки острого воспаления
- •Этиология воспаления
- •Патогенез воспаления
- •Альтерация
- •Медиаторы воспаления
- •Виды медиаторов воспаления
- •1. Клеточные медиаторы:
- •Клеточные медиаторы воспаления
- •Плазменные медиаторы воспаления
- •Экссудация
- •Причины выхода жидкой части крови из сосудов (экставазация)
- •Экссудат
- •Значение экссудации при воспалении
- •Эмиграция
- •Фагоцитоз
- •Пролиферация
- •Исходы воспаления
- •Виды воспаления
- •Течение воспаления
- •Роль реактивности в воспалении
- •Роль нервной и эндокринной системы
- •Роль эндокринной системы
- •Теории воспаления
- •Значение воспаления для организма
Экссудат
Экссудат – жидкость, выходящая при воспалении из сосудов в ткань. Термины «экссудат» и «экссудация» употребляются только по отношению к воспалению. Они призваны подчеркнуть отличие воспалительной жидкости (и механизма ее образования) от тканевой жидкости и транссудата – невоспалительного выпота (при невоспалительных отеках, например, при хронической сердечной недостаточности). Экссудат в отличие от транссудата содержит большое количество белка (более 2 – 3%) и, как правило, ФЭК.
Виды экссудата. В зависимости от качественного состава различают следующие виды экссудатов.
• Серозный экссудат – полупрозрачная жидкость, богатая белком (до 2–3%), содержит небольшое количество клеток крови (лейкоциты, Эр.). Чаще всего серозный экссудат наблюдается при ожоговом, вирусном, аллергическом воспалении.
• Фибринозный экссудат содержит большое количество фибриногена, что является результатом значительного повышения проницаемости сосудов. Фибринозный экссудат может формироваться при дифтерии, дизентерии, туберкулезе.
• Гнойный экссудат – мутная густая жидкость, содержащая до 6–8% белка, большое количество полиморфно-ядерных лейкоцитов (главным образом погибших и разрушенных – «гнойные тельца»); ферментов; продуктов аутолиза тканей. Характерен для воспалительных процессов, вызванных кокковой инфекцией, патогенными грибками или химическими флогогенами (такими как скипидар, отравляющие вещества).
• Геморрагический экссудат характеризуется большим содержанием эритроцитов, что придает ему розовый или красный цвет. Характерен для туберкулезных поражений (туберкулезный плеврит), чумы, сибирской язвы, черной оспы, токсического гриппа, аллергического воспаления, т.е. для воздействия высоковирулентных агентов, бурно протекающего воспаления, сопровождающегося значительным повышением проницаемости сосудов.
• Гнилостный экссудат отличается наличием продуктов гнилостного разложения тканей, вследствие чего имеет грязно-зеленую окраску и дурной запах. Любой вид экссудата может приобрести гнилостный (ихорозный) характер при внедрении в очаг воспаления гнилостной микрофлоры (анаэробов, например, синегнойной палочки).
• Смешанные экссудаты наблюдаются при воспалении, протекающем на фоне ослабленных защитных сил организма и присоединения вследствие этого вторичной инфекции. Различают серозно-фибринозный, серозно-гнойный, серозно-геморрагический, гнойно-фибринозный экссудаты.
Состав экссудата (химический и клеточный) зависит: от причины воспаления; ткани, в котором развивается воспаление; реактивности организма.
Значение экссудации при воспалении
В очаге воспаления значение процесса экссудации имеют двоякое биологическое значение: адаптивное и патогенное (рис. 9).
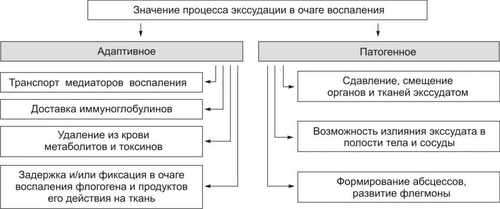
Рис. 9. Значение процесса экссудации в очаге воспаления
Эмиграция
Эмиграция (лат. emigrati – выселяться, переселяться) – переход лейкоцитов из кровеносных сосудов в ткань (при воспалении – очаг воспаления). Процесс эмиграции лейкоцитов совершается и в норме, но при воспалении приобретает большие масштабы.
Биологическое значение: в очаге воспаления должно появиться достаточное количество клеток-эффекторов воспаления – лейкоцитов.
Пусковым моментом активации лейкоцитов является воздействие на рецепторы клеточных мембран разнообразных хемотаксических агентов, высвобождаемых микроорганизмами или фагоцитами, а также образующихся в ткани в результате действия воспалительного агента или под влиянием самих фагоцитов.
Процесс эмиграции лейкоцитов последовательно проходит этапы:
• краевого стояния лейкоцитов,
• адгезии лейкоцитов к эндотелию,
• проникновения лейкоцитов через сосудистую стенку,
• направленного движения лейкоцитов в очаг воспаления.
Стадия краевого стояния лейкоцитов (маргинация) – это переход лейкоцитов из циркулирующего пула в пристеночный (маргинальный). На этой стадии условно выделяют 2 этапа.
• Выход лейкоцитов из осевого цилиндра кровяного потока и приближение к стенке микрососуда, обращенной в сторону очага воспаления. Причина: действие хемоаттрактантов, замедление тока крови (вследствие развития венозной гиперемии).
• Медленное движение лейкоцитов вдоль стенки микрососуда по поверхности клеток эндотелия (rolling – роллинг). Причины: экспрессия молекул адгезии (селектинов) клетками эндотелия и лейкоцитами под действием хемоаттрактантов, рецепторное взаимодействие лейкоцитов и активированного эндотелия. Селектины обеспечивают слабую адгезию лейкоцитов к эндотелию, в результате движение лейкоцитов замедляется, но они не приклеиваются к эндотелию.
Адгезия (прилипание) лейкоцитов к мембранам эндотелиальных клеток микрососудов. Причины: адгезия лейкоцитов к эндотелию обеспечивается молекулами адгезии – интегринами и иммуноглобулиноподобными молекулами клеточной адгезии (Ig-подобные, ICAM).
Значение адгезии – создает условия для трансмиграции лейкоцитов через стенку сосуда. У человека выявлены заболевания обусловленные дефицитом молекул адгезии лейкоцитов или рецепторов к ним. У таких больных нарушены механизмы воспаления, это приводит к частым инфекциям, несмотря на нормальное или даже повышенное содержание лейкоцитов в периферической крови.
Выход лейкоцитов из просвета сосудов через сосудистую стенку в очаг воспаления реализуется через эндотелий и базальную мембрану микрососуда. Нейтрофилы и моноциты проходят через эндотелий по межэндотелиальным щелям. Они выпускают свои псевдоподии в пространства между эндотелиоцитами и «раздвигают» клетки.
Преодоление базальной мембраны может быть обусловлено двумя механизмами. Первый механизм состоит в явлении тиксотропии – при контакте нейтрофила с базальной мембраной её коллоиды переходят из состояния геля в состояние золя (происходит разжижение мембраны). Нейтрофил легко проходит через золь, после чего золь обратно превращается в плотный гель. Второй механизм заключается в выделении нейтрофилами протеаз (эластазы, коллагеназы), которые расщепляют волокнистые компоненты базальной мембраны.
Направленное движение лейкоцитов в очаг воспаления – таксис (от греч. taxis – порядок). Без таксиса не было бы воспаления, т.к. лейкоциты не собирались бы в одном месте, а рассредоточивались по ткани.
Хемотаксиc – направленное движение лейкоцитов под влиянием химических раздражителей – хемоаттрактантов. Лейкоциты при воспалении активно перемещаются в строго определенном направлении – в сторону максимальной концентрации притягивающих их веществ – хемоаттрактантов (лат. attractio – притяжение).
Экзогенные хемоаттрактанты: микробы, микробные продукты (ЛПС, липотейхоевые кислоты, эндо- и экзотоксины).
Эндогенные хемоаттрактанты: цитокины (хемокины); калликреин, активатор плазминогена (ф.Хагемана); С3а,С5а-фракция комплемента; лейкотриены; простагландины и др.
Электротаксиc – движение лейкоцитов несущих на своей поверхности отрицательный заряд по направлению к эпицентру очага воспаления, где накапливаются положительно заряженные частицы – электротаксины (ионы H+, K+, Mg2+ и др.), формирующие положительный заряд.
Механизмы таксиса.
• Скопление хеморецепторов (кэппинг) на стороне лейкоцита, обращённой к региону наибольшей концентрации хемотаксинов (хемоаттрактантов). Этот полюс («голова») лейкоцита становится ведущим, а хвостовой – ведомым.
• Изменение коллоидного состояния цитозоля лейкоцита: переход из состояния геля в состояние золя.
• Снижение поверхностного натяжения на обращённой в сторону очага воспаления области мигрирующего лейкоцита («головной» полюс), что стимулирует перемещение цитозоля лейкоцита именно в головной конец. Поверхностное натяжение снижается под влиянием ВЖК, катионных белков и внеклеточных катионов, накапливающихся при воспалении.
• Сокращение актиновых микрофиламентов хвостового полюса и перестройка других структур цитоскелета лейкоцитов.
• Выталкивание цитозоля к головному концу и движение лейкоцита в очаг воспаления.
• Движению лейкоцита в очаг воспаления способствует ток жидкой части крови из просвета микрососудов через их стенки в интерстиций (по градиенту фильтрационного, осмотического и онкотического давления).
Последовательность эмиграции лейкоцитов в очаг острого воспаления: сначала в очаге воспаления появляются нейтрофильные гранулоциты, затем моноциты/макрофаги, позднее лимфоциты. Гранулоциты могут наблюдаться уже к 10-й мин от начала воспаления. Количество их достигает максимума через 4-6 ч (в этот период лейкоциты в очаге воспаления представлены нейтрофилами более чем на 90%). Моноциты обычно преобладают в очаге острого воспаления спустя 16-24 ч и достигают максимума, как правило, на 3-и сутки.
В процессе завершения воспаления в очаге наблюдается постепенное исчезновение сначала нейтрофильных гранулоцитов, затем – моноцитов и лимфоцитов.
Причина очередности эмиграции лейкоцитов – стадийность появления факторов хемотаксиса и адгезии.
Значение эмиграции: в очаге воспаления должно появиться достаточное количество клеток-эффекторов воспаления – лейкоцитов.
