
- •Расчетно–графическая работа № 1 Термодинамический расчет газового цикла
- •1. Задание
- •1.1. Общие положения
- •1.2. Содержание задания
- •2. Исходные данные и варианты к расчетно-графической работе
- •3. Расчет термодинамического газового цикла
- •Параметры состояния идеального газа в характерных точках цикла
- •Приближенные значения мольных теплоемкостей при постоянном объеме и постоянном давлении ( ) [ ]
- •Расчет термодинамических процессов газового цикла
- •4. Анализ эффективности цикла
- •1. Задание
- •4. Расчет
- •Параметры состояния в характерных точках газового цикла
- •Калорические параметры процессов газового цикла
- •1. Расчет промежуточных точек процессов 1-2 и 4 -5 в pv-диаграмме (рис. 2):
- •Молекулярные массы и плотности некоторых газов при нормальных условиях
- •Физические свойства сухого воздуха (давление 1,013·105 Па)
- •Физические свойства воды на линии насыщения
- •Физические свойства водяного пара на линии насыщения
Калорические параметры процессов газового цикла
Процессы |
l, кДж/кг |
∆u, кДж/кг |
q , кДж/кг |
∆h , кДж/кг |
∆S, кДж/(кг·К) |
1 – 2 |
- 478,61 |
0 |
- 478,61 |
0 |
- 0,598 |
2 – 3 |
0 |
523,43 |
523,43 |
733,08 |
0,453 |
3 – 4 |
207,74 |
523,01 |
730,78 |
732,42 |
0,371 |
4 – 5 |
1183,14 |
0 |
1183,14 |
0 |
0,492 |
5 – 1 |
0 |
- 1046,5 |
- 1046,5 |
- 1465,5 |
- 0,718 |
Проверка |
|
|
|
|
|
3. Анализ эффективности цикла
Определение подведенного количества теплоты
q1 = q2-3 + q3-4 + q4-5 =523,43 + 730,78 +1183,14 = 2437,35 кДж/кг.
Определение отведенного количества теплоты
q2 = q1-2 + q5-1 = 478б,61 + 1046,5 = 1525,11 кДж/кг.
Работа цикла
l0 = q0 = q1 – q2 = 2437,35 – 1525,11 = 912,24 кДж/кг.
Термический КПД цикла
![]() =
(
=
(![]() )
. 100%
= (
)
. 100%
= (![]() )
. 100%
= 37,4 %.
)
. 100%
= 37,4 %.
4. Построение в масштабе газового цикла

Рис.2
1. Расчет промежуточных точек процессов 1-2 и 4 -5 в pv-диаграмме (рис. 2):
Точка 1’
Задаемся
![]() = 2 м3/кг;
= 2 м3/кг;
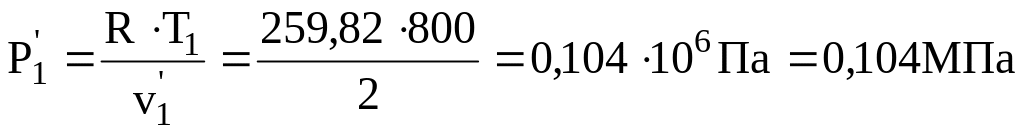 ;
;
Точка 1”
Задаемся
v”
= 1 м3/кг;
![]() ;
;
Точка 1’”
Задаемся
![]() = 0,5 м3/кг;
= 0,5 м3/кг;
![]() ;
;
Точка 4’”
Задаемся
![]() =
0,5 м3/кг;
=
0,5 м3/кг;
![]() ;
;
Точка 4”
Задаемся
![]() = 1 м3/кг;
= 1 м3/кг;
![]() ;
;
Точка 4’
Задаемся
![]() =2
м3/кг;
=2
м3/кг;
![]() .
.

Рис. 3
2. Расчет промежуточных точек процессов 2 - 3, 3 - 4 и 5 – 1 в диаграмме Тs (рис. 3):
Точка 2’
Задаемся
T=1000
K;
 ;
;
Точка 3’
Задаемся
T=2000
K;
 ;
;
Точка 5’
Задаемся
T=2000
K;
 ;
;
Точка 5”
Задаемся
T=1000
K;
![]() .
.
Приложение 3
Таблица 7
Молекулярные массы и плотности некоторых газов при нормальных условиях
Вещество
|
Химическое обозначение |
Молекулярная масса , кг/к моль |
Плотность , кг/м3 |
Воздух |
— |
28,96 |
1,293 |
Кислород |
О2 |
32,00 |
1,429 |
Азот |
N2 |
28,026 |
1,251 |
Водород |
H2 |
2,016 |
0,090 |
Окись углерода |
CO |
28,01 |
1,250 |
Двуокись углерода |
CO2 |
44,01 |
1,977 |
Таблица 8
Физические свойства сухого воздуха (давление 1,013·105 Па)
t, 0C |
, кг/м3 |
Cp, кДж/кгК |
102, Вт/мК |
α106, м2/с |
106, Пас |
106, м2/с |
Pr, |
0 |
1,293 |
1,005 |
2,44 |
18,7 |
17,2 |
13,28 |
0,707 |
10 |
1,247 |
1,005 |
2,51 |
20,0 |
17,6 |
14,16 |
0,705 |
20 |
1,205 |
1,005 |
2,59 |
21,4 |
18,1 |
15,06 |
0,703 |
30 |
1,165 |
1,005 |
2,67 |
22,9 |
18,6 |
16,00 |
0,701 |
40 |
1,128 |
1,005 |
2,76 |
24,3 |
19,1 |
16,96 |
0,699 |
50 |
1,093 |
1,005 |
2,83 |
25,7 |
19,6 |
17,95 |
0,698 |
60 |
1,060 |
1,005 |
2,90 |
27,2 |
20,1 |
18,97 |
0,696 |
70 |
1,029 |
1,009 |
2,96 |
28,6 |
20,6 |
20,02 |
0,694 |
80 |
1,00 |
1,009 |
3,05 |
30,2 |
21,1 |
21,09 |
0,692 |
90 |
0,972 |
1,009 |
3,13 |
31,9 |
21,5 |
22,10 |
0,690 |
100 |
0,946 |
1,009 |
3,21 |
33,6 |
21,9 |
23,13 |
0,688 |
120 |
0,898 |
1,009 |
3,34 |
36,8 |
22,8 |
25,45 |
0,686 |
140 |
0,854 |
1,013 |
3,49 |
40,3 |
23,7 |
27,80 |
0,684 |
160 |
0,815 |
1,017 |
3,64 |
43,9 |
24,5 |
30,09 |
0,682 |
180 |
0,779 |
1,022 |
3,78 |
47,5 |
25,3 |
32,49 |
0,681 |
200 |
0,746 |
1,026 |
3,93 |
51,4 |
26,0 |
34,85 |
0,680 |
250 |
0,674 |
1,038 |
4,27 |
62,8 |
27,4 |
40,61 |
0,677 |
300 |
0,615 |
1,047 |
4,60 |
71,4 |
29,7 |
48,33 |
0,674 |
350 |
0,566 |
1,059 |
4,91 |
81,9 |
31,4 |
55,46 |
0,676 |
400 |
0,524 |
1,068 |
5,21 |
96,3 |
33,0 |
63,09 |
0,678 |
Таблица 9
