
- •1 Механика
- •1.1 Основные понятия, законы и формулы
- •1.2 Примеры решения задач
- •Решение
- •Решение
- •Решение.
- •1.3 Задачи для самостоятельного решения
- •2. Молекулярная физика и термодинамика
- •2.1. Постоянные величины
- •2.2.Основные обозначения
- •2.3. Основные понятия, законы и формулы
- •Относительные атомные массы а (округленные значения) некоторых химических элементов
- •2.3 Примеры решения задач
- •Решение
- •Решение.
- •Решение.
- •Решение
- •Решение
- •Решение.
- •Решение
- •2.4 Задачи для самостоятельного решения
- •3. Электростатика. Постоянный ток.
- •3.1 Основные понятия и формулы.
- •Решение.
- •Решение
- •Решение
- •Решение
- •3.3.Методические указания к решению задач.
- •3.4. Задачи для самостоятельного решения
- •4. Магнетизм
- •4.1 Основные понятия и формулы
- •4.2 Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •4.3 Задачи для самостоятельного решения
- •5 Оптика
- •5.1 Основные понятия и формулы
- •5 .2 Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •5.3 Задачи для самостоятельного решения
- •6 Физика микромира
- •6.1 Основные понятия и формулы
- •6.2 Справочные таблицы
- •Основные физические постоянные
- •Масса и энергия покоя некоторых частиц
- •Периоды полураспада радиоактивных изотопов
- •Массы атомов легких изотопов
- •6.3 Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •6.4 Задачи для самостоятельного решения
- •Список использованной литературы
- •1.Учебники.
- •2.Сборники задач.
- •Приложения
- •1.Порядок выбора варианта и требования к оформлению контрольной работы.
- •Определение варианта по шифру
- •2.Таблицы заданий на контрольные работы по вариантам бакалавриат
- •Специалисты
- •Специальности поз, позс
- •Специальности пгсз, пгсзс
- •Содержание
Решение.
Учитывая, что четырехатомная молекула метана (СН4) имеет 6 степеней свободы (i3= 6), запишем формулу для средней кинетической энергии его молекулы:
3
=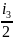 kT
=
kT
=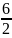 kT.
kT.
Tемпературу газовой смеси найдем из формулы средней квадратичной скорости молекулы азота:

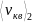 =
=
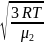 Т =
Т =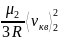
Молярная масса азота (N2): = 28-10~3 кг/моль.
Внутренняя энергия газовой смеси складывается из энергии каждого газа в отдельности:
U
= U
1
+
U2
+ U3
=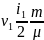 RT+
v2
RT+
v2
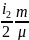 RT+
RT+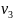
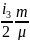 RT
=
RT
=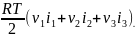
где i1 = 3 - число степеней свободы одноатомной молекулы неона,
i2 = 5 - число степеней свободы двухатомной молекулы азота,
i3 = 6 - число степеней свободы трехатомной молекулы метана.
Внутренняя энергия молекулы неона Ul целиком приходится на поступательное движение, так как одноатомная молекула не имеет вращательных степеней свободы.
Двухатомная молекула имеет две вращательные степени свободы(i2вращ=2),
а многоатомная - три (i3вращ =3). Поэтому часть внутренних энергий U2 и U3
приходящихся на вращательное движение :
U2(вращ)
= v2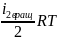 ;
U3
(вращ) =
v3
;
U3
(вращ) =
v3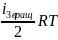 .
.
Внутренняя энергия газовой смеси, приходящаяся на вращательное движение, определяется формулой
U
(вращ)=
U2(вращ)
+ U3(вращ)
=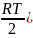 +
+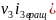
Поделив U(вpащ) на U, найдем долю энергии, приходящуюся на вращательное движение:
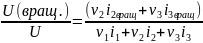
Произведем вычисления:
T
=
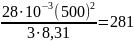 K
K
( )3 = 3 1,38 10-23 281 = 1,1 6 10-20Дж.
U
=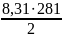 (0,l
3
+ 0,6
5
+ 0,3
6;
= 5955 Дж = 5,955 кДж.
(0,l
3
+ 0,6
5
+ 0,3
6;
= 5955 Дж = 5,955 кДж.
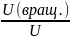 =
=
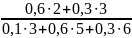 =
0,41
=
0,41
Пример 4
Эффективный диаметр молекулы азота d = 3 l0-10 м. Найти при нормальных условиях (р = 1атм = 1,01 5Па; Т= 273 К):
1) концентрацию молекул п ;
2) среднюю арифметическую скорость молекул ;
среднее число столкновений молекулы в 1 с ;
среднюю длину свободного пробега молекул ;
коэффициент диффузии D ;
коэффициент внутреннего трения .
Дано: d = 3 10-'°м; р = 1 атм = 1,01 105 Па; Т=273 К
Найти: п; ; (z); ; D; .
Решение
Концентрацию молекул находим из формулы р = пkТ':
n
=
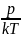
Искомые величины определяем из формул:
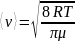 ;
=
n
;
=
;
D=
;
=
;
=
n
;
=
;
D=
;
=
 .
.
Учтем, что плотность азота
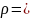 т0п=
т0п=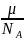 п
п
а молярная масса азота (N2) = 2 14 10-3 = 28 10-3 кг/моль. Подставляя числовые данные, рассчитаем искомые величины:
n
=
=
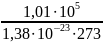 =
2,68
1025
1/м3;
=
2,68
1025
1/м3;
=
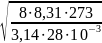 =454 м/с;
=454 м/с;
=
n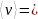
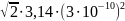 2,68
1023
454
= 4,86
109
1/c;
2,68
1023
454
= 4,86
109
1/c;
=
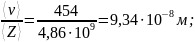
D=
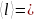
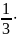 454
454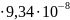 = 1,41
= 1,41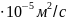 ;
;
т0п=
п
=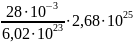 =
1,25
=
1,25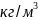 ;
;
=
=
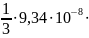 454
454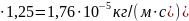 .
.
Пример 5.
Для
уменьшения тепловых потерь воздух
между стенками термоса откачали
до очень низкого давления. Начиная с
какого значения р'
коэффициент
теплопроводности воздуха уменьшался
при дальнейшей откачке?
Расстояние между стенками термоса
х
= 6 мм, температура
воздуха
t
= 17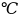 ,
эффективный
диаметр молекулы d
= 3
10-10
м.
,
эффективный
диаметр молекулы d
= 3
10-10
м.
Дано: х = 6 мм = 6 10-3 м; Т = 17 + 273 = 290 К; d = 3 10-10м.
Найти: р'.
