
- •1 Механика
- •1.1 Основные понятия, законы и формулы
- •1.2 Примеры решения задач
- •Решение
- •Решение
- •Решение.
- •1.3 Задачи для самостоятельного решения
- •2. Молекулярная физика и термодинамика
- •2.1. Постоянные величины
- •2.2.Основные обозначения
- •2.3. Основные понятия, законы и формулы
- •Относительные атомные массы а (округленные значения) некоторых химических элементов
- •2.3 Примеры решения задач
- •Решение
- •Решение.
- •Решение.
- •Решение
- •Решение
- •Решение.
- •Решение
- •2.4 Задачи для самостоятельного решения
- •3. Электростатика. Постоянный ток.
- •3.1 Основные понятия и формулы.
- •Решение.
- •Решение
- •Решение
- •Решение
- •3.3.Методические указания к решению задач.
- •3.4. Задачи для самостоятельного решения
- •4. Магнетизм
- •4.1 Основные понятия и формулы
- •4.2 Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •4.3 Задачи для самостоятельного решения
- •5 Оптика
- •5.1 Основные понятия и формулы
- •5 .2 Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •5.3 Задачи для самостоятельного решения
- •6 Физика микромира
- •6.1 Основные понятия и формулы
- •6.2 Справочные таблицы
- •Основные физические постоянные
- •Масса и энергия покоя некоторых частиц
- •Периоды полураспада радиоактивных изотопов
- •Массы атомов легких изотопов
- •6.3 Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •6.4 Задачи для самостоятельного решения
- •Список использованной литературы
- •1.Учебники.
- •2.Сборники задач.
- •Приложения
- •1.Порядок выбора варианта и требования к оформлению контрольной работы.
- •Определение варианта по шифру
- •2.Таблицы заданий на контрольные работы по вариантам бакалавриат
- •Специалисты
- •Специальности поз, позс
- •Специальности пгсз, пгсзс
- •Содержание
Относительные атомные массы а (округленные значения) некоторых химических элементов
Элемент |
Символ |
|
Элемент |
Символ |
А |
Азот |
N |
14 |
Натрий |
Na |
23 |
Аргон |
Аr |
40 |
Неон |
Ne |
20 |
Водород |
Н |
1 |
Ртуть |
Hg |
201 |
Гелий |
Не |
4 |
Углерод |
C |
12 |
Кислород |
О |
16 |
Хлор |
Cl |
35 |
2.3 Примеры решения задач
Пример 1.
Определить массу молекулы, количество вещества и число молекул в капле воды объемом 6 мм3. Плотность воды равна 1000 кг/м .
Дано: V= 6мм3=6×10 -9м3; = 103 кг/м3.
Найти: т0, v, N.
Решение
Учитывая, что молекула воды Н2О содержит 2 атома водорода и 1 атом кислорода, найдем относительную молекулярную массу воды:
М = 2АН+АО = 2∙1 + 16 = 18,
где АН =1 и АО =16 - относительные атомные массы водорода и кислорода ( см. табл.2.1).
Масса молекулы воды равна
т0 = М × а.е.м. = 18 ∙ 1,66 ∙ 10-27 кг 3 ∙10-26 кг.
Масса капли т, число молекул в капле N и количество вещества v
определяются но формулам:
т =
V
; N=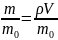 ;
v
=
;
v
=
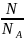 .
.
Вычисляем т, N и v :
т
= 103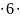 10-9
=
6
10-9
=
6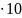 -6кг ;
N
=
-6кг ;
N
=
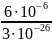 =
2∙
1020кг;
=
2∙
1020кг;
v
=

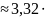 10-4
моль.
10-4
моль.
Пример 2.
Баллон содержит 6 г гелия и 160 г аргона. Давление смеси составило 760 мм.рт.ст., а температура равна 300 К. Определить объем баллона.
Дано:
т1
=
16 10-3
кг; т2
=160
10-3
кг;
=
760 мм.рт.ст.; Т
=
300 К.
10-3
кг; т2
=160
10-3
кг;
=
760 мм.рт.ст.; Т
=
300 К.
Найти: V.
Решение.
По закону Дальтона давление смеси газов равно
p = p1 + p2 (1)
где р1 и p2 - парциальные давления гелия и аргона.
Воспользовавшись уравнением Менделеева-Клапейрона, находим р1 и р2 :
р1
=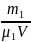 RT;
p2
=
RT;
p2
=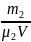 RT
RT
где
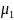 и
и
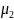 -
молярные массы гелия и аргона. Подставляя
р1
и р2
в формулу
(1), получаем
-
молярные массы гелия и аргона. Подставляя
р1
и р2
в формулу
(1), получаем
р=
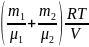 ,
,
откуда находим объем баллона
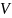 =
=
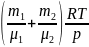 .
.
Учитывая, что инертные газы гелий и аргон - одноатомные и воспользовавшись табл.2.1., находим их относительные молекулярные массы :
М1=АНе= 4; . М2=ААr= 40.
Тогда молярные массы гелия и аргона равны :
= 4 10-3 кг/моль; = 40 10-3 кг/моль;
Выражаем давление смеси газов в паскалях, имея в виду, что 1 мм рт.ст. = 133,3 Па:
р = 760 мм.рт.ст. = 760 133,3 Па = 1,01 105 Па
Вычисляем искомый объем:
V
=
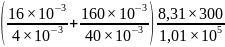 =
0,197 м3.
=
0,197 м3.
Пример 3.
В сосуде находится газовая смесь, состоящая из v1 = 0,1 моля неона,
v2 = 0,6 моля азота (N2) и v3 = 0,3 моля метана (СH4). Средняя квадратичная скорость молекулы азота =500 м/с.Определить:
среднюю кинетическую энергию 3 молекулы метана;
внутреннюю энергию U газовой смеси;
долю энергии, приходящуюся на вращательное движение молекул.
Дано: v1= 0,1 моль; v2 = 0,6 моль; v3 = 0,3 моль; 2 = 500 м/с.
Найти: 3 ; U, Uвращ/U .

 А
А