
- •1 Уровни организации белковых молекул. Аминокислотный составбелков.
- •2 Олигомерные белки. Гемоглобин. Миоглобин.
- •3 Физико-химические св-ва белков.
- •4 Лабильность. Денатурация. Прионы.
- •5 Основные св-ва белковых фракций крови и их классификация.
- •6 Глобулярные и фибрилярные белки
- •7 Хромопротеины
- •8 Нуклеиновые кислоты
- •9 Вторичная структура днк и рнк
- •12 Витамин в1 (тиамин)
- •13 Тиаминпирофосфат
- •14 Витамин в12, представление о его химическом строении. Биологическая роль, основные пищевые источники.
- •18 Пантотеновая кислота (в5)
- •19. Фолиевая кислота и ее коферментная форма. Биологическое значение ее.
- •20 Кофакторы ферментов: ионы металлов и коферменты. Коферментные функции витаминов.
- •21 Никотиновая кислота, ее химическое строение и биологическая роль. Основные пищевые источники никотиновой кислоты.
- •21 Витамин в2 (рибофлавин)
- •22 Витамин а, его химическое строение и роль в обмене веществ клеток. Основные пищевые источники витамина а.
- •23 Витамины группы д, их строение и физиологическая роль.
- •24. Аскорбиновая кислота, ее строение и роль в метаболизме.
- •25 Витамин е. Его химическое строение и физиологическое значение.
- •26 Витамин к, его строение и физиологические функции
- •27 История открытия и изучения ферментов Особенности ферментативного катализа. Различия ферментного состава органов и тканей. Органоспецифичные ферменты.
- •29 Специфичность действия ферментов. Зависимость скорости ферментативных реакций от температуры, pH, концентрации фермента и субстрата.
- •30 Классификация ферментов, и ее принципы:
- •31 Зависимость скорости ферментативной реакции от концентрации субстрата. Графики Михаэлиса-Ментен и Лайнуивера-Бэрка. Медико-биологическое значение константы Михаэлиса.
- •34, 37Классификация ферментов, и ее принципы:
- •36 Ингибирование ферментативной активности и его виды. Медико-биологическое значение ингибирования.
- •38 Эндоэнергетические и экзергонические реакции в живой клетке.
- •40 Биологическое значение цтк
- •45 Дыхательная цепь митохондрий, ее локализация в клетке, строение и основные принципы функционирования.
- •48 Токсичность кислорода.
- •50 Иерархия регуляторных систем.
- •51. Механизм действия гормонов.
- •53 Г. Задней доли гипофиза.
- •54. Гомоны надпочечников: Кортикостероиды(корковое вво).
- •55 Эстрогены
- •56 Андрогены
- •57. Прогестерон.
- •59. Гормоны мозгового в-ва надпочечников
- •60. Гормоны щитовидной железы.
- •62,63 Углеводы, в общем. Гликолипиды и гликопротеиды. Гомо- и гетерополисахариды.
- •64 Глюкоза – важнейший метаболит углеводного обмена.
- •65 Наследственные нарушения обмана моносахаридов и дисахаридов.
- •66 Аэробный распад глюкозы. Физиологическое значение аэробного распада глюкозы. Использование глюкозы для синтеза жиров в печени и в жировой ткани.
- •67 Глюкозо-6-фосфат, схема путей его образования и использования в организме
- •68 Синтез гликогена и гликогенолиз. Биологическое значение и регуляция этих процессов и роль печени в их реализации.
- •69Пути синтеза полисахаридов. Роль утф в синтезе полисахаридов. Регуляция синтеза и распада полисахаридов. Гликогенозы и биохимические механизмы их возникновения.
- •71 Гликогенолиз и его биологическое значение.
- •70 Свойства и строение гликогена. Биосинтез гликогена. Мобилизация гликогена и его гормональная регуляция.
- •73 Молочнокислое брожение, последовательность реакций, энергетический выход, биологическое значение.
- •75 Окислительное декарбоксилирование пвк и роль этого процесса в клеточном метаболизме. Пируват как ключевой метаболит в превращениях углеводов, аминокислот и жирных кислот.
- •76 Взаимопревращение углеводов и его роль в клеточном метаболизме.
- •78 Глюкозо-лактатный и глюкозо-аланиновый циклы.
- •80 Челночные механизмы транспорта восстановительных эквивалентов из цитоплазмы в митохондрии. Химизм, медико-биологическое значение.
- •82 Представление о пентозофосфатном пути превращения глюкозы. Его роль в метаболизме клеток. Окислительные реакции (до стадии рибулозо-5-фосфата).
- •83 Пентозофосфатный путь превращения глюкозы в эритроцитах и жировой ткани. Значение этого пути для данного вида тканей. Особенности протекания в пролиферирующих клетках.
- •85 Классификация сфинголипидов, их физико-химическое строение и физиологическая роль. Представление о сфинголипидозах.
- •86 Пищевые жиры и их переваривание. Всасывание продуктов переваривания. Нарушения переваривания и всасывания. Биосинтез триглицеридов, локализация этого процесса в клетке и его значение.
- •87 Ненасыщенные жирные кислоты, их физико-химические свойства и значение для клеток. Незаменимые липидные факторы питания.
- •88 Липидный состав мембран - фосфолипиды, гликолипиды, холестерин. Роль липидов в формировании липидного бислоя. Латеральная диффузия липидов и белков. Участие фосфолипаз в обмене фосфолипидов.
- •89 Распад и синтез триацилглицеринов: химизм, биологическое значение и регуляция.
- •90 Представление о биосинтезе и катаболизме фосфолипидов и гликолипидов. Функции фосфолипидов и гликолипидов. Сфинголипидозы.
- •91 Образование желчных кислот и их роль в переваривании жиров. Конъюгирование желчных кислот, первичные и вторичные желчные кислоты. Связь с обменом холестерина. Строение желчных кислот.
- •93 Химическое строение гликолипидов и их биологическая роль.
- •94 Окисление ненасыщенных жирных кислот, метаболические особенности этого процесса.
- •97 Биосинтез кефалина и лецитина и их биологическая роль. Липотропные факторы.
- •99 Холестерин как предшественник других стероидов. Биохимические основы развития атеросклероза.
- •100 Ресинтез триацилглицеринов в стенке кишечника. Образование хиломикронов и транспорт жиров. Роль аполипопротеинов в составе хиломикронов. JIипопротеинлипаза.
- •101 Краткая характеристика липопротеидов крови. Роль апопротеинов в функционировании липопротеидов. Диагностическое значение определения липопротеинов в клинике.
- •102 Хиломикроны, их физико-химическая характеристика и физиологическое значение.
- •104 Роль печени в липидном обмене.
- •108 Типы дезаминирования аминокислот и их значение в клеточном обмене. Непрямое дезаминирование, химизм процесса, стадии, биологическое значение.
- •109 Цикл мочевины. Связь орнитинового цикла с превращениями фумаровой и аспарагиновой кислот. Нарушения синтеза и выведения мочевины. Гипераммониемии.
- •110 Трансаминирование, химизм процесса, специфичность аминотрансфераз. Диагностическое значение определения аминотрансфераз.
- •111 Пути обезвреживания аммиака в организме. Цикл мочевинообразования. Механизмы обезвреживания аммиака в печени; в нервной и мышечной ткани.
- •112Глицин, его строение и роль в обмене веществ. Основные пути метаболизма глицина. Глицин как важнейший донор углеродных фрагментов для биосинтезов.
- •113 Аспарагиновая и глутаминовая кислоты, строение, роль в метаболизме основные пути метаболизма, биологическое значение глутатиона.
- •114 Строение аргинина и гистидина. Их роль в обмене веществ.
- •116 Роль цистеина и метионина в обмене веществ. Липотропные факторы. S-аденозилметионин, как липотропный фактор.
- •117Роль лизина и аргинина в клеточном метаболизме.
- •118 Роль тирозина в метаболизме человека и животных.
- •120 Строение днк эукариотических клеток и механизмы, лежащие в основе ее пространственной упаковки. Многообразие азотистых оснований. Функции нуклеиновых кислот в живых организмах.
- •121 Генетический код и его характеристика. Молекулярные механизмы возникновения наследственных болезней. Краткое описание процесса трансляции.
- •122 Строение рибосом прокариот и эукариот. Роль рибосом в биосинтезе белка.
- •123 Синтез белка на рибосомах. Условия необходимые для реализации этого процесса.
- •125 Распад пуриновых оснований. Химизм процесса и его медико-биологическое значение. Подагра.
- •126 Представления о распаде и биосинтезе пиримидиновых нуклеотидов.
- •127 Распад гема. Образование и пути выделение билирубина. Желтухи, диагностика. Характеристика распада гемоглобина в неонатальном периоде. Физиологическая желтуха новорожденных.
- •132 Обмен веществ: питание, метаболизм и выделение продуктов метаболизма. Состав пищи человека. Органические и минеральные компоненты. Основные и минорные компоненты.
- •128 Биосинтез гема и его регуляция. Химизм реакций до порфобилиногена, представление о дальнейших путях синтеза гема. Порфирии.
- •129 Взаимосвязь обмена углеводов, липидов и белков.
- •130 Незаменимые факторы питания и их медико-биологическое значение. Необходимость оптимального обеспечения детского организма незаменимыми факторами питания.
- •131 Основные пищевые вещества: углеводы, жиры, белки; суточная потребность, переваривание; частичная взаимозаменяемость при питании.
118 Роль тирозина в метаболизме человека и животных.
Роль тирозина в метаболизме.
Фенилаланин - незаменимая аминокислота, так как в клетках животных не синтезируется её бензольное кольцо. Тирозин - условно заменимая аминокислота, поскольку образуется из фенилаланина. Содержание этих аминокислот в пищевых белках (в том числе и растительных) достаточно велико. Кроме использования в синтезе белков, тирозин в разных тканях выступает предшественником таких соединений, как катехоламины, тироксин, меланины, и ка-таболизируется до СО2 и Н2О. В пигментных клетках (меланоцитах) тирозин выступает предшественником тёмных пигментов - меланинов. Среди них преобладают 2 типа: эумеланины и феомеланины. Эумеланины (чёрного и коричневого цвета) - нерастворимые высокомолекулярные гетерополимеры 5,6-дигидроксииндола и некоторых его предшественников. Феомеланины - жёлтые или красновато-коричневые полимеры, растворимые в разбавленных щелочах. Находятся они, в основном, в составе волос. Меланины присутствуют в сетчатке глаз. В щитовидной железе синтезируются и выделяются гормоны йодтиронины: тироксин (тет-райодтиронин) и трийодтиронин. Эти гормоны представляют собой йодированные остатки тирозина, которые попадают в клетки щитовидной железы через базальную мембрану.В мозговом веществе надпочечников и нервной ткани тирозин является предшественником катехоламинов (дофамина, норадреналина и адреналина). При образовании катехоламинов, которое происходит в нервной ткани и надпочечниках, и меланина в меланоцитах промежуточным продуктом служит диоксифенилаланин (ДОФА) .
119 Химическое строение триптофана и пути его метаболизма. Химическое строение триптофана и пути его метаболизма.
Триптофан - незам. АК, явл. предш. важных биологически актт. в-в, в т.ч. серотонина и рибонуклеотида никотиновой к-ты. Один из его метаболитов - индолуксусная к-та - ростстимулирующий фактор растений. Триптофан окисляется по кинурениновому пути или по серотониновому пути. Кинурен. путь приводит к синтезу НАД . Триптофан под дейст. триптофан2,3диоксигеназы превращ. в формилкинуренин, который под действием формамидазы распадается на муравьиную к-ту и кинуренин, к-й ок-ся в 3-оксикинуренин. 3-оксикинуренин превращ в хинолиновую к-ту - предш. рибонуклеотида никотиновой к-ты.
120 Строение днк эукариотических клеток и механизмы, лежащие в основе ее пространственной упаковки. Многообразие азотистых оснований. Функции нуклеиновых кислот в живых организмах.
Строение ДНК эукориотических клеток и механизмы лежащие в основе ее пространственной упаковки.
Структурными единицами нукл кислот явл нуклеотиды,сост из азотист основания,углевода(заним центр место) и фосфорной к-ты. Нуклеозиды- соединения, сост из остатка азотистого основания и углевода — рибозы (рибонуклеозиды) или дезоксирибозы (дезоксирибонуклеозиды):
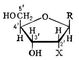
ДНК — Дезоксирибонуклеиновая к-та. Сахар — дезоксирибоза, азотистые основания: пуриновые — гуанин (G), аденин (A), пиримидиновые — тимин (T) и цитозин (C).
ДНК часто состоит из двух полинуклеотидных цепей, направленных антипараллельно
Нуклеотиды. –сложн ысокомолекулярн соедин,обеспеч хранение,передачу наследств инфы и реализацию этой инфы.Их структурные компоненты выполн фу-ию кофакторов,аллостерич эффекторов,вход в состав коферментов, приним участие в обмене ве-в и Э.
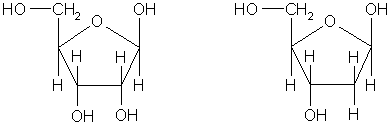
β-рибоза β-дезоксирибоза (C5H10O5) (C5H10O4)
Азотистые основания : пиримидиновые (цитозин,урацил,тимин) и пуриновые (аденин, гуанин)
Структурными единицами нукл кислот явл нуклеотиды,сост из азотист основания,углевода(заним центр место) и фосфорной к-ты. Нуклеозиды- соединения, сост из остатка азотистого основания и углевода — рибозы (рибонуклеозиды) или дезоксирибозы (дезоксирибонуклеозиды):
Каждый нуклеотид содержит 3 химически различных компонента: гетероциклическое азотистое основание, моносахарид (пентозу) и остаток фосфорной к-ты. В состав нуклеиновых к-т входят азотистые основания двух типов: пуриновые - аденин (А), гуанин (G) и пиримидиновые - цитозин (С), тимин (Т) и урацил (U). Пентоза представлена дезоксирибозой. Пентозу соединяет с основанием N-гликозидная связь, образованная С1-атомом пентозы и N1 -атомом пиримидина или N9-aтомом пурина. Нуклеиновые кислоты, в мономеры которых входит дезоксирибоза, называют дезоксири-бонуклеиновыми кислотами, или ДНК. В молек. ДНК - аденин (А), тимин (Т), гуанин (G) и цитозин (С). Каждая молекула ДНК упакована в отдельную хромосому. Компактизация и суперспирализация ДНК осуществляются с помощью разнообразных белков, взаимодействующих с определёнными последовательностями в структуре ДНК. Все связывающиеся с ДНК эукариотов белки можно разделить на 2 группы: гисгоновые и негистоновые белки. Комплекс белков с ядерной ДНК клеток называют хроматином. Гистоны - белки с молекулярной массой 11-21 кД, содержащие много остатков аргинина и лизина. Благодаря положительному заряду гистоны образуют ионные связи с отрицательно заряженными фосфатными группами, расположенными на внешней стороне двойной спирали ДНК. Существует 5 типов гистонов. Четыре гистона Н2А, Н2В, НЗ и Н4 образуют октамерный белковый комплекс (Н2А, Н2В, НЗ, Н4)2, который называют "нуклеосомный кор". Молекула ДНК "накручивается" на поверхность гистонового октамера, совершая 1,75 оборота. Такой комплекс гистоновых белков с ДНК служит основной структурной единицей хроматина, её называют "нуклеосома". ДНК-связ. негист. белки. К этой группе относят семейство сайт-специфических белков типа "цинковые пальцы", гомодимеры, белки высокой подвижности, ферменты репликации, транскрипции и репарации.
