
- •Основные понятия и законы химии. Современные представления о строении атома.
- •Строение атома.
- •Квантовые числа электронов
- •Периодический закон и периодическая система д.И. Менделеева в свете учения строения атома.
- •Определение, виды, условия образования, природа химической связи.
- •Ковалентная связь
- •Ионная связь
- •Металлическая связь
- •Гибридизация орбиталей
- •Определение, механизм образования, свойства ковалентной связи. Валентность. Степень окисления.
- •Оксиды. Определение, классификация, номенклатура, свойства и способы получения.
- •Химические свойства Основные оксиды
- •Кислотные оксиды
- •Амфотерные оксиды
- •Получение
- •Кислоты: определение, классифиакация, номенклатура, свойства и способы получения.
- •Основания: определение, классифиакация, номенклатура, свойства и способы получения.
- •Соли: определение, классификация ,номенклатура, свойства и способы получения.
- •Комплексные соединения: определение, строение по а.Вернеру, типы, номенклатура.
- •Классификация
- •По заряду комплекса
- •]По числу мест, занимаемых лигандами в координационной сфере
- •По природе лиганда
- •Номенклатура
- •Скорость химической реакции. Факторы, влияющие на скорость химической реакции.
- •Условия, влияющие на скорость химических реакций
- •Необратимые и обратимые химические реакции. Химическое равновесие. Принцип Ле-Шателье. Констранта равновесия.
- •Окислительно-восстановительные реакции: определение, основные понятия, сущность окисления и восстановления, важнейшие окислители и восстановители реакции.
- •Дисперсионые системы: определение, классификация. Грубодисперсные системы: суспензии, аэрозоли, эмульсии.
- •Коллоидные растворы: определение, свойства, получение, строение мицелл.
- •Истинные растворы: определение, основыне понятия, сущность процесса растворения. Диффузия. Осмос. Осмотическое давление.
- •Основные положения теории электролитической диссоциации. Механизм электролитической диссоциации. Степень и константа диссоциации.
- •Диссоциация кислот, оснований, солей. Диссоциация воды рН-показатель.
- •Сущность гидролиза. Гидролиз различных типов солей. Степень гидролиза.
- •Общая характеристика элементов главной подгруппы VII группы. Медико-биологическое значение галогенов.
- •20 Хлор, хлороводород и соляная кислота. Получение, свойства. Хлориды
- •Получение.
- •Химические свойства.
- •21. Кислородные соединения хлора.
- •Общая характеристика халькогенов. Кислород и его соединения. Медико-биологическое значение кислорода.
- •Кислород, его общая характеристика и нахождения в природе
- •Получение кислорода
- •Химические свойства
- •Фториды кислорода
- •Биологическая роль кислорода
- •Свойства соединений кислорода с водородом (вода, пероксид водорода). Применение н2о2 в медицине. Значение воды.
- •24.Сера. Аллотропия свободной серы. Химические свойства серы. Сероводород. Сероводородная кислота и ее соли.
- •Природные минералы серы
- •Физические свойства
- •Химические свойства
- •Биологическая роль
- •Физические свойства
- •Химические свойства
- •Сульфиды
- •Получение
- •Соединения, генетически связанные с сероводородом
- •Применение
- •Биологическая активность
- •25. Физические и химические свойства оксидов серы, сернистой и серной кислот, солей сернистой, серной кислот, их применение.
- •Получение
- •]Химические свойства
- •Применение
- •Физиологическое действие
- •Химические свойства
- •Применение
- •Физические и физико-химические свойства
- •Химические свойства
- •Свойства сульфитов
- •Качественные реакции
- •26. Общая характеристика элементов главной подгруппы V группы. Азот и его свойства.
- •Азот. Получение
- •Химические свойства, строение молекулы
- •Промышленное связывание атмосферного азота
- •Соединения азота
- •27. Свойства аммиака и солей аммония. Применение в медицине и фармации.
- •Химические свойства
- •Комплексообразование
- •Биологическая роль
- •Физиологическое действие
- •Применение
- •Получение
- •Аммиак в медицине
- •28. Оксиды азота. Азотистая кислота и ее соли. Физические и химические свойства, применение. Список оксидов
- •N(no2)3Тринитрамид
- •N4oНитрозилазид
- •]Воздействие на организм
- •Химические свойства
- •Получение
- •Применение
- •Физиологическое действие
- •29. Физические и химические свойства азотной кислоты. Нитраты. Медико – биологическое значение азота и его соединений.
- •Физические и физико-химические свойства
- •Химические свойства
- •Нитраты
- •30. Характеристика элемента 15 р. Свободный фосфор: аллотропия, физические и химические свойства, получение.
- •Физические свойства
- •31.Фосфин. Оксиды фосфора и фосфорные кислоты: свойства, получение. Медико-биологическое значение фосфора.
- •Физические свойства
- •]Получение
- •Химические свойства
- •Токсичность
- •Получение
- •Применение
- •Значение фосфора
- •32. Общая характеристика элементов IV группы главной подгруппы. Углерод: строение и физические свойства аллотропов углерода, химические свойства.
- •Физические свойства
- •Графит и алмаз
- •Фуллерены и углеродные нанотрубки
- •Аморфный углерод (строение)
- •Нахождение в природе
- •Химические свойства
- •Неорганические соединения
- •Органические соединения
- •Применение
- •33. Кислородные соединения углерода: строение молекул, физические и химические свойства. Медико- биологическое значение углерода и его соединений.
- •34. Кремний и его соединения: нахождение в природе, получение, физические и химические свойства. Медико - биологическое значение кремния.
- •Нахождение в природе
- •Получение
- •Физические свойства
- •Химические свойства
- •Биологическая роль
- •35. Главная подгруппа III группы: общая характеристика элементов. Бор и его соединения: получение, физические и химические свойства, применение в медицине.
- •36. Алюминий и его соединения: получение, физические и химические свойства. Медико-биологическое значение алюминия.
- •Получение
- •38. Щелочные металлы: общая характеристика, получение, свойства, важнейшие соединения. Медико-биологическое значение.
- •Общая характеристика щелочных металлов
- •Химические свойства щелочных металлов
- •Получение щелочных металлов
- •Соединения щелочных металлов Гидроксиды
- •Карбонаты
- •39. Общая характеристика d- элементов. Металлы побочной подгруппы I группы. Соединения меди, серебра. Медико- биологическое значение.
- •Химические свойства Возможные степени окисления
- •Простое вещество
- •Соединения меди(I)
- •Химические свойства
- •40. Металлы побочной подгруппы II группы: общая характеристика строения, физические и химические свойства. Медико- биологическое значение
- •Химические свойства:
- •41. Побочные подгруппы VI,VII группы: общая характеристика элементов подгруппы, свойства хрома, марганца и их соединений. Медико- биологическое значение.
- •Получение
- •42. Побочная подгруппа VIII группы: общая характеристика элементов подгруппы, свойства железа и его соединений. Медико-биологическое значение.
- •Получение металлов подгруппы железа
Физические свойства
Углерод существует во множестве аллотропных модификаций с очень разнообразными физическими свойствами. Разнообразие модификаций обусловлено способностью углерода образовывать химические связи разного типа.
Изотопы углерода
Природный углерод состоит из двух стабильных изотопов — 12С (98,93 %) и 13С (1,07 %) и одного радиоактивного изотопа 14С (β-излучатель, Т½= 5730 лет), сосредоточенного в атмосфере и верхней части земной коры. Он постоянно образуется в нижних слоях стратосферы в результате воздействия нейтронов космического излучения на ядра азота по реакции:14N (n, p) 14C, а также, с середины 1950-х годов, как техногенный продукт работы АЭС и в результате испытания водородных бомб.
На образовании и распаде 14С основан метод радиоуглеродного датирования, широко применяющийся в четвертичной геологии и археологии.
Аллотропные модификации углерода
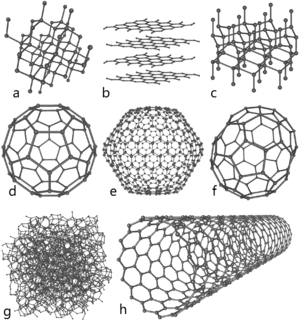
Схемы строения различных модификаций углерода a: алмаз, b: графит, c: лонсдейлит, d: фуллерен — бакибол C60, e: фуллерен C540, f: фуллерен C70, g: аморфный углерод, h: углеродная нанотрубка
Кристаллический углерод
Алмаз, Графен, Графит, Карбин, Лонсдейлит, Наноалмаз, Фуллерены, Фуллерит, Углеродное волокно, Углеродные нановолокна, Углеродные нанотрубки
Аморфный углерод
Активированный уголь, Древесный уголь, Ископаемый уголь: антрацит, Кокс каменноугольный, нефтяной, Стеклоуглерод, Техуглерод, Сажа, Углеродная нанопена
На практике, как правило, перечисленные выше аморфные формы являются химическими соединениями с высоким содержанием углерода, а не чистой аллотропной формой углерода.
Кластерные формы
Астралены
Диуглерод
Структура
Электронные орбитали атома углерода могут иметь различную геометрию, в зависимости от степени гибридизации его электронных орбиталей. Существует три основных геометрии атома углерода.
тетраэдрическая, образуется при смешении одного s- и трех p-электронов (sp3-гибридизация). Атом углерода находится в центре тетраэдра, связан четырьмя эквивалентными σ-связями с атомами углерода или иными в вершинах тетраэдра. Такой геометрии атома углерода соответствуют аллотропные модификации углерода алмаз и лонсдейлит. Такой гибридизацией обладает углерод, например, в метане и других углеводородах.
тригональная, образуется при смешении одной s- и двух p-электронных орбиталей (sp2-гибридизация). Атом углерода имеет три равноценные σ-связи, расположенные в одной плоскости под углом 120° друг к другу. Не участвующая в гибридизации p-орбиталь, расположенная перпендикулярно плоскости σ-связей, используется для образования π-связи с другими атомами. Такая геометрия углерода характерна для графита, фенола и др.
дигональная, образуется при смешении одного s- и одного p-электронов (sp-гибридизация). При этом два электронных облака вытянуты вдоль одного направления и имеют вид несимметричных гантелей. Два других р-электрона дают π-связи. Углерод с такой геометрией атома образует особую аллотропную модификацию — карбин.
