
- •1. История развития учения о биологическом окислении
- •2. Современные представления о биологическом окислении (тканевом дыхании)
- •3. Строение первичной дегидрогеназы. Окисленная и восстановленная формы.
- •4. Строение вторичной дегидрогеназы. Окисленная и восстановленная формы.
- •Строение окисленных форм фад и фмн
- •5. Особенности строения убихинона. Его роль.
- •6. Роль цитохромов в биологическом окислении. Цитохромоксадаза, особенности строения.
- •7. Процесс окислительного фосфорилирования.
- •8. Хемиосмотическая теория митчелла
1. История развития учения о биологическом окислении
Изучение процессов окисления в организме было начато в XVIII веке А. Лавуазье. Он обратил внимание на наличие известного сходства между процессами горения органических веществ вне организма и дыханием животных. Лавуазье считал, что сущность процесса дыхания состоит в соединении кислорода вдыхаемого воздуха с углеродом и водородом органических веществ внутри тела. После работ Лавуазье в науке в течение долгого времени господствовало мнение о тождестве явлений горения и медленного окисления питательных веществ в организме. Вместе с тем было ясно, что биологическое окисление протекает при весьма необычных условиях: при низкой температуре (температура тела), без появления пламени (как это бывает при горении) и, наконец, в присутствии воды, содержание которой обычно достигает в тканях 75 — 80\% от общей массы. Причину столь своеобразного течения окислительных процессов в живых организмах ученые вначале пытались объяснить «активацией» кислорода в клетках организма. Одна из первых теорий биологического окисления, связанных с «активацией» кислорода, была развита А. Н. Бахом.
1. Теория активации кислорода (А.Н.Бах). Согласно этой теории непосредственным агентом, окисляющим субстрат является активированный кислород. Активация молекуляр ного кислорода осуществляется особыми ферментами оксигеназами и ведет к образованию реакционноспособных пероксидов, которые при участии ферментов пероксидаз и взаи модействуют с субстратом.

В дальнейшем оказалось, что действительно в клетках существует ферменты, способные активировать молекулярный кислород и использовать его для окисления ряда веществ. Су ществуют ферменты монооксигеназы, которые присоединяют к субстрату один атом кисло рода (SH +1/2 O2 → SOH ) и диоксигеназы, которые присоединяют к субстрату 2 атома ки слорода (S + O2 → SO2). Монооксигеназы и диоксигеназы катализируют реакции гидрокси лирования стероидов, ксенобиотиков, образование простагландинов и лейкотриенов, но не принимают участия в процессах биологического окисления в митохондриях.
2.Теория активации водорода (Палладин, Украина). По этой теории, биологическое окисление может происходить путем дегидрирования субстрата и без участия кислорода, но при помощи коферментов – акцепторов водорода, т.е. окисление на первых этапах может происходить и в анаэробных условиях, а затем может идти при участии кислорода в аэроб ных условиях, в результате чего образуются молекулы воды.

3.Виланд подтвердил теорию Палладина, и показал, что окисление спиртов и гидратных форм альдегидов принципиально возможно и в отсутствии свободного кислорода (до этого считалось, что только кислород способен оторвать атомы водорода от вещества).
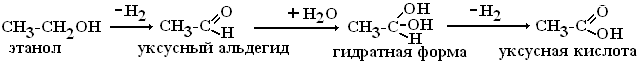
2. Современные представления о биологическом окислении (тканевом дыхании)
Процесс тканевого дыхания обеспечивается содержащимся во всех без исключения клетках организма набором ферментов, составляющих дыхательную цепь ферментов. Начало процесса окисления осуществляется ферментами, непосредственно реагирующими с субстратом и получившими название дегидрогеназ. Субстратом может быть любое из окисляющихся в тканях органических соединений (углеводы, жиры, белки и различные промежуточные продукты, их расщепления). Окисляемый субстрат (суб. Нг) при участии различных специфических (реагирующих лишь с определенным субстратом) дегидрогеназ подвергается окислению (дегидрированию): соответственно величине их окислительно-восстановительного потенциала (см. общую схему цепи дыхательных ферментов). Из всех цитохромов только цитохром а3 способен передавать свои электроны на кислород, восстанавливая его, в связи с этим он получил название цитохромоксидазы — фермента, непосредственно реагирующего с молекулярным кислородом.
Суммируя все реакции цепи дыхательных ферментов, опустив при этом промежуточные переносчики протонов и электронов, получим
Создается впечатление, что кислород присоединяется прямо к субстрату. К такому написанию часто прибегают для обозначения процесса окисления в сокращенном виде, но это справедливо лишь по валовому результату, в действительности же механизм этого процесса, как мы в этом убедились, совсем иной.
Дыхательная цепь ферментов может и удлиняться, и укорачиваться. Некоторые ферменты, например флавиновые, способны взаимодействовать с субстратом, минуя зависимые дегидрогеназы, и цепь окисления такого субстрата будет короче. Количество функционирующих в цепи цитохромов может изменяться, отчего длина цепи дыхательных ферментов также будет различной. Но, как бы то ни было, перенос электронов в цепи дыхательных ферментов всегда является процессом многоступенчатым. Это, по-видимому, следует расценивать как одно из важнейших эволюционных приобретений живых организмов. Проходя через длинную цепь дыхательных ферментов, электроны отдают свою энергию постепенно. При этом энергия выделяется не одномоментно, как это имеет место при окислении (горении) на воздухе, а небольшими порциями, что создает благоприятные возможности для высокой степени ее аккумуляции.
Значительная часть энергии, освобождаемой электронами, запасается в форме энергии фосфатных связей АТФ (см. раздел 5.2), которая образуется в реакции фосфорилирования — в результате присоединения неорганического фосфата к АДФ (АДФ): энергия окисления.

Схема превращения энергии в живых клетках: тканевое дыхание, образование АТФ и пути его использования.
