
- •Российский Химико-Технологический Университет
- •1. Оценка экономического ущерба от загрязнения атмосферы
- •2. Оценка экономического ущерба от загрязнения водных объектов
- •3. Оценка экономического ущерба от загрязнения поверхности почвы твердыми отходами
- •Внедрение природоохранных мероприятий
- •Очистка от пыли нетоксичных металлов и их оксидов.
- •Очистка газов от диоксида серы
- •Очистка газов от диоксида азота
- •Очистка от неорганических веществ
Внедрение природоохранных мероприятий
Очистка газообразных выбросов.


Очистка от сточных вод.
Очистка от
сульфат-ионов
Очистка от Cd
Очистка от пыли нетоксичных металлов и их оксидов.
Для обезвреживания пылей и туманов используют сухие, мокрые и электрические методы. В основе работ сухих аппаратов лежат гравитационные, инерционные и центробежные механизмы осаждения или фильтрационные механизмы. В мокрых пылеуловителях осуществляется контакт запыленных газов с жидкостью, при этом осаждение происходит на капли, на поверхность газовых пузырей или на пленку жидкости. В электрофильтрах отделение заряженных частиц аэрозоля происходит на осадительных электродах.
Зависимость аппарата для улавливания частиц от их размера.
Размер частиц, мкм |
Аппараты |
Размер частиц, мкм |
Аппараты |
40-1000 |
Пылеосадительные камеры |
20-100 |
Скрубберы |
20-1000 |
Циклоны диаметром 1-2 м. |
0,9-100 |
Тканевые фильтры |
5-1000 |
Циклоны диаметром 1 м. |
0,01-100 |
Электрофильтры |
Наиболее эффективными являются фильтры. В основе работы всех фильтров лежит процесс фильтрации газа через перегородку, в ходе которого твердые частицы задерживаются, а газ полностью проходит через нее.
Рукавный фильтр представляет собой металлический шкаф, разделенный вертикальными перегородками на секции, в каждой из которых размещена группа фильтрующих рукавов. Верхние концы рукавов заглушены и подвешены к раме, соединенной с встряхивающим механизмом. Внизу имеется бункер для пыли со шнеком для ее выгрузки.
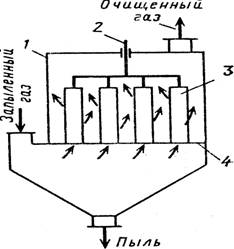 Рукавный
фильтр: 1
– корпус; 2
– встряхивающее
устройство; 3 – рукав; 4 – распределительная
решетка.
Рукавный
фильтр: 1
– корпус; 2
– встряхивающее
устройство; 3 – рукав; 4 – распределительная
решетка.
Очистка газов от диоксида серы
Для очистки отходящих газов от диоксида серы предложено большое количество хемосорбционных методов, применение нашли только некоторые из них. Это из-за того, что объёмы отходящих газов велики, а концентрации SO2 в них малы, газы характеризуются большой температурой и значительным содержанием пыли. Для абсорбции могут быть использованы вода, водные растворы и суспензии солей щелочных и щелочноземельных металлов.
Наиболее эффективны известковый и известняковый методы
Основные химические реакции, протекающие при взаимодействии SО2 с пульпой гидроксида кальция или известняка, описываются следующими уравнениями:
CaO + H2O à Сa(OH)2
Ca(OH)2 + СO2 à СаСО3 + H2O
CaCO3 + CO2 + H2O à Са(НСО3)2
Са(НСО3)2 + SO2 + H2O à CaSO3 * 2 H2O + 2 СO2
CaSO3 * 2 H2O + 1/2 О2 à CaSO4 * 2 H2O
Очистка газов от диоксида азота
Каталитическое восстановление
Одним из основных, хорошо освоенных промышленных методов очистки отходящих газов от оксидов азота является их восстановление на катализаторе до молекулярного азота. При использовании неселективного катализатора восстановитель расходуется не только на восстановление азота, но и вступает во взаимодействие с кислородом, обычно содержащимся в газовом потоке. В качестве восстановителя применяются водород, природный газ, оксид углерода и др. Катализаторами обычно служат элементы платиновой группы. Температура процесса колеблется от 400 до 800оС.
Наиболее широкое распространение получило селективное каталитическое восстановление оксидов азота аммиаком:
6 NO + 4NH3 à 5 N2 + 6 H2О,
6 NO2 + 8NH3 à 7 N2 + 12 H2O.
Процесс восстановления протекает при 200-3600С, степень очистки составляет 96-98,5%. Основным недостатком метода является необходимость точного дозирования аммиака, что при переменном составе отходящих газов (меняется концентрация оксидов азота) практически невозможно. При недостатке аммиака происходит проскок оксидов азота, а при избытке – проскок аммиака, и отходящие газы загрязняются токсичными соединениями.
Карбамидный метод
Карбамидный метод позволяет очищать дымовые газы от оксидов азота на 95% и практически полностью удалять оксиды серы из них. Процесс не требует предварительной подготовки газов, в результате очистки образуются нетоксичные продукты - N2, СО2, Н2О и (NH4)2SO4. Эффективность метода практически не зависит от колебаний входных концентраций оксидов азота и серы.
В общем виде процесс описывается приведенными ниже уравнениями реакций:
NO + NO2 + (NH2)2CO à 2 Н2О + СО2 + 2 N2,
SO2 + (NH2)2CO + 2 Н2О + 1/2 О2 à (NH4)2SO4 + СО2
