
- •Содержание
- •Введение § 1. Предмет и задачи токсикологической химии, ее связь с другими дисциплинами
- •§ 2. Краткий исторический очерк возникновения и развития отечественной токсикологической химии
- •Глава I. Общие вопросы химико-токсикологического анализа
- •§ 1. Объекты химико-токсикологического анализа. Вещественные доказательсва
- •§ 2. Особенности химико-токсикологического анализа
- •§ 3. Осмотр объектов исследования и определение некоторых их свойств
- •§ 4. Предварительные пробы в химико-токсикологическом анализе
- •§ 5. План химико-токсикологического анализа
- •§ 6. Организация органов судебно-медицинской и судебно-химической экспертизы в ссср
- •§ 7. Эксперт-химик
- •§ 8. Правила судебно-химической экспертизы вещественных доказательств
- •§ 9. Акт судебно-химической экспертизы вещественных доказательств
- •§ 10. Некоторые вопросы терминологии в токсикологической химии
- •§ 11. Классификация ядовитых и сильнодействующих веществ в токсикологической химии
- •Глава II. Отравления и некоторые вопросы токсикокинетики ядов
- •§ 1. Отравления и их классификация
- •§ 2. Пути поступления ядов в организм
- •§ 3. Всасывание ядов в организме
- •§ 4. Распределение ядов в организме
- •§ 5. Связывание ядов в организме
- •§ 6. Выделение ядов из организма
- •§ 7. Факторы, влияющие на токсичность химических соединений
- •§ 8. Методы детоксикации
- •§ 9. Метаболизм чужеродных соединений
- •§ 10. Окисление чужеродных соединений
- •§ 11. Восстановление чужеродных соединений
- •§ 12. Гидролиз чужеродных соединений
- •§ 13. Дезалкилирование, дезаминирование и десульфирование чужеродных соединений
- •§ 14. Другие метаболические превращения
- •§ 15. Реакции конъюгации
- •§ 16. Посмертные изменения лекарственных веществ и ядов в трупах
- •§ 17. Разложение биологического материала после наступления смерти
- •§ 18. Изменение ядов при разложении трупов
- •Глава III. Методы анализа, применяемые в токсикологической химии
- •§ 1. Метод экстракции
- •§ 2. Микрокристаллоскопический анализ
- •§ 3. Метод микродиффузии
- •Глава IV. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала перегонкой с водяным паром
- •§ 1. Аппараты для перегонки с водяным паром
- •§2. Влияние рН среды на перегонку химических соединений с водяным паром
- •§ 3. Перегонка ядовитых веществ с водяным паром из подкисленного биологического материала
- •§ 4. Перегонка ядовитых веществ с водяным паром из подкисленного, а затем из подщелоченного биологического материала
- •§ 5. Фракционная перегонка веществ, содержащихся в дистиллятах
- •§ 6. Синильная кислота
- •§ 7. Формальдегид
- •§ 8. Метиловый спирт
- •§ 9. Этиловый спирт
- •§ 10. Изоамиловый спирт
- •§ 11. Ацетон
- •§ 12. Фенол
- •§ 13. Крезолы
- •§ 14. Хлороформ
- •§ 15. Хлоралгидрат
- •§ 16. Четыреххлористый углерод
- •§ 17. Дихлорэтан
- •§ 18. Реакции, позволяющие отличить хлорпроизводные друг от друга
- •§ 19. Тетраэтилсвинец
- •§ 20. Уксусная кислота
- •§ 21. Этиленгликоль
- •Глава V. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала подкисленным этиловым спиртом или подкисленной водой
- •§ 1. Развитие методов выделения алкалоидов и других азотистых оснований из биологического материала
- •§ 2. Влияние рН среды на изолирование алкалоидов и других азотистых оснований из биологического материала
- •§ 3. Влияние состава извлекающих жидкостей на изолирование алкалоидов и других азотистых основании из биологического материала
- •§ 4. Влияние подкисленной воды и подкисленного спирта на извлечение примесей, переходящих в вытяжки из биологического материала
- •§ 5. Очистка вытяжек из биологического материала от примесей
- •§ 6. Экстракция алкалоидов и других токсических веществ из вытяжек
- •§ 7. Обнаружение ядовитых веществ, изолируемых подкисленной водой или подкисленным этиловым спиртом
- •§ 8. Количественное определение токсических веществ, изолированных подкисленной водой или подкисленным спиртом
- •§ 9. Метод выделения токсических веществ, основанный на изолировании их этиловым спиртом подкисленным щавелевой кислотой
- •§ 10. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной щавелевой кислотой
- •§ 11. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной серной кислотой
- •§ 12. Барбитураты и методы их исследования
- •§ 13. Барбамил
- •§ 14. Барбитал
- •§ 15. Фенобарбитал
- •§ 16. Бутобарбитал
- •§ 17. Этаминал-натрий
- •8. Обнаружение этаминала-натрия по уф- и ик-спектрам.
- •§ 18. Бензонал
- •§ 19. Гексенал
- •§ 20. Производные ксантина
- •§ 21. Кофеин
- •§ 22. Теобромин
- •§ 23. Теофиллин
- •§ 24. Наркотин
- •§ 25. Меконовая кислота
- •§ 26. Меконин
- •§ 27. Ноксирон
- •§ 28. Салициловая кислота
- •§ 29. Антипирин
- •§ 30. Амидопирин
- •§ 31. Фенацетин
- •§ 32. Хинин
- •§ 33. Опий и омнопон
- •§ 34. Морфин
- •§ 35. Кодеин
- •§ 36. Папаверин
- •§ 37. Галантамин
- •§ 38. Анабазин
- •§ 39. Никотин
- •§ 40. Ареколин
- •§ 41. Кониин
- •§ 42. Атропин
- •§ 43. Скополамин
- •§ 44. Кокаин
- •§ 45. Стрихнин
- •§ 46. Бруцин
- •§ 47. Резерпин
- •§ 48. Пахикарпин
- •§ 49. Секуренин
- •§ 50. Эфедрин
- •§ 51. Аконитин
- •§ 52. Новокаин
- •§ 53. Дикаин
- •§ 54. Аминазин
- •§ 55. Дипразин
- •§ 56. Тизерцин
- •§ 57. Хлордиазепоксид
- •§ 58. Диазепам
- •§ 59. Нитразепам
- •§ 60. Оксазепам
- •§ 61. Апоморфин
- •§ 62. Дионин
- •§ 63. Промедол
- •Глава VI. Вещества, изолируемые из объектов минерализацией биологического материала
- •§ 1. Связывание «металлических ядов» биологическим материалом
- •§ 2. Методы минерализации органических веществ
- •§ 3. Сухое озоление и сплавление органических веществ
- •§ 4. Окислители, применяемые для минерализации органических веществ
- •§ 5. Отбор и подготовка проб биологического материала для минерализации
- •§ 6. Разрушение биологического материала азотной и серной кислотами
- •§ 7. Разрушение биологического материала хлорной, азотной и серной кислотами
- •§ 8. Разрушение биологического материала пергидролем и серной кислотой
- •§ 9. Дробный метод и систематический ход анализа «металлических ядов»
- •§ 10. Маскировка ионов в дробном анализе
- •§ 11. Реактивы, применяемые в дробном анализе «металлических ядов» для маскировки ионов
- •§ 12. Реакции, применяемые в химико-токсикологическом анализе для обнаружения ионов металлов
- •§ 13. Соединения бария
- •§ 14. Соединения свинца
- •§ 15. Соединения висмута
- •§ 16. Соединения кадмия
- •§ 17. Соединения марганца
- •§ 18. Соединения меди
- •§ 19. Соединения мышьяка
- •§ 20. Соединения серебра
- •§ 21. Соединения сурьмы
- •§ 22. Соединения таллия
- •§ 23. Соединения хрома
- •§ 24, Соединения цинка
- •§ 25. Соединения ртути
- •§ 26. Количественное определение «металлических ядов» в минерализатах
- •§ 27. Количественное определение ртути
- •§ 28. Экстракционно-фотоколориметрическое определение меди
- •Глава VII. Вещества, изолируемые из биологического материала настаиванием исследуемых объектов с водой
- •Минеральные кислоты и щелочи
- •§ 1. Серная кислота
- •§ 2. Азотная кислота
- •§ 3. Соляная кислота
- •§ 4. Гидроксид калия
- •§ 5. Гидроксид натрия
- •§ 6. Аммиак
- •§ 7. Нитриты
- •Глава VIII. Ядохимикаты и методы их химико-токсикологического анализа
- •§ 1. Классификация ядохимикатов
- •§ 2. Гексахлорциклогексан (гхцг)
- •§ 3. Гептахлор
- •§ 4. Фосфорсодержащие органические соединения и методы их анализа
- •§ 5. Хлорофос
- •§ 6. Карбофос
- •§ 7. Метафос
- •§ 8. Карбарил
- •§ 9. Гранозан
- •Глава IX. Вещества, определяемые непосредственно в биологическом материале
- •§ 1. Оксид углерода (II)
- •§ 2. Спектроскопический метод обнаружения оксида углерода (II) в крови
- •§ 3. Химические методы обнаружения оксида углерода (II) в крови
- •§ 4. Количественное определение оксида углерода (II) в крови
- •Приложение 1. Приготовление реактивов
- •Приложение 2. Приготовление хроматографических пластинок
- •Список рекомендуемой литературы
§ 10. Маскировка ионов в дробном анализе
Все объявления
ЯндексДирект
Дать объявление
Растворители в различной фасовке
Растворители 646,ацетон, у-спирит, скипидар,лак НЦ и БТ, краски МА и ПФ,в/э
www.chemservice.ru
Маскировка ионов является одной из важнейших операций в дробном анализе. Маскировкой называется процесс устранения влияния мешающих ионов, находящихся в сложной смеси, на обнаружение искомых ионов. При маскировке мешающие ионы переводят в соединения или в другие ионы, которые теряют способность реагировать с реактивами на искомые ионы. Существует несколько способов маскировки ионов. С целью маскировки мешающие ионы переводят в устойчивые комплексы, изменяют валентность этих ионов при помощи окислителей или восстановителей, изменяют рН среды и т. д.
Основным способом маскировки мешающих ионов, который применяется в аналитической химии и в химико-токсикологическом анализе, является комплексообразование. Пользуясь этим способом, для маскировки подбирают такой реактив, который с мешающими ионами образует бесцветные прочные комплексные ионы, не способные реагировать с реактивами на искомые ионы. Использование комплексообразования для маскировки ионов можно показать на нескольких примерах.
1. Для обнаружения ионов Со 2+ применяют роданид аммония. При этом образуется соединение (NH 4 ) 2 [Co(SCN) 4 ], имеющее синюю окраску. Обнаружению ионов Со 2+ роданидом аммония мешают ионы железа (III), которые с этим реактивом дают кроваво-красную окраску. Для устранения мешающего влияния ионов железа (III) к смеси, содержащей ионы кобальта и железа, прибавляют растворы фторидов или фосфатов, которые переводят ионы железа (III) в бесцветный комплекс [FeF 6 ] 3-, не реагирующий с роданидом аммония. Таким образом, после маскировки ионов железа (III) фторидами или фосфатами можно легко обнаружить ионы кобальта, находящиеся в смеси с ионами железа, используя роданид аммония.
2. Обнаружению ионов кадмия реакцией с сероводородом (образуется желтый осадок CdS) мешают ионы меди, которые с этим реактивом дают черный осадок CuS. Для маскировки ионов меди прибавляют растворы цианидов, образующие с указанными ионами бесцветный комплекс [Cu(CN) 4 ] 3-, не реагирующий с сероводородом.
Демаскировка ионов. Демаскировкой называют процесс освобождения ранее замаскированных ионов от маскирующих реактивов. В результате демаскировки ранее замаскированные ионы восстанавливают способность вступать в реакции с соответствующими реактивами. Демаскировка в основном осуществляется разложением комплексных ионов, которые ранее образовались в процессе маскировки.
Процесс демаскировки можно показать на примере разложения следующих комплексных ионов:

§ 11. Реактивы, применяемые в дробном анализе «металлических ядов» для маскировки ионов
Все объявления
ЯндексДирект
Дать объявление
Низкотемпературные камеры
низкотемпературные морозильники с температурным режимом -24С, -55С, -85С
Адрес и телефон · www.winecoolers.ru
В дробном анализе «металлических ядов» для маскировки мешающих ионов применяются цианиды, фториды, фосфаты, тиосульфаты, тиомочевина и другие вещества.
1. Цианиды. Применение цианидов для маскировки ионов основано на том, что с их помощью мешающие ионы можно перевести в комплексы:
[Co(CN) 6 ] 4-, [Fe(CN) 6 ] 4-, [Fe(CN) 6 ] 3-, [Ni(CN) 4 ] 2-, [Zn(CN) 4 ] 2-, Cd(CN) 4 ] 2-, [Hg(CN) 4 ] 2-, [Ag(CN) 2 ] -.
Образование цианидных комплексов меди происходит в 2 этапа. Вначале восстанавливаются ионы меди (II), а затем образуется комплексный ион:

Широкое применение цианидов для маскировки ионов объясняется тем, что при необходимости из комплексных цианидов можно легко демаскировать катионы соответствующих металлов.
Следует отметить, что применение цианидов для маскировки ионов имеет и некоторое ограничение. Цианиды довольно токсичны. Их нельзя прибавлять к кислым растворам, так как в присутствии кислот происходит разложение цианидов и выделяется летучая очень ядовитая синильная кислота. Поэтому работа с цианидами должна производиться под вытяжным шкафом с хорошей тягой.
2. Фториды. Фториды часто используются для маскировки ионов железа (III), с которыми они образуют бесцветные устойчивые комплексные ионы [FeF 6 ] 3-.
3. Фосфаты. В дробном анализе фосфаты также применяются для маскировки ионов железа (III). В кислой среде фосфаты и фосфорная кислота с ионами железа образуют бесцветные комплексы [Fe(PO 4 ) 2 ] 3-.
4. Тиосульфаты. Тиосульфаты применяются для маскировки ионов серебра, свинца, железа (III), меди и других катионов. При взаимодействии тиосульфатов с перечисленными ионами образуются комплексы: [Ag 2 (S 2 O 3 ) 3 ] 4-, [Pb(S 2 O 3 ) 3 ] 4-, [Fe(S 2 O 3 ) 2 ]-.
Реакция ионов меди с тиосульфатом происходит в 2 этапа. Вначале тиосульфаты восстанавливают ионы меди (II), а затем образуются комплексы:

5. Гидроксиламин. Маскирующее действие гидроксиламина основано на том, что с одними ионами он образует комплексы, а с другими — вступает в реакции окисления-восстановления. С ионами кобальта гидроксиламин образует комплекс [Co(NH 2 OH) 6 ] 2+. В зависимости от природы ионов, с которыми реагирует гидроксиламин, он может быть окислителем и восстановителем. Гидроксиламин восстанавливает ионы железа (III) и окисляет ионы AsO 2 - и SbO 2 - :
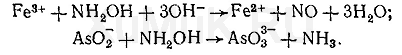
Для связывания избытка гидроксиламина применяют формальдегид, с которым он образует формальдоксим:
![]()
6. Тиомочевина. В дробном анализе тиомочевина используется для маскировки ионов висмута, железа (III), сурьмы (III). кадмия, ртути, серебра и других катионов. С указанными ионами тиомочевина образует прочные внутрикомплексные соединения.
7. Глицерин. С катионами висмута, свинца, кадмия и другими глицерин образует глицераты:

С некоторыми ионами глицерин дает окрашенные соединения. Образование этих соединений используется в анализе для идентификации ионов.
8. Комплексен III (трилон Б) широко применяется в количественном анализе. Однако этот реактив довольно часто используется и для маскировки ионов кадмия, кобальта, меди, железа, марганца, свинца, цинка, магния и др. При взаимодействии комплексона III с указанными ионами образуются прочные внутрикомплексные соединения.
Комплексон III с ионами металлов независимо от их валентности реагирует в соотношении 1 : 1. При взаимодействии ком-плексона III с ионами металлов образуются внутрикомплексные соединения за счет замещения атомов водорода в карбоксильных группах комплексона и за счет образования координационных связей между ионами металлов и атомами азота аминогрупп. Строение внутрикомплексных соединений двух- и трехвалентных металлов с комплексоном III можно представить следующими формулами;
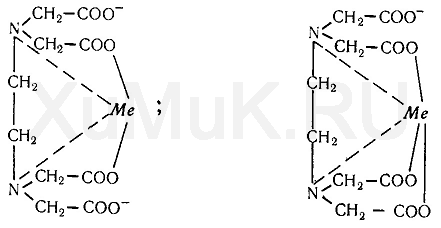
9. Лимонная кислота и ее соли (цитраты) с катионами ряда металлов дают прочные соединения, строение которых можно выразить следующими формулами:

В дробном анализе лимонная кислота используется для маскировки ионов висмута, меди, железа (III), сурьмы (III), кадмия, ртути, серебра и некоторых других.
10. Винная кислота и ее соли (тартраты) с многими металлами образуют прочные растворимые в воде комплексы:

Способность винной кислоты образовывать прочные комплексные соединения с металлами используется для маскировки ионов меди, железа (III), алюминия, висмута, кадмия, ртути, свинца, цинка и др.
11. Аскорбиновая кислота. Применение аскорбиновой кислоты как маскирующего средства в основном базируется на восстановительных свойствах этой кислоты. При взаимодействии аскорбиновой кислоты с сильными окислителями она переходит в щавелевую или треоновую кислоту, а при взаимодействии с окислителями средней силы аскорбиновая кислота превращается в дегидроаскорбиновую кислоту:

Восстанавливающие свойства аскорбиновой кислоты используются в анализе для маскировки ионов железа (III), олова (IV) и др.
