
- •1. Основні положення мкт. Ідеальний газ.
- •Основні визначення (тиск, густина, кількість речовини, константи й розмірність)
- •2) Число молекул у речовини;
- •3) Число молекул у речовини;
- •Кількість речовини можна знайти по формулі
- •2. Основне рівняння мкт, температура, середньоквадратична швидкість
- •Основне рівняння молекулярно-кінетичної теорії записується так:
- •Основне рівняння молекулярно-кінетичної теорії записується так:
- •Основне рівняння молекулярно-кінетичної теорії записується так:
- •Температура знизилася з до . Як змінилася при цьому середньоквадратична швидкість молекул?
- •1) Зменшилася в 2 рази;
- •3. Рівняння Менделеева-Клапейрона, газові закони
- •Рівняння Менделеева-Клапейрона має вигляд
- •Рівняння Менделеева-Клапейрона має вигляд
- •Рівняння ізобари має вигляд
- •4. Складні завдання на газові закони
- •5.Основні визначення статистики Максвелла
- •6. Знання формул для статистики Максвелла, середньоквадратична швидкість
- •7.Розподіл Больцмана (не скрізь знання формули)
- •1) ; 2) ; 3) Обидві формули вірні.
- •8. Довжина вільного пробігу молекули
- •9. Термодинаміка. Визначення. 1-е начало. Прості питання.
- •10.Перше начало термодинаміки для ізопроцесів. Складні формули. Задачі.
- •11.Теплоємність, адіабатний процес
- •12. Теплові машини
- •13. Друге начало термодинаміки. Ентропія
- •3. Обидві формули вірні.
- •3. Обидві формули вірні.
6. Знання формул для статистики Максвелла, середньоквадратична швидкість
Розподіл Максвелла має вигляд
1)
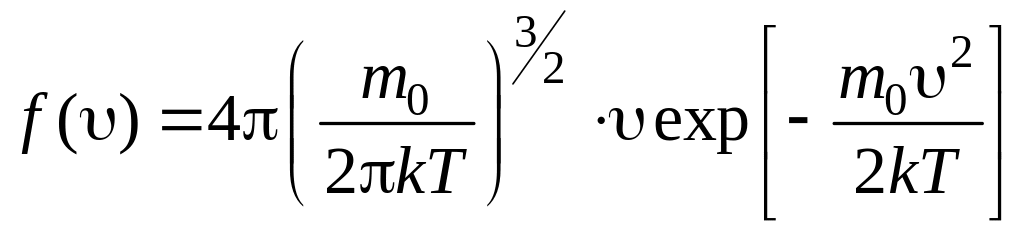
2)

3)
![]() .
.
Розподіл Максвелла має вигляд
1)
![]() ;
;
2)
![]() ;
;
3) .
Розподіл Максвелла має вигляд
1) ;
2) ;
3) .
Середня швидкість молекул визначається формулою
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Найбільш імовірна швидкість молекул визначається формулою
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Середньоквадратична швидкість молекул визначається формулою
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Середня швидкість молекул визначається формулою
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Найбільш імовірна швидкість молекул визначається формулою
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Середньоквадратична швидкість молекул визначається формулою
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Середньоквадратична швидкість молекул залежить від температури як
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Середньоквадратична швидкість молекул деякого газу при температурі 500 К була 500 м/с. Чому стала дорівнює середньоквадратична швидкість молекул цього газу при температурі 900 К?
1) 670 м/с 2) 740 м/с; 3) 800 м/с.
Середня швидкість молекул деякого газу при температурі 300 К була 1000 м/с. Чому стала дорівнює середня швидкість молекул цього газу при температурі 800 К?
1) 1,6 км/з 2) 2 км/з; 3) 2,4 км/с.
Найбільш імовірна швидкість молекул деякого газу при температурі 400 К була 400 м/с. Чому стала дорівнює найбільш імовірна швидкість молекул цього газу при температурі 1200 К?
1) 571 м/с 2) 692 м/с; 3) 813 м/с.
Середньоквадратична швидкість молекул кисню (молярна маса ) при температурі 23 0С дорівнює
1) 267 м/с 2) 320 м/с; 3) 483 м/с.
Середньоквадратична швидкість молекул кисню (молярна маса ) при температурі 500 0С дорівнює
1) 644 м/с 2) 776 м/с; 3) 915 м/с.
Середня швидкість молекул водню при температурі 23 0С дорівнює
1) 1,21 км/з 2) 1,782 км/з; 3) 2,156 км/с.
Середня швидкість молекул водню при температурі 500 0С дорівнює
1) 2,86 км/з 2) 3,07 км/з; 3) 5,72 км/с.
При якій температурі середньоквадратична швидкість молекул водню дорівнює 500 м/с
1) 80 К 2) 140 К 3) 210 К.
Чому дорівнює середньоквадратична швидкість молекул водню при температурі 100 К?
1) 513 м/с 2) 883 м/с; 3) 1116 м/с.
Між величинами середньої швидкості
 ,
середньоквадратичної швидкості
,
середньоквадратичної швидкості
 й найбільш імовірної швидкості
й найбільш імовірної швидкості
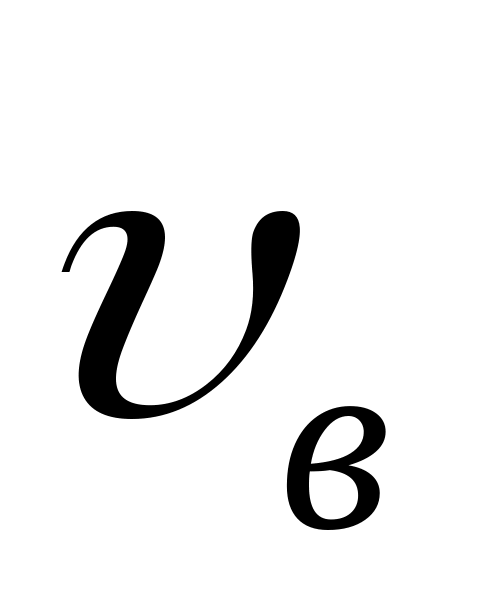 справедливе співвідношення
справедливе співвідношення
1);![]() 2);
2);
![]() 3)
3)
![]() .
.
7.Розподіл Больцмана (не скрізь знання формули)
Розподіл Больцмана - це розподіл часток по
1) потенціальній енергії;
2) висоті;
3) обоє твердження вірні.
Розподіл Больцмана справедливий
1) для молекул ідеального газу;
2) для мікроскопічних часток у полі тяжіння ;
3) обоє твердження вірні.
Розподіл Больцмана - це розподіл часток по
1) потенціальній енергії;
2) кінетичної енергії;
3) енергії хаотичного руху.
Розподіл Больцмана має вигляд
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Розподіл Больцмана має вигляд
1)
; 2)
![]() ; 3)
; 3)
![]() .
.
Барометрична формула має вигляд
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Барометрична формула має вигляд
