
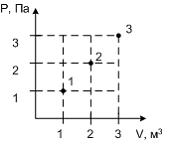
Идеальный газ
имеет минимальную внутреннюю энергию
в состоянии …
 Решение:
Решение:
Внутренняя энергия
идеального газа равна
![]() (учитываем,
что
(учитываем,
что
![]() ),
где
),
где
![]() давление,
давление,
![]() объем,
объем,
![]() полное
число степеней свободы,
полное
число степеней свободы,
![]() универсальная
газовая постоянная,
универсальная
газовая постоянная,
![]() абсолютная
температура,
абсолютная
температура,
![]() масса
газа,
масса
газа,
![]() молярная
масса газа. В нашем случае минимальное
значение произведения
молярная
масса газа. В нашем случае минимальное
значение произведения
![]() соответствует
состоянию газа, обозначенному на
соответствует
состоянию газа, обозначенному на ![]() -
диаграмме точкой 1. Следовательно,
идеальный газ имеет минимальную
внутреннюю энергию в состоянии 1.
-
диаграмме точкой 1. Следовательно,
идеальный газ имеет минимальную
внутреннюю энергию в состоянии 1.
Изменение внутренней
энергии газа при изохорном процессе
возможно …![]()
![]()
 в
результате совершения газом работы
в
результате совершения газом работы
Ответ неверный!
![]()
Так как при изохорном
процессе объем
![]() то
работа газа
то
работа газа
![]() .
.
Закрыть данную подсказку.
в результате совершения внешними силами работы над газом
Ответ неверный!
Так как при изохорном
процессе объем
то
работа внешних сил
![]() .
.
Закрыть данную подсказку.
при теплообмене с внешней средой без теплообмена с внешней средой
Решение:
Согласно
первому
началу термодинамики изменение внутренней
энергии системы определяется формулой
![]() ,
где
,
где
![]() количество
теплоты, переданное системе внешней
средой и
не связанное с изменением объема;
количество
теплоты, переданное системе внешней
средой и
не связанное с изменением объема;
![]() работа,
совершенная внешними телами над системой
и связанная с изменением объема.
Так
как при изохорном процессе объем
то
работа
.
Тогда первое начало термодинамики
приобретает вид:
работа,
совершенная внешними телами над системой
и связанная с изменением объема.
Так
как при изохорном процессе объем
то
работа
.
Тогда первое начало термодинамики
приобретает вид:
![]() ,
т.е. изменение внутренней энергии
возможно лишь при передаче газу
теплоты извне (либо при передаче газом
теплоты внешним телам).
,
т.е. изменение внутренней энергии
возможно лишь при передаче газу
теплоты извне (либо при передаче газом
теплоты внешним телам).
Уравнение
кинетической теории для давления
идеального газа имеет вид ![]() ,
где
,
где
![]() концентрация
молекул. Для газа водорода
концентрация
молекул. Для газа водорода ![]() равно
…
равно
…
Решение:
Давление газа
обусловлено ударами молекул о стенку
сосуда и определяется средним значением
кинетической энергии поступательного
движения молекул, а значит, поступательными
степенями свободы ![]() .
Следовательно,
.
Следовательно,
![]() и
не зависит от вида газа.
и
не зависит от вида газа.
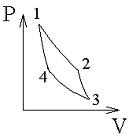
Тепловой двигатель,
работающий по циклу Карно (см. рисунок),
совершает за цикл работу, равную…
Решение:
Цикл Карно состоит
из изотермического расширения газа
1-2, адиабатического расширения 2-3,
изотермического сжатия 3-4 и адиабатического
сжатия 4-1. Работа газа за цикл:
![]() ,
причем при расширении газ совершает
положительную работу, а при сжатии –
отрицательную. В адиабатическом процессе
работа совершается только за счет
изменения внутренней энергии газа.
Поскольку температуры газа
,
причем при расширении газ совершает
положительную работу, а при сжатии –
отрицательную. В адиабатическом процессе
работа совершается только за счет
изменения внутренней энергии газа.
Поскольку температуры газа
![]() и
и
![]() ,
изменение внутренней энергии
,
изменение внутренней энергии
![]() (в
процессе 2-3 газ охлаждается, а в 4-1 –
нагревается
на одну и ту же температуру).
Следовательно,
(в
процессе 2-3 газ охлаждается, а в 4-1 –
нагревается
на одну и ту же температуру).
Следовательно,
![]() ,
а работа за цикл
,
а работа за цикл
![]() ,
причем
,
причем
![]() .
.
На
рисунке представлен график функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
![]() –
доля молекул, скорости которых заключены
в интервале скоростей от
–
доля молекул, скорости которых заключены
в интервале скоростей от
![]() до
до
![]() в
расчете на единицу этого интервала.
в
расчете на единицу этого интервала.
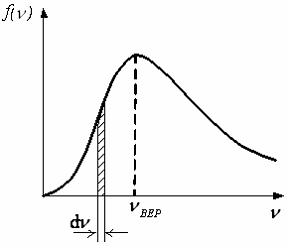 Для
этой функции является верным утверждение,
что …
Для
этой функции является верным утверждение,
что …
при изменении температуры площадь под кривой не изменяется с увеличением температуры величина максимума функции увеличивается
Ответ неверный!
С увеличением температуры положение максимума смещается вправо в сторону больших скоростей, площадь под кривой не изменяется, следовательно, величина максимума убывает.
Закрыть данную подсказку.
с уменьшением температуры величина максимума функции уменьшается
Ответ неверный!
С уменьшением температуры положение максимума смещается влево в сторону меньших скоростей, площадь под кривой не изменяется, следовательно, величина максимума возрастает.
Закрыть данную подсказку.
при изменении температуры положение максимума не изменяется
Решение:
Полная
вероятность равна: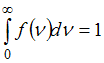 ,
т.е. площадь, ограниченная кривой
распределения Максвелла, равна единице
и при изменении температуры не
изменяется. Из формулы наиболее вероятной
скорости
,
т.е. площадь, ограниченная кривой
распределения Максвелла, равна единице
и при изменении температуры не
изменяется. Из формулы наиболее вероятной
скорости
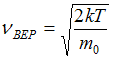 ,
при которой функция
,
при которой функция
![]() максимальна,
следует, что при повышении температуры
максимум функции сместится вправо.
максимальна,
следует, что при повышении температуры
максимум функции сместится вправо.
Средняя
кинетическая энергия молекул газа при
температуре
![]() зависит
от их конфигурации и структуры, что
связано с возможностью различных видов
движения атомов в молекуле и самой
молекулы. При условии, что имеет место
только поступательное и вращательное
движение молекулы как целого, средняя
кинетическая энергия молекул азота
зависит
от их конфигурации и структуры, что
связано с возможностью различных видов
движения атомов в молекуле и самой
молекулы. При условии, что имеет место
только поступательное и вращательное
движение молекулы как целого, средняя
кинетическая энергия молекул азота
![]() равна
…
равна
…
Решение:
Для
статистической системы в состоянии
термодинамического равновесия на каждую
поступательную и вращательную степени
свободы приходится в среднем кинетическая
энергия, равная
![]() ,
а на каждую колебательную степень –
,
а на каждую колебательную степень –
![]() .
Средняя кинетическая энергия молекулы
равна
.
Средняя кинетическая энергия молекулы
равна
![]() ,
где
,
где
![]() –
сумма числа поступательных, числа
вращательных и удвоенного числа
колебательных степеней свободы молекулы.
При условии, что имеют место только
поступательное и вращательное движение,
сумма числа степеней свободы равна
–
сумма числа поступательных, числа
вращательных и удвоенного числа
колебательных степеней свободы молекулы.
При условии, что имеют место только
поступательное и вращательное движение,
сумма числа степеней свободы равна
![]() ;
где
;
где
![]() –
число степеней свободы поступательного
движения, равное
–
число степеней свободы поступательного
движения, равное
![]() ;
;
![]() –
число степеней свободы вращательного
движения, которое может быть равно
–
число степеней свободы вращательного
движения, которое может быть равно
![]() .
Для
молекулярного азота (двухатомной
молекулы)
и
.
Для
молекулярного азота (двухатомной
молекулы)
и
![]() .
Следовательно,
.
Следовательно,
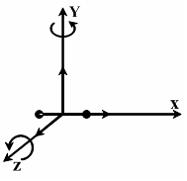
![]() (3
степени свободы поступательного движения
по направлениям осей ординат
(3
степени свободы поступательного движения
по направлениям осей ординат![]() и 2 степени свободы вращательного
движения вокруг осей
и 2 степени свободы вращательного
движения вокруг осей
![]() и
и
![]() )
(см. рис.). Тогда средняя энергия молекул
азота
равна
)
(см. рис.). Тогда средняя энергия молекул
азота
равна
![]() .
.
Если количество теплоты, отдаваемое рабочим телом холодильнику, увеличится в два раза, то коэффициент полезного действия тепловой машины …
уменьшится
на
![]()
