
- •Вступ Лабораторія теплотехніки
- •Зміст лабораторного практикуму
- •Порядок виконання лабораторних робіт
- •Принципи складання лабораторних установок і найбільш поширене лабораторне обладнання, яке використовується в установках
- •Оформлення лабораторних робіт і складання звітів по роботі
- •Визначення теплоємності повітря
- •Мета і задача роботи
- •Теоретичні викладки до роботи
- •Лабораторна установка
- •Порядок виконання роботи
- •Обробка експериментальних даних
- •Форма подання звіту
- •Контрольні питання для самоперевірки
- •Побудова процесів водяної пари в і-s діаграмі
- •Мета і задача роботи
- •Теоретичні викладки до виконання роботи
- •Побудова процесів водяної пари в і-s діаграмі
- •Процеси водяної пари в і-s діаграмі
- •Ізобарний процес
- •Ізохорний процес
- •Ізотермічний процес
- •Зміна внутрішньої енергії, кДж/кг
- •Робота ізотермічного процесу
- •Адіабатний процес
- •Робота процесу
- •Процес дроселювання
- •3. Порядок виконання роботи
- •Побудова термодинамічних процесів
- •Обробка результатів побудування процесів
- •Форма звіту по роботі
- •7. Контрольні питання для самоперевірки
- •Побудова процесів вологого повітря
- •Мета і задачі роботи
- •Теоретичні викладки до виконання роботи
- •Побудова процесів вологого повітря в і-d діаграмі
- •Характерні лінії процесів
- •Процеси вологого повітря в і-d діаграмі
- •Нагрівання повітря
- •2.3.2. Охолодження повітря
- •Адіабатне зволоження повітря
- •Ізотермічне зволоження повітря
- •Змішування потоків повітря
- •Визначення температури точки роси і мокрого термометру
- •Визначення парціального тиску
- •Порядок виконання роботи
- •Побудування термодинамічних процесів
- •Обробка результатів побудування термодинамічних процесів
- •Форма звіту по роботі
- •Контрольні питання для самоперевірки
- •Дослідження термодинамічних процесів вологого повітря
- •Мета і задачі роботи
- •2. Теоретичні викладки до виконання роботи
- •2.1. Параметри вологого повітря
- •2.2. Термодинамічні процеси вологого повітря
- •3. Схема лабораторної установки
- •4. Порядок проведення роботи
- •Дослідження процесів нагрівання і зволоження
- •Дослідження процесів змішування і охолодження
- •5. Обробка результатів проведених
- •5.2. Проводимо побудування процесів нагрівання і адіабатного зволоження в I-d діаграмі
- •6. Склад звіту
- •7. Контрольні питання для самоперевірки
- •Визначення ефективностi роботи холодильної установки
- •Мета і задача роботи
- •Теоретичні викладки до роботи
- •2.1. Зворотній тепловий цикл
- •2.2. Холодопродуктивність
- •Лабораторна установка - холодильний шкаф шх-0,4 м.
- •Робота і процеси холодильного агрегату:
- •Порядок проведення лабораторної роботи
- •5. Обробка результатів вимірювання
- •6. Склад звіту
- •7. Контрольні питання для самоперевірки
- •Дослідження процесу тепловіддачі при вимушеному руху повітря в круглій трубі
- •Мета і задача роботи
- •2. Теоретичні викладки до роботи
- •3. Схема лабораторної установки
- •4. Порядок проведення дослідів
- •5. Обробка результатів вимірювання
- •6. Склад звіту
- •Контрольні питання для
- •Визначення коефiцiєнта теплопередачi через багатошарову цилiндричну стiнку
- •Мета і задача роботи
- •2. Теоретичнi викладки до роботи
- •2.1. Коефiцiєнт теплопровiдностi
- •2.2. Коефіцієнт тепловіддачі
- •2.3. Коефiцiєнт теплопередачi
- •Для одношарової стiнки
- •3. Схема лабораторної установки
- •4. Порядок проведення лабораторної роботи
- •5. Обробка результатiв вимiрювання
- •6. Склад звiту
- •7. Контрольнi питання для самоперевiрки
- •Визначення показникiв якостi води
- •Мета і задача роботи
- •2. Теоретичнi викладки до роботи
- •2.1. Домiшки природних вод
- •2.2. Показники якостi води
- •2.3. Способи очистки води
- •3. Схема лабораторної установки
- •4. Порядок проведення роботи
- •4.1. Визначення жорсткостi води за допомогою трилону б
- •4.2. Визначення лужностi води по фенолфталеїну
- •4.3. Визначення вмiсту нафтопродуктiв у водi
- •4.4. Визначення вмiсту нiтратiв у водi
- •5. Склад звiту
- •6. Контрольнi питання для самоперевiрки
- •Визначення вологості і зольності твердого палива
- •Мета і задача роботи
- •2. Теоретичнi викладки до роботи
- •2.1. Склад твердих, рiдинних I газових палив
- •2.2. Вологiсть палива
- •2.3. Зольнiсть палива
- •3. Схеми лабораторних установок
- •3.1. Лабораторна установка для визначення вологостi твердого палива
- •3.2. Лабораторна установка для визначення зольностi палива
- •4. Методика проведення дослiдiв
- •4.1. Визначення вологостi твердого палива
- •4.2. Визначення зольностi палива
- •5. Обробка результатiв дослiдження
- •5.1. Розрахунок вологостi палива
- •5.2. Розрахунок зольностi палива
- •6. Склад звiту
- •Дослідження процесів тепловіддачі при природній конвекції від горизонтальних труб
- •1. Мета I задача роботи
- •2. Теоретичнi викладки до роботи
- •3. Схема лабораторної установки
- •4. Порядок проведення дослiдiв
- •5. Обробка результатiв вимiрювання
- •6. Склад звiту
- •7. Контрольнi питання для самоперевiрки
- •Ардашев Віктор Олексійович
- •П’ятак Ольга Володимирівна
- •Теплотехніка
- •Лабораторні роботи
Форма подання звіту
Звіт по лабораторній роботі подається на подвійному аркуші учнівського зошиту. На першій сторінці оформлюється титульний лист. На інших сторінках розміщається:
Мета та задача роботи
Схема установки та короткий опис її роботи
Таблиця 1.1 – вимірювання дослідних даних
Таблиця 1.2 – розрахункових значень теплоємності
Таблиця 1.3 – розрахункових значень параметрів ізобарного процесу та похибки досліду
Висновки по роботі
Звіт складається та пред’являється студентом до захисту індивідуально.
Контрольні питання для самоперевірки
7.1. Ціль та задачі роботи.
7.2. Дати визначення масової, мольної та об’ємної теплоємності.
7.3. Взаємозв’язок між видами теплоємності.
7.4. Середня та істина теплоємності.
7.5. Ізобарна та ізохорна теплоємності.
7.6. Рівняння Майєра.
7.7. Формула для визначення середньої масової ізобарної теплоємності.
7.8. Схема лабораторної установки та її робота.
7.9. Визначення витрати повітря.
7.10. Порядок проведення роботи.
7.11. Обробка експериментальних даних.
7.12. Розрахунок параметрів ізобарного процесу.
Звужуючий пристрій та проточний калориметр.
8. Л І Т Е Р А Т У Р А
8.1. Кириллин В.А., Сычев В.В., Шейндлин А.Е. Техническая термодинамика. - М.: Наука, 1979. - 512 с.
Нащекин В.В. Техническая термодинамика и теплопередача. - М.: Высшая школа, 1960. - 469 с.
Кириллин В.А., Шейндлин А.Е. Основы экспериментальной термодинамики. - М.: Наука, 1967.
Преображенский В.П. Теплотехнические измерения и приборы. - М.: Энергия, 1976. - 704 с.
Андрианова Т.Н., Дзампов Б.В., Зубарев В.Н., Ремизов С.А. Сборник задач по технической термодинамике. - М.: Энергоиздат, 1981. - 240 с.
Рабинович О.М. Сборник задач по технической термодинамике. - М.: Машиностроение, 1973. - 344 с.
Лабораторна робота № 2
Побудова процесів водяної пари в і-s діаграмі
Мета і задача роботи
Мета роботи – отримання практичних навичок роботи з і-s діаграмою.
Задача роботи – побудова і розрахунок термодинамічних процесів водяної пари в і-s діаграмі.
Теоретичні викладки до виконання роботи
і-s діаграма водяної пари
Сітку і-s діаграми складають: горизонтальні лінії і =const, кДж/кг та вертикальні лінії s = const кДж/(кгК). На сітку наноситься нижня (ліва) погранична крива ОК, яка виходить з початку координат і верхня погранична крива КМ. Обидві криві сходяться у точці К, яка характеризує критичний стан води і називається критичною.
Між пограничними кривими розміщаються лінії проміжних значень ступенів сухості х. Ступінь сухості пари являє собою відношення маси сухої насиченої пари mс.н.п. до маси вологої насиченої пари mв.н.п. = mс.н.п. + mр ; mр – маса рідини (води)
![]() (2.1)
(2.1)
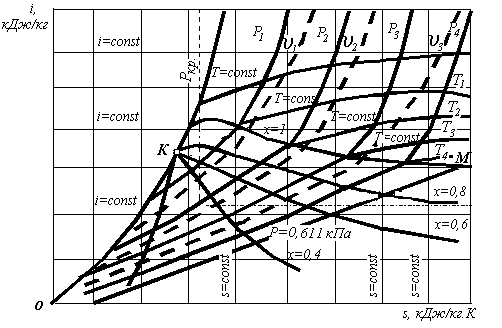
Рис.2.1. і-s діаграма водяної пари
Для води нижня погранична крива ОК, х = 0, для сухої насиченої пари, верхня погранична крива КМ, х = 1. Пара, температура якої дорівнює температурі насичення і в якій відсутня рідина, називається сухою насиченою. Суміш сухої насиченої пари і рідини називається вологою насиченою парою. Зліва від нижньої пограничної кривої ОК вода знаходиться у рідинному стані. Будь-яка точка на пограничній кривій відповідає стану рідини, нагрітої до температури кипіння. Між пограничними кривими ОК і КМ вода знаходиться у стані вологої насиченої пари. Будь-яка точка на верхній (правій) пограничній кривій відповідає стану сухої насиченої пари. Поверх кривої КМ вода знаходиться у стані перегрітої пари.
В області вологої насиченої пари ізобари співпадають з ізотермами. Прямі лінії ізобар Р = const виходять віялом з початку координат, причому Р1 Р2 Р3 Р4 . . . .В області перегрітої пари ізобари та ізотерми розходяться. Ізобари піднімаються до верху у виді логарифмічних кривих, а ізотерми t = const відхиляються до горизонталі, причому t1 t2 t3 t4 . .
На сітку діаграми наносяться ізохори, лінії v = const, це пунктирні лінії, причому v1 v2 v3 . .Вони мають вид кривих, які порівняно з ізобарами піднімаються більш крутіше у верх.
Область діаграми, яка лежить нижче ізобари Р=0,611 кПа, відповідає стану суміші пара – лід.
В практичній роботі використовується не вся і-s діаграма, а тільки частина її. На рисунку ця частина діаграми відокремлена штрихпунктирною лінією.
В і-s діаграмі у вигляді ліній наведені шість параметрів водяної пари: Р, v, t, i, s, x.
