
- •Лабораторная работа № 1 (4 ч.)
- •Теоретическая часть
- •Формулы и названия основных кислот.
- •Экспериментальная часть
- •Порядок выполнения работы
- •2. Получение и свойства гидроксидов
- •3. Получение солей.
- •Контрольные задания:
- •Групповые реакции катионов и анионов.
- •Экспериментальная часть
- •Образец записи в лабораторный журнал
- •Реакция на po ион
- •Реакция на Cl- ион
- •Реакция на ch3coo- ион
- •Реакция на no ион
- •Реакция на j- ион
- •Реакция на c2o ион
- •Качественные реакции на катионы
- •Реакция на ион nh
- •Контрольные вопросы
- •Теоретическая часть
- •Классификация воды по уровню жёсткости
- •Экспериментальная часть
- •Порядок выполнения работы:
- •1. Гидролиз карбонатов
- •2. Действие кислот на карбонаты и гидрокарбонаты.
- •3. Устранение временной (карбонатной ) жесткости.
- •4. Устранение постоянной жесткости.
- •Лабораторная работа №4 (4 ч.) учение о составе – первый уровень в познании свойств веществ
- •Опыт № 1 доктор, который всегда под рукой
- •Опыт № 2 как различить шерсть и хлопок?
- •Опыт № 3 странная жидкость
- •Опыт № 4 гипосульфит натрия – внештатный сотрудник химчистки
- •Опыт № 5 влияние кислотности среды или марганцовка в роли хамелеона
- •Лабораторная работа №5 (4 ч.) структурная химия - второй уровень познания свойств веществ
- •Опыт № 1 как обнаружить фруктозу в меде, ягодах и фруктах?
- •Опыт № 2 до синей окраски, если не нагревать
- •Опыт № 3 денатурация белковых молекул – польза или вред?
- •Часть 1 осаждение белков хлоридом натрия
- •Часть 2 осаждение белков солями тяжелых металлов
- •Лабораторная работа №6 (4 ч.) учение о химических процессах – третий уровень познания свойств веществ
- •Опыт № 1 влияние концентрации веществ на химическое равновесие
- •Часть 1
- •Часть 2
- •Опыт № 2 изучение скорости взаимодействия тиосульфата натрия и серной кислоты
- •Опыт № 3 влияние катализатора на скорость реакции разложения пероксида водорода
- •3. Список используемой литературы
- •5. Приложения
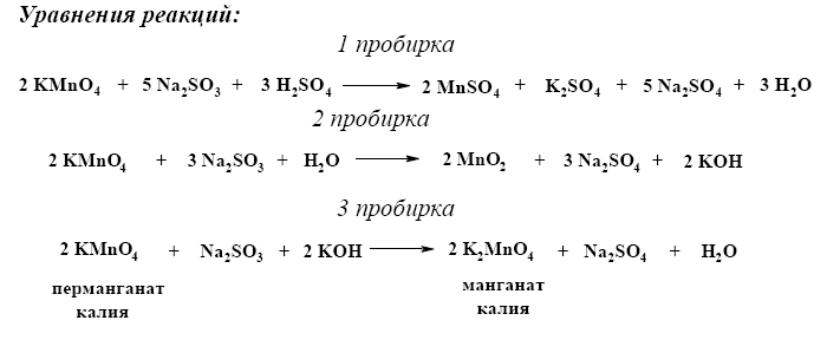
Опыт № 5 влияние кислотности среды или марганцовка в роли хамелеона
Предварительные сведения. Перманганат калия (KMnO4), в быту на-зываемый марганцовкой, один из самых сильных окислителей. В зависи-мости от среды раствора (кислая, нейтральная или щелочная) марганец восстанавливается до разных степеней окисления (Mn+2, Mn+4, Mn+6).
Порядок выполнения:
1. Налейте в три пробирки по 1 мл раствора перманганата калия KMnO4.
2. Добавьте в первую пробирку - разбавленный раствор серной кислоты H2SO4, во вторую - воду, в третью - концентрированный раствор гидроксида натрия NaOH.
3. Добавьте в каждую пробирку несколько кристаллов сухой соли сульфита натрия Nа2SО3.
Наблюдения:
Как изменилась окраска раствора в каждой пробирке?
1. Отметьте цвет растворов в кислой, нейтральной и щелочной средах.
Выводы:
1. Какой тип реакции имеет место в проведенном Вами эксперименте?
2. Как влияет рН среды на состав продуктов восстановления перман-ганат-иона МnО4-?
3. Почему в разных средах происходит изменение окраски перманганат-иона МnО4-?
Лабораторная работа №5 (4 ч.) структурная химия - второй уровень познания свойств веществ
Цель работы: доказать, что в процессе познания и использования свойств веществ необходимо учитывать их структуру.
Опыт № 1 как обнаружить фруктозу в меде, ягодах и фруктах?
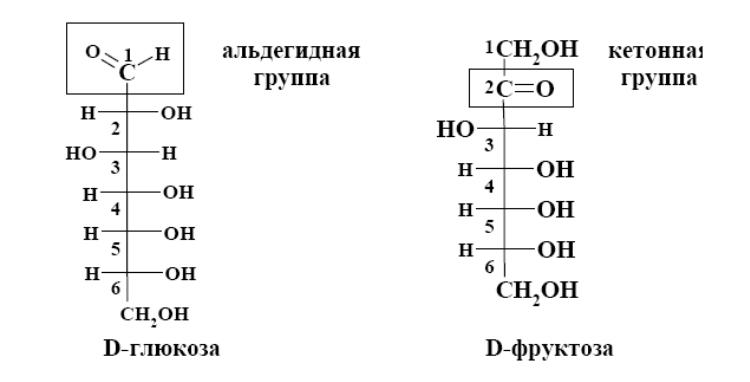
Предварительные сведения. Наиболее важными природными углеводами, относящимися к классу моносахаридов, являются глюкоза и фруктоза, брутто-формула которых одинакова - С6Н12О6, а строение разное, и потому свойства различные.
В структуре глюкозы имеется альдегидная группа (Н-С=О), а в структуре фруктозы - кетонная группа (С=О)
Глюкоза занимает второе место в питании человека после сахарозы (свекловичный или тростниковый сахар). В медицине инъекции глюкозы применяют при явлениях сердечной слабости, шока, потере крови. Она входит в состав заменителей крови и противошоковых препаратов. В свободном виде глюкоза содержится в плодах фруктов, особенно в винограде, поэтому ее часто называют виноградным сахаром.
Фруктоза - пищевой сахар, который хорошо усваивается организмом. Она слаще сахарозы в 1.7 раза. В меде содержится 50% фруктозы, что является причиной повышенной сладости меда перед обычным сахаром (сахарозой). Фруктозу могут употреблять больные диабетом, так как пути превращения фруктозы в человеческом организме не связаны с наличием гормона инсулина. Причиной недостаточно широкого использования фруктозы является ее высокая гигроскопичность и высокая цена.
Порядок выполнения:
Налейте в одну пробирку 1 мл 0.5% раствора глюкозы, в другую 1 мл 0.5% раствора фруктозы.
Добавьте в каждую пробирку 1 мл реактива Селиванова.
Закрепите обе пробирки в пробиркодержателе и нагревайте на водяной бане до изменения окраски в одной из пробирок.
Наблюдения:
Какие видимые изменения произошли в одной из пробирок?
Выводы:
1. Какие простые углеводы можно обнаружить с помощью реактива Се-ливанова?
2. Почему молекулы глюкозы и фруктозы, имея одинаковый состав, проявляют разные химические свойства?
3. Может ли реакция Селиванова быть использована для качественного определения фруктозы?
