
- •Курсовой проект
- •Пояснительная записка
- •1Теоретическая часть.
- •1.1Общие сведения.
- •1.2Свойства и строение электролита.
- •1.3 Температура плавления.
- •1.4 Плотность.
- •1.5 Вязкость.
- •1.6 Поверхностное натяжение.
- •1.7 Удельная электропроводность расплавов.
- •1.8 Термодинамика основных процессов.
- •1.9 Разложение глинозема.
- •1.10 Разложение фторидов.
- •1.11 Основные электродные реакции, протекающие на электродах.
- •1.12 Выход по току.
- •1.13 Состав анодных газов и расход углерода.
- •1.14 Анодный эффект.
- •1.15 Температура.
- •1.16 Плотность тока.
- •1.17 Межполюсное расстояние.
- •1.18 Состав электролита и криолитовое отношение.
- •2 Конструктивный расчет алюминиевого электролизера
- •2.1Расчет анодов
- •2.2. Внутренние размеры шахты
- •2.3. Конструкция подины
- •2.4 Внутренние размеры катодного кожуха
- •2.5 Расчет ошиновки
- •3 Расчет материального баланса
- •3.1. Приход материалов
- •3.2 Расход материалов
- •4 Электрический баланс электролизера
- •4.1. Напряжение поляризации
- •4.2Падение напряжения в обожженном аноде
- •4.2.1. Падение напряжения в угольной части анода
- •4.2.2. Падение напряжения в контакте ниппель-анод
- •4.2.3. Падение напряжения в контактах кронштейн – ниппель и штанга – кронштейн
- •4.2.4 Падение напряжения в ниппеле
- •4.2.5Падение напряжения в кронштейне
- •4.2.6Падение напряжения в алюминиевой штанге
- •4.2.7Падение напряжения в электролите
- •4.2.8Падение напряжения в катодном устройстве
- •4.2.9 Падение напряжения в выступающих из подины участках катодных стержней
- •4.2.10 Падение напряжения в алюминиевых соединительных лентах
- •4.3Падение напряжения в ошиновке
- •4.3.1. Падение напряжения в катодной ошиновке
- •4.3.2. Падение напряжения в анодной ошиновке
- •4.4Падение напряжения за счет анодных эффектов
- •5 Тепловой баланс
- •5.2.4.1. Потери тепла с поверхности анодов
- •5.2.4.2. Потери тепла с открытой поверхности электролита
- •5.2.4.3. Потери тепла с поверхности глиноземной засыпки
- •5.2.4.4Потери тепла с обортовочного листа
- •5.2.4.5. Потери тепла с катодного кожуха
1.3 Температура плавления.
В первом приближении электролит можно представить в виде смеси - - . Однако в пусковой период в электролите алюминиевых электролизеров имеется избыток фторида натрия. Поэтому в общем случае электролит следует представлять не как тройную систему - - , а как взаимную тройную систему
![]() (1)
(1)
Как видно, в электролите образуется
новое химическое соединение
![]() -
алюминат натрия, отличное от остальных
компонентов системы по своим
кристаллооптическим характеристикам.
-
алюминат натрия, отличное от остальных
компонентов системы по своим
кристаллооптическим характеристикам.
Получающаяся система состоит из четырех веществ, но независимых составляющих в ней только три, поэтому система трехкомпонентная. В отличие от обычных тройных систем в ней протекает реакция взаимного обмена, а такие системы называются взаимными .
Существование конгруэнтных химических соединений и позволяет разбить систему (1) на несколько частных:
тройную систему - - ; (2)
тройную взаимную систему
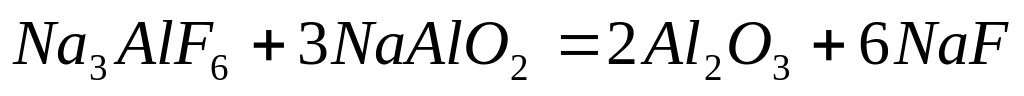 ;
(3)
;
(3)
тройную систему
-
-
![]() ;
;
Температурный интервал последнего соединения очень узкий, при высоком содержании фторида алюминия в расплаве выше 50 % давление насыщенного пара возрастает настолько сильно, что изменения температуры кристаллизации затруднены.
1.4 Плотность.
Важным свойством электролитов является плотность. В системе - (рис.1) с ростом концентрации глинозема плотность монотонно понижается.

Рис.1. Изотермы плотности расплавов системы - .
В системе
-
-
плотность понижается в сторону увеличения
содержания
и
от
.
Плотность необходима для оценки границы
раздела электролит - металл. Для
максимального разделения фаз необходимо,
чтобы плотность металла была во много
раз больше чем электролит. Так при
температуре 960
![]() плотность алюминия
плотность алюминия
![]()
![]() ,
а плотность электролита 2,02 - 2,05
.
Из чего ясно, что алюминий будет осаждаться
на подине ванны, а сверху будет находиться
электролит. В твердом состоянии при
комнатной температуре наоборот, плотность
металла составляет 2,6996 г/см3, а
электролита 2,948 г/см3. Поэтому в
обычных условиях, когда происходит
кристаллизация во всем объеме электролита,
общая плотность смеси жидкой и взвешенной
в ней твердой части электролита
оказывается больше плотности металла,
который сплывает на поверхность ванны.
Это может произойти во время отключения
электроэнергии, когда происходит
охлаждение электролита. И приводит к
прекращению расслаивания металла и
электролита .
,
а плотность электролита 2,02 - 2,05
.
Из чего ясно, что алюминий будет осаждаться
на подине ванны, а сверху будет находиться
электролит. В твердом состоянии при
комнатной температуре наоборот, плотность
металла составляет 2,6996 г/см3, а
электролита 2,948 г/см3. Поэтому в
обычных условиях, когда происходит
кристаллизация во всем объеме электролита,
общая плотность смеси жидкой и взвешенной
в ней твердой части электролита
оказывается больше плотности металла,
который сплывает на поверхность ванны.
Это может произойти во время отключения
электроэнергии, когда происходит
охлаждение электролита. И приводит к
прекращению расслаивания металла и
электролита .
Плотность электролита понижается с
добавками
,
,
и
![]() .
Хлорид натрия оказывает наибольший
эффект. Это понижение плотности может
быть объяснено увеличением объема с
внедрением иона
.
Хлорид натрия оказывает наибольший
эффект. Это понижение плотности может
быть объяснено увеличением объема с
внедрением иона
![]() в
расплав и относительно высокой
температурой по сравнению с температурой
первичной кристаллизации соответствующей
смеси .
в
расплав и относительно высокой
температурой по сравнению с температурой
первичной кристаллизации соответствующей
смеси .
Введение
и
оказывает
меньшее влияние на плотность смеси.
Это, вероятно, обусловлено тем, что при
высоких концентрациях криолита молярный
объем определяется комплексными ионами
![]() .
.
Влияние и на плотность очень мало. Плотность электролита значительно повышается с введением .
1.5 Вязкость.
Вязкость электролита - имеет существенное значение, так как от нее зависит скорость диффузии компонентов электролита, полнота отделения от него металла, удаление анодных газов и другие процессы, сопровождающие электролиз.
Исследования вязкости расплавленных смесей фторидов натрия и алюминия показывают, что увеличение содержания в этих смесях от чистого до криолита значительно повышает вязкость расплава. Максимум вязкости отвечает криолиту, далее происходит резкое снижение.
Вязкость криолитовых расплавов возрастает под влиянием фтористых кальция и магния, но снижается при введении .
Например:
Если вязкость чистого электролита 2,8
![]() (Т=1000
),
то при введении добавки 10 % (по массе)
она возрастает до 3
.
На вязкость электролита влияет
концентрация глинозема, который растворен
в электролите. При 10% (по массе)
в криолите вязкость увеличивается до
3,8
.
Вязкость промышленных электролитов
равна 3,25 - 3,4
(К.О. = 2,7 - 2,5; 5%
Т=1000
).
В системе
-
(рис.2) вязкость повышается с ростом
концентрации глинозема .
(Т=1000
),
то при введении добавки 10 % (по массе)
она возрастает до 3
.
На вязкость электролита влияет
концентрация глинозема, который растворен
в электролите. При 10% (по массе)
в криолите вязкость увеличивается до
3,8
.
Вязкость промышленных электролитов
равна 3,25 - 3,4
(К.О. = 2,7 - 2,5; 5%
Т=1000
).
В системе
-
(рис.2) вязкость повышается с ростом
концентрации глинозема .

Рис.2. Изотермы вязкости расплавов систем - .
