
- •I технология защиты биосферы
- •1 Источники, классификация и методы переработки твердых отходов
- •1.1 Источники и классификация твёрдых отходов
- •1.2 Механическая, механотермическая и термическая переработка твердых отходов (то)
- •2 Переработка отходов неорганических производств
- •2.1 Переработка отходов сернокислотного производства
- •2.2 Переработка отходов производства фосфорных удобрений
- •2.3 Переработка отходов производства калийных удобрений
- •2.4 Переработка отходов производства кальцинированной соды
- •2.5 Переработка отходов горнодобывающей промышленности
- •2.6 Переработка отходов углеобогащения
- •2.7 Переработка и использование сопутствующих пород
- •3 Отходы черной металлургии
- •3.1 Технологические процессы производства шлакового щебня
- •3.2 Шлаки цветной металлургии
- •4 Отходы тепловых электростанций
- •5 Технологии переработки твердых бытовых отходов
- •5.1 Технология сбора, удаления и складирования тбо
- •5.1.1 Масштабы образования и нормы накопления тбо
- •5.1.2 Состав и свойства тбо
- •5.1.3 Технология сбора тбо на местах их образования
- •5.1.4 Технология эвакуации тбо
- •5.1.5 Технология складирования тбо на полигонах
- •5.2 Технология рекультивации территорий закрытых полигонов
- •5.3 Термические методы переработки тбо
- •5.3.1 Классификация методов
- •5.3.2 Термические методы переработки тбо при температурах ниже температуры плавления шлака
- •5.3.2.1 Слоевое сжигание неподготовленных тбо в топках мусоросжигательных котлоагрегатов
- •5.3.2.2 Слоевое сжигание тбо в топке с наклонно переталкивающей решёткой
- •5.3.3 Сжигание в барабанных вращающихся печах
- •5.3.4 Сжигание в печах кипящего слоя
- •5.3.5 Сжигание-газификация в плотном слое кускового материала без его принудительных перемешивания и перемещения
- •5.3.6 Термические методы переработки тбо при температурах выше температуры плавления шлака
- •5.3.6.1 Сжигание в слое шлакового расплава
- •5.3.6.2 Сжигание с использованием электрошлакового расплава
- •5.3.6.3 Пиролиз тбо
- •5.4 Выработка и использование тепловой и других видов энергии на мусоросжигательных заводах
- •5.4.1 Основные предпосылки и факторы сравнения технологических схем утилизации мсз
- •5.4.2 Использование тепла мсз в системах теплоснабжения
- •5.4.2.1 Выбор варианта включения мсз в схему теплоснабжения
- •5.4.3 Использование тепла мсз для выработки электрической энергии
- •5.4.4 Использование тепла мсз для холодильных установок и систем кондиционирования воздуха
- •5.4.5 Использование тепла мсз для сушки осадков сточных вод
- •5.4.5.1 Испарительная сушка осв с использованием в качестве теплоносителя дымовых газов мсз
- •5.4.5.2 Испарительная установка сушки осв с использованием в качестве теплоносителя получаемого на мсз пара
- •5.5 Охрана окружающей среды при эксплуатации мсз
- •5.5.1 Очистка дымовых газов мсз
- •5.5.1.1 Характеристика дымовых газов мсз
- •5.5.1.2 Приемы очистки дымовых газов мсз
- •5.5.2 Утилизация золошлаковых отходов мсз
- •5.6 Аэробное компостирование тбо
- •5.7 Комплексная переработка тбо
- •II технология рекуперации промышленных отходов
- •1 Определения и классификация
- •2 Классификация твердых промышленных и бытовых отходов (тп и бо)
- •3 Технология переработки отходов. Содержащих или образующих органические вещества (диоксины и родственные им соединения)
- •3.1 Полиароматические углеводороды
- •3.2 ”Грязная дюжина”
- •3.3 Процессы, источники образования диоксинов, их токсичность
- •3.4 Полувыведение и полупревращение диоксинов
- •3.5 Показатели токсичности диоксинов
- •4 Технология переработки отходов. Содержащих или образующих неорганические вещества
- •4.1 Неорганические токсины
- •5 Переработка и утилизация отходов пластмасс
- •1 Предварительная очистка и сортировка 2 Измельчение 3 Отмывка и сепарация 4а Классификация по видам 4б Сушка
- •6 Использование при выпуске изделий 5 Конфекционирование и гранулирование
- •5.1 Сепарация пластмассовых отходов из бытового мусора
- •6 Переработка термопластичного вторичного сырья
- •6.1 Измельчение
- •6.2 Уплотнение
- •6.3 Агломерация
- •6.4 Промывка и сушка
- •6.5 Дегазация и фильтрование
- •6.6 Гомогенизация и пластикация
- •6.7 Технология подготовки и использования вторичного сырья из смесей термопластов с другими материалами
- •7 Переработка вторичного сырья эластомеров. Шины и рти
- •7.1 Использование целых шин
- •7.2 Сжигание шин с целью получения энергии
- •7.3 Пиролиз шин
- •7.4 Дробление (измельчение) изношенных шин
2.2 Переработка отходов производства фосфорных удобрений
Основное количество добываемых фосфатных руд служит для производства фосфорсодержащих минеральных удобрений. Наиболее важны апатитовые и фосфоритные руды, содержащие минералы апатитовой группы с общей формулой 3M3(PO4)2 · CaX2 (где М – ионы кальция, натрия, стронция и других элементов, а Х – ионы фтора, хлора и группа ОН-). Кроме апатита, фосфатные руды содержат минералы-примеси.
В зависимости от состава руд применяют различные методы химической переработки природных фосфатов. В большинстве случаев руду предварительно размалывают и подвергают обогащению различными способами. Процессы обогащения сопровождаются образованием больших количеств твердых отходов в виде хвостов и пыли, уносимой с воздухом аспирационных систем и с газами сушильных установок.
Концентраты фосфатного сырья перерабатывают химическим путем двумя группами методов. К первой относится прямая кислотная или термическая переработка сырья с непосредственным получением готовых продуктов: суперфосфатов, обесфторенных фосфатов и др. Вторая группа – это разложение фосфатов с получением термической и экстракционной фосфорных кислот, которые служат для производства различных продуктов, в том числе и минеральных удобрений.
Например, при прямой сернокислотной обработке фосфатов получают простой суперфосфат, являющийся низкоконцентрированным фосфорным удобрением, содержание усвояемого Р2О5 в котором обычно не превышает 20 %. В этой связи вполне понятно стремление частично или полностью заменить серную кислоту на фосфорную. Последнюю в промышленности получают из фосфатов двумя методами: сернокислотным (экстракционным или мокрым) и электротермическим.
Отходы производства экстракционной фосфорной кислоты. В качестве твердого отхода производства фосфорной кислоты сернокислотным способом образуется фосфогипс – сульфат кальция с примесями фосфатов.
В зависимости от условий получения фосфорной кислоты в осадке образуется дигидрат CaSO4 ·2H2O, полугидрат CaSO4 ·0,5 H2O или безводный сульфат кальция, что и обуславливает соответствующие названия продуктов – фосфогипс, фосфополугидрат и фосфоангидрит. Эти отходы представляют собой серый мелкокристаллический комкующийся порошок влажностью до 25-40 % (в зависимости от условий получения фосфорной кислоты). В пересчете на сухое вещество они содержат до 94 % CaSO4. Основными примесями в них являются непрореагировавшие фосфаты, полуторные оксиды, соединения фтора и стронция, неотмытая фосфорная кислота, органические вещества. В них присутствуют соединения марганца, молибдена, кобальта, цинка, меди, редкоземельных и некоторых других элементов.
Основную массу образующегося фосфогипса в настоящее время сбрасывают в отвалы. Транспортирование фосфогипса в отвалы и его хранение связаны с большими капитальными и эксплуатационными затратами, достигающими 40 % от стоимости сооружения и эксплуатации основного производства, и осложняет работу заводов.
По агрохимической значимости для растений сере отводят четвертое место среди питательных элементов. В этой связи фосфогипс, содержащий до 22,1% серы и до 0,5% неотмытой фосфорной кислоты, может быть использован как содержащее серу и фосфор минеральное удобрение. Однако использование такого удобрения экономически оправдано только на сравнительно небольших расстояниях от заводов, не превышающих 500 км.
Утилизация фосфогипса возможна в цементной промышленности (в качестве минерализатора при обжиге и добавки к цементному клинкеру), для химической мелиорации солонцовых почв, для получения сульфата аммония, серной кислоты, гипсовых вяжущих материалов и изделий из них.
Для использования в цементном производстве фосфогипс гранулируют и подсушивают в барабанных сушилках до содержания гигроскопической влаги около 5 %. Применение фосфогипса в этом производстве уменьшает расход топлива, повышает производительность печей и качество цементного клинкера, удлиняет срок службы футеровки печей. Вместе с тем, широкомасштабное потребление фосфогипса в цементной промышленности сдерживается значительным содержанием таких регламентируемых для сырьевых материалов примесей, как водорастворимый Р2О5 и соединения фтора. С целью кондиционирования фосфогипса разработаны различные приемы его обработки перед дегидратацией и гранулированием. Обработку осуществляют водой, кислотами, щелочами. Утилизация фосфогипса в качестве минерализатора при обжиге сырьевых смесей для цементного клинкера обеспечивает экономический эффект по сравнению с использованием природного гипсового камня. Для получения цементного клинкера и диоксида серы приготовляют шихту, содержащую фосфоангидрит, кокс, песок и глину.
Разработанные схемы различаются в основном способом приготовления шихты и некоторыми элементами аппаратурного оформления. Различают три способа приготовления шихты: сухой, мокрый и комбинированный. При сухом способе этот процесс сводится к простому смешиванию компонентов, при мокром процесс ведут в присутствии воды. Комбинированный способ предусматривает мокрое приготовление шихты, а для получения диоксида серы и цементного клинкера используют дегидратированный шлам. В этом случае шихта имеет более однородный состав.
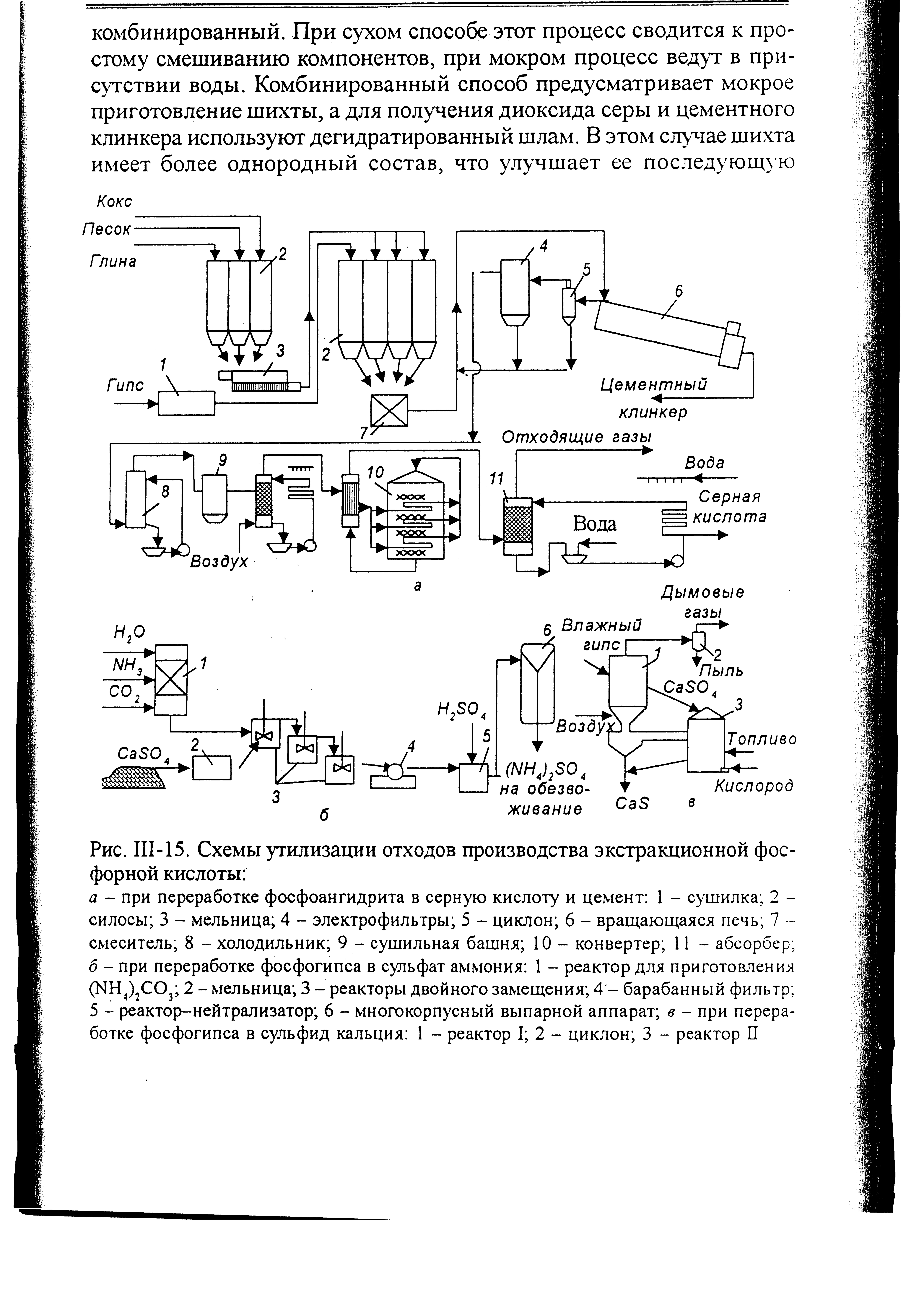
а – при переработке фосфоангидрита в серную кислоту и цемент: 1 - сушилка; 2 - силосы; 3 - мельница; 4 - электрофильтры; 5 - циклон; 6 - вращающаяся печь; 7 - смеситель; 8 - холодильник; 9 – сушильная башня; 10 - конвертер; 11 - абсорбер; б – при переработке фосфогипса в сульфат аммония: 1 - реактор для приготовления (NH4)2CO3; 2 - мельница; 3 – реакторы двойного замещения; 4 – барабанный фильтр; 5 – реактор-нейтрализатор; 6 - многокорпусный выпарной аппарат; в – при переработке фосфогипса в сульфид кальция: 1 – реактор №1; 2 - циклон; 3 – реактор №2
Рисунок 13 – Схемы утилизации отходов производства экстракционной фосфорной кислоты
Технологический процесс (рисунок 13 а) включает стадии сушки гипса, размола добавок и подготовки сырья для обжига (сухой способ). В процессе обжига шихты при температуре до 1400-1450 ºС идет восстановление сульфата кальция коксом с образованием клинкера. Присутствующие в шихте песок и глина способствуют интенсификации протекающей при обжиге конверсии сульфата кальция. В качестве топлива для обжиговой печи используют мазут, газ или распыленный уголь. Получающийся клинкер размалывают.
Горячий газ, содержащий диоксид серы, очищают в циклонах и электрофильтрах и подают на сернокислотную установку. На получение 1 т 98 %-ной серной кислоты (для типовой установки производительностью 1000 т/сут) расходуется 1,6 т фосфоангидрита, 0,14 т глины, 0,08 т песка, 0,11 т кокса, 85 м3 воды, 160 кВт · ч электроэнергии и 6,3 гДж (1,5 · 106 ккал) топлива.
Реакция разложения CaSO4 в присутствии восстановителя протекает в две стадии. На первой стадии образуются сульфид кальция и диоксид углерода (частично и СО):
CaSO4 + 2C→ CaS + 2CO2 (24)
Вторая стадия может быть представлена двумя параллельными процессами:
CaS + 3CaSO4 → 4CaO + 4SO2, (25)
CaS + 2SO2 → CaSO4 + S2 (26)
При 900 ºС скорости этих процессов близки, а при более высокой температуре преобладает первый из них. Процесс сопровождается побочными реакциями (CO2 + C → 2CO, 3 CaS + CaSO4 → 4 CaO + 2S2 , S2 + C → CS2) и прямым термическим разложением фосфоангидрита (при 1100 º С достигает 5 %). На побочные реакции расходуется углерод, поэтому его берут с избытком по отношению к стехиометрическому количеству согласно суммарной реакции:
2CaSO4 + С → 2CaO + 2SO2 + CO2 (27)
Избыток углерода составляет 20 % при переработке фосфоангидрита, полученного при экстракции кислоты из фосфоритов, и 30 % - в случае переработки апатитов. При больших избытках восстановителя получается слишком много сульфида кальция, при недостатке – велик процент неразложившегося сульфата кальция.
Себестоимость серной кислоты из фосфогипса выше, чем из флотационного колчедана.
Использование аммиака для производства сульфата аммония, получаемого в значительных количествах в качестве побочного продукта в таких крупнотоннажных производствах, как коксохимическое, менее экономично, чем для производства более концентрированных и агрохимических ценных азотных удобрений. Однако проблема использования процесса конверсии фосфогипса в сульфат аммония актуальна в связи с развитием азотно-сернокислотной переработки природных фосфатов для получения сложных удобрений.
Замена части серной кислоты на сульфат аммония в этих процессах дает определенную экономию и тем самым увеличивает эффективность производства сложных удобрений.
Это обстоятельство может быть проиллюстрировано на примере суммарных реакций процесса переработки азотнокислотной вытяжки по сульфатному способу:
2Ca5(PO4)3F + 12HNO3 + 4H2SO4 → 6H3PO4 + 6 Ca(NO3)2 + 4CaSO4 + 2HF
6H3PO4 + 6Ca(NO3)2 + 4CaSO4 + 2HF + 13NH3 →
→ 12NH4NO3 + 5CaHPO4 + NH4H2PO4 + 4CaSO4 + CaF2 (28)
2Ca5(PO4)3F + 12HNO3 + 13NH3 + 4H2SO4 → 12NH4NO3 + NH4H2PO4 +
5CaHPO4 + 4CaSO4 + CaF2 (29)
При получении из фосфогипса 1 т сульфата аммония выделяется 760 кг высококачественного мела, который может быть использован в производстве строительных материалов, для известкования почв и ряда других целей.
Переработка фосфогипса в сульфат аммония может быть организована и в более сложном варианте, предусматривающем прокалку осажденного мела с последующим растворением образующегося CaO путем его обработки растворами аммонийных солей (например, NH4Cl) и одновременным получением концентрата нерастворимых в них солей редкоземельных элементов. При этом насыщенный аммиаком раствор CaCl2 карбонизуют газами печей прокалки с целью регенерации NH4Cl, а повторно образующийся осадок CaCO3 вновь прокаливают с получением очищенного CaO, направляя газы прокалки на стадию карбонизации.
Большое внимание уделяется процессам переработки фосфогипса в элементную серу и известь, в серную кислоту и известь. Для этого сульфат кальция восстанавливают коксом или продуктами конверсии природного газа:
CaSO4 + 2C → CaS + 2CO2 (30)
CaSO4 + 4CO → CaS + 4CO2 (31)
CaSO4 + 4H2 → CaS + 4H2O (32)
Влажный фосфогипс обезвоживают в реакторе, необходимую температуру в котором поддерживают сжиганием углеводородов. Смесь газов (воздух и метан) служит также для конвертирования с взаимодействием находящегося во взвешенном слое безводного CaSО4 в CaS. Процесс протекает действием восстанавливающих реагентов, получающихся в результате неполного сгорания топлива при температуре около 850 ºС.
Далее CaS обрабатывают в виде водной суспензии газом CO2 с целью получения H2S:
CaS + H2O + CO2 → H2S + CaCO3 (33)
Выделяющийся Н2S может быть полностью сожжен до SO2 с последующим получением серной кислоты и частично окислен для получения элементной серы. Такой способ переработки фосфогипса представляет интерес для производственных объединений, включающих производство аммиака методом конверсии природного газа, при котором образуется значительное количество CO2 (Кирово-Чепецкий ЗМУ).

1 – смеситель; 2 – емкость-накопитель; 3 – расходная емкость; 4 - автоклав; 5 – сборник фильтрата; 6 - теплообменник; 7 – ленточный вакуум-фильтр; 8 - топка; 9 – сушильный барабан; 10 - бункер; 11 – циклон
Рисунок 14 – Схема опытно-промышленной установки переработки гипсовых отходов
На рисунке 14 представлена принципиальная схема установки производства α-полугидрата сульфата кальция из фосфогипса. Возможным технологическим вариантом утилизации фосфогипса по данной схеме является его гидротермальная обработка в виде пульпы (Ж : Т = 1) в автоклаве в течение 20-40 мин при температуре 140-170 ºС с последующим отфильтровыванием образующихся кристаллов полугидрата и их сушкой дымовыми газами с получением готового продукта.
Отходы производства термической фосфорной кислоты
Термическую фосфорную кислоту можно получать двумя способами: одно- и двухступенчатым. При одноступенчатом (непрерывном) способе печные газы сжигают, затем охлаждают, гидратируют и пропускают через электрофильтры для улавливания тумана образовавшейся фосфорной кислоты. Более совершенным является применяемый в настоящее время двухступенчатый способ, по которому фосфор сначала конденсируют из газов, а затем сжигают с последующей гидратацией образовавшегося P2O5 до фосфорной кислоты.
Термическое восстановление трикальцийфосфата проводят при помощи углерода (кокса) в электропечах (рисунок 15) с введением в шихту кремнезема в качестве флюса:
Ca3(PO4)2 + 5C + 2SiO2 → P2 + 5CO + Ca3Si2O7 (34)
Процесс сопровождается побочными реакциями, важнейшими из которых являются следующие:
Ca3(PO4)2 + 8C → Ca3P2 + 8CO (35)
Ca3P2 + 6C → 3CaC2 + P2 (36)
2CaF2 + SiO2 → 2CaO + SiF4 (37)
Fe2O3 + 3C → 2Fe +3CO (38)
4Fe + P2 → 2Fe2P (39)
На 1 т получаемого фосфора в электропечи образуется до 4000 м3 газа с высоким содержанием оксида углерода, 0,1-0,5 т феррофосфора, 0,05-0,35 т пыли и 7,5-11 т силикатного шлака, а также около 50 кг ферросодержащих шламов.
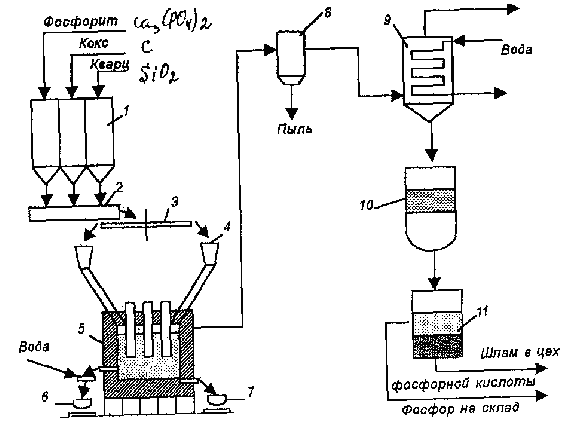
1 – бункеры сырья; 2 - смеситель; 3 – кольцевой питатель; 4 – бункер шихты; 5 - электропечь; 6 – ковш для шлака; 7 – ковш для феррофосфора; 8 - электрофильтр; 9 - конденсатор; 10 – сборник жидкого фосфора; 11 - отстойник
Рисунок 15 – Схема производства фосфора
Утилизация шлама, феррофосфора, пыли и газов. Образующийся в конденсаторах жидкий фосфор собирается под слоем воды в сборниках, откуда сифоном отправляется в отстойники. Здесь фосфор расслаивается с образованием шлама (фосфор, пыль, диоксид кремния, сажа), из которого получают фосфорную кислоту.
Образующиеся при восстановлении Ca3(PO4)2 и Fe2O3 фосфиды железа (Fe2P, Fe3P ) периодически сливают из печи. При застывании их расплава образуется чугуноподобная масса – феррофосфор, выход которого зависит от содержания в исходной руде оксидов железа. Его используют в основном в металлургии как присадку в литейном производстве или как раскислитель, а также в качестве защитного материала от радиоактивного излучения.
Пыль, собирающаяся в электрофильтрах при очистке печных газов, может быть использована как минеральное удобрение, так как она содержит до 22 % усвояемого P2O5 и K2O (иногда до 15%).
Газ, покидающий конденсаторы, содержит до 85 % (об.) оксида углерода, 0,05% фосфора, 0,2-0,4 % PH3, 0,5-1 % H2S и другие примеси. Его обычно используют как топливо, но целесообразнее после очистки от примесей (PH3, H2S, P и др.) использовать СО в химических синтезах.
Утилизация шлаков. Электротермическая возгонка фосфора сопровождается образованием больших количеств огненно-жидких шлаковых расплавов, содержащих в среднем 38-43 % SiO2, 2-5 % Al2O3, 44-48 % CaO, 0,5-3 % P2O5, 0,5-1 % MgO, 0,5-1 % Fe2O3 и другие компоненты. Процесс утилизации осложняет присутствие в них фтора (примерно до 3,6 % в виде CaF2), фосфора (примерно до 3,6 % в виде P2O5), серы, что не дает возможности непосредственно применить их для утилизации в доменных процессах. Переработка фосфорных шлаков направлена на использование их в строительных материалах в виде гранулированных шлаков, шлакового щебня, шлаковой пемзы, минеральной ваты, литых строительных изделий и материалов.
Производство шлаово пемзы. Вспучивание расплавленных фосфорных шлаков для производства шлаковой пемзы вододутьевым способом может быть организовано на установках, выполненных в различных вариантах. Схема одной из таких установок показана на рисунке 16 а.
Расплавленный шлак дробят струей воды под давлением в вододутьевом аппарате и дополнительно разрушают при ударе об экран, после чего он попадает на настил пластинчатого конвейера, где вспучивается в результате выделения газов и охлаждается. Застывшие горячие куски шлака конвейером подают в дробилку, где их измельчают примерно до размера 100 мм. После этого шлак охлаждают в чашевом охладителе и транспортером передают на последующую переработку. Выделяющиеся при вспучивании шлака газы отводят из газосборной камеры и галереи через газоотводные трубы.
Наиболее легкую шлаковую пемзу получают при переработке расплавленных шлаков бассейновым способом. Однако сложность герметизации опрокидных бассейнов и отвода выделяющихся в них газов и паров заставляет отказаться от их применения для переработки фосфорных шлаков. Для этой цели требуются бассейны иных типов. На рисунке 16 б представлена схема получения шлаковой пемзы с применением стационарного бассейна с толкающим разгружателем.
Производство шлаковой пемзы бассейновым способом является высокоэффективным процессом переработки фосфорных шлаков. Экономическая эффективность использования 1 т шлаков в виде шлаковой пемзы по сравнению с керамзитом составляла в ценах 1990 г. 10 руб. Вододутьевой способ еще эффективнее.
Гранулированные фосфорные шлаки можно использовать как активную минеральную добавку к цементной шихте (до 15 %). Их применение в цементной промышленности позволяет снизить расход топлива на 6-7 %. Шлакопортландцемент на основе фосфорных шлаков имеет высокую прочность в изделиях, которая превышает прочность обычных цементов.
Использование фосфорных шлаков, таким образом, позволяет повысить рентабельность основного производства и получить дополнительную продукцию без затрат дорогого и дефицитного сырья.
В связи с важностью извлечения редкоземельных элементов при переработке фосфатного сырья в последние годы значительное внимание уделяется вопросам химической переработки фосфорных шлаков с получением ряда ценных продуктов и концентратов редкоземельных элементов.
При выщелачивании шлаков электротермического производства фосфора из апатитового сырья азотной кислотой может быть получен дисперсный диоксид кремния и раствор нитрата кальция, перерабатываемый в известково-аммиачную селитру, используемую в качестве удобрения, с одновременным получением соединений редкоземельных элементов их экстракцией трибутилфосфатом и реэкстрацией водой с последующим осаждением аммиаком в виде гидроксидов. Обработка таких шлаков соляной кислотой обеспечивает возможность получения концентрата редкоземельных элементов наряду с производством высокочистого диоксида кремния и товарного хлорида кальция.
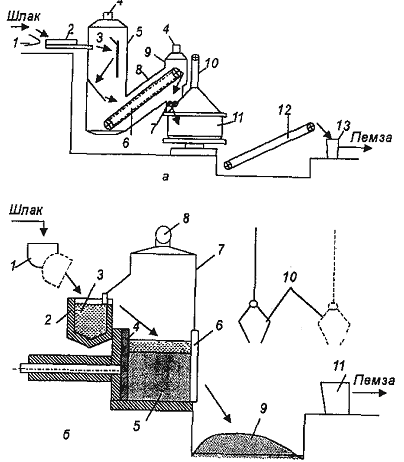
а – вододутьевой способ: 1 – шлаковый желоб электропечи; 2 - струйный вододутьевой аппарат; 3 - экран; 4 – газоотводные трубы; 5 - газосборная камера; 6 – пластинчатый конвейер; 7 – валковая дробилка; 8 - наклонная галерея; 9 – разгрузочная камера; 10 - воздуховод; 11 – чашевый охладитель; 12 - транспортер; 13 – приемный бункер дробильно-сортировочного узла; б – бассейный способ: 1 – шлаковый ковш; 2 – шлаковый желоб; 3 - гидрозатвор; 4 - толкатель; 5 – стационарный бассейн; 6 – откидная стенка; 7 - газосборная камера; 8 – отводная труба; 9 – приямок для шлаковой пемзы; 10 - грейферный захват; 11 – приемный бункер дробильно-сортировочного узла
Рисунок 16 – Схемы производства шлаковой пемзы
Комплексное использование фосфатного сырья. Выше отмечалось образование больших масс отходов в процессах обогащения фосфатных руд. Например, на 1 т апатитового концентрата в настоящее время получают 0,6-0,7 т нефелинового концентрата. Одним из важнейших путей утилизации таких отходов является их комплексная переработка, обеспечивающая получение ряда ценных и дефицитных продуктов: соды, поташа, цемента, глинозема.
В соответствии с этой технологией нефелиновый концентрат в порошкообразном виде спекают с известняком или мелом:
(Na,K)2O·Al2O3·nSiO2+2CaCO3→Na2O·K2O·Al2O3+n(2CaO·SiO2)+2CO2 (40)
При последующем выщелачивании спека водой образовавшиеся алюминаты натрия и калия переходят в раствор. Затем водную пульпу подвергают фильтрованию от нерастворимых силикатов кальция, которые направляют в цементное производство, а фильтрат, содержащий Na2SiO3, - на автоклавное обескремнивание при давлении 0,6-0,7 МПа:
5Na2SiO3+3Na2O·Al2O3+aq→(3-4)Na2O·3Al2O3+5SiO2·nH2O+(8-10)NaOH+aq (41)
Образующийся осадок после отстаивания пульпы в сгустителе в виде шлама возвращают на спекание, а осветленный раствор подвергают карбонизации газами печей спекания:
Na2O · K2O ·Al2O3 + 2CO2 + 3H2O → 2Al(OH)3 ↓+Na2CO3 + K2CO3 (42)
Для получения глинозема осадок Al(OH)3 отфильтровывают и подвергают кальцинации. В фильтрате (карбонатовых щелоках) кроме Na2CO3 и K2CO3 содержится определенное количество K2SO4 и бикарбонатов натрия и калия, что обусловлено присутствием SO2 в газах печей спекания и режимом процесса карбонизации. Для предотвращения коррозии аппаратуры кислые соли при помощи гидроксида натрия (каустической соды) переводят в углекислые:
NaHCO3 + NaOH → Na2CO3 + H2O, (43)
KHCO3 + KOH→ K2CO3 + H2O (44)
Для получения нужного количества щелочей часть карбонатных щелоков подвергают каустификации:
(Na,K)2CO3 + Ca(OH)2 → 2 (Na,K)OH + CaCO3 (45)
Отфильтрованный и промытый шлам, полученный при каустификации, направляют на спекание. Содержащиеся в карбонатных щелоках соли выделяют затем методом политермического разделения, основанным на их различной растворимости при разных температурах (рисунок 17).
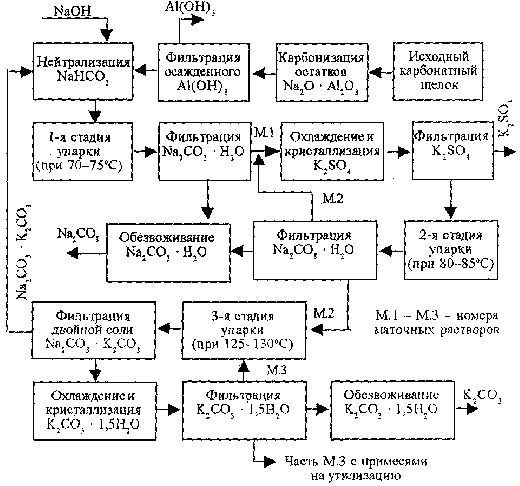
Рисунок 17 – Схема переработки карбонатного щелока из нефелина
Карбонатный щелок, нейтрализованный щелочью (для перевода кислых солей в нейтральные), после карбонизации для освобождения остатков Al2O3 и выделения осажденного Al(OH)3 подают на I стадию упаривания, где из него выделяется 25-30 % соды. После отделения кристаллов соды маточник №1 смешивают с маточником №2, получаемым на II стадии упаривания, и этот раствор охлаждают до 35 ºС.
В процессе охлаждения в осадок выпадает K2SO4, который затем отделяют от раствора, поступающего на II стадию упаривания, в результате которой выделяют остальные 70-75 % имевшейся в карбонатном щелоке соды. Отделенные на обеих стадиях упаривания осадки соды смешивают и обезвоживают.
Часть маточника №2, не пошедшую на смешение с маточником №1, подают на III стадию упаривания, в результате которой кристаллизуется смесь двойной соли K2CO3 · Na2CO3, Na2CO3 и K2SO4. Осадок отделяют от суспензии и передают на растворение в нейтрализованном карбонатном щелоке, а жидкую фазу охлаждают для выделения K2CO3 · 1,5 H2O, который затем отфильтровывают и высушивают. Маточник №3 возвращают на III стадию упаривания и частично выводят из системы в виде поташного раствора (≈ 50% K2CO3).
Разработан и безупарочный способ переработки карбонатных щелоков, при котором путем их карбонизации и высаливания аммиаком можно выделить в осадок в виде NaHCO3 до 97% Na2CO3 и до 85% K2SO4. Кроме того, по этому способу получается аммиачная вода, являющаяся жидким удобрением.
Значительный интерес представляет разработка процессов совместной переработки нефелина и фосфогипса. В этом случае наряду с получением глинозема, цемента, соды и поташа могут быть получены цемент и сульфаты калия и натрия. Процесс протекает следующим образом:
(Na,K2)O Al2O3 2SiO2 + 2CaSO4 → (Na,K)2О∙ Al2О3 + 2CaSiO3 + 2SO2 + O2 (46)
Таким образом, замена известняка на фосфогипс в процессе комплексной переработки нефелина может позволить не только комплексно использовать апатитовое сырьё, но и способствовать утилизации твёрдых отходов производства экстракционной фосфорной кислоты.
