
- •Предисловие
- •Содержание
- •Основы строения и реакционной способности органических соединений
- •Классификация
- •2. Номенклатура
- •3. Химическая связь
- •6. Изомерия
- •Реакционная способность основных
- •1. Углеводороды
- •Механизм реакции радикального замещения:
- •2. Региоселективность реакций радикального замещения
- •Особенности реакций в малых циклах
- •Замещённые углеводороды
- •I. Реакции нуклеофильного замещения (sn1 и sn2)
- •Реакции элиминирования (е)
- •Альдегиды и кетоны
- •4. Карбоновые кислоты
- •Гетерофункциональные соединения
- •Гетероциклические соединения
- •Углеводы
- •Гомополисахариды
- •Аминокислоты
- •I. Химическая
- •II. Биологическая
- •Пептиды
- •Нуклеиновые кислоты (полинуклеотиды)
- •И нуклеотидов
- •Раздел I.
- •Глава 1.
Пептиды
Пептиды построены из остатков аминокислот, соединенных пептидной –СО–NH– связью.
Строение пептидной связи
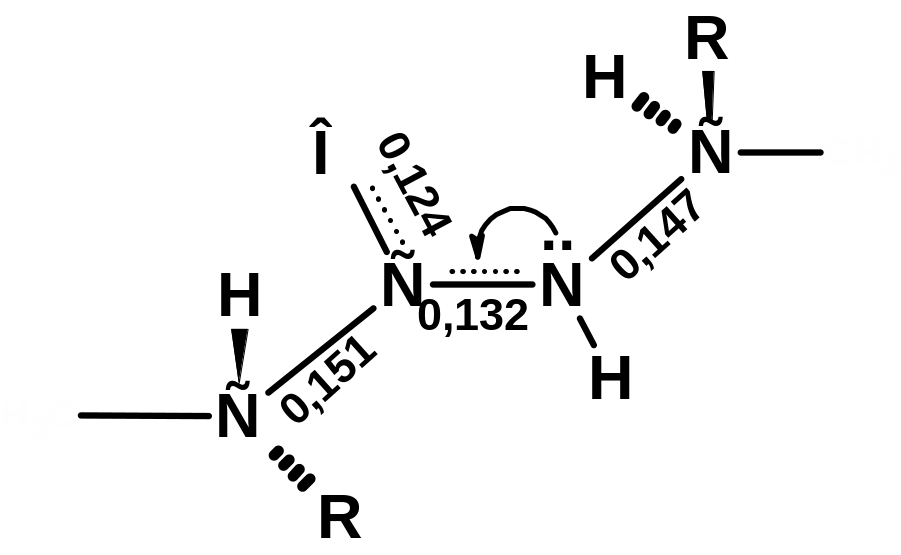
Пептидная связь обладает цис- и трансформой относительно -углеродных атомов, расположенных по обе стороны от этой связи.

Трансформа более предпочтительна, т.к. стерически она менее затруднена R-группами, чем цис-форма.
Пептиды образуются либо при распаде белков, либо в реакции поликонденсации α–аминокислот.

БЕЛКИ
Классификации белков
Химическая

Биологическая

Ценность белка определяется:
содержанием незаменимых аминокислот
степенью усваиваемости организмом.
Уровни структурной организации белка
Первичная – последовательность соединения аминокислот в бел-
ковой цепи (линейная).
Связи ковалентные:
–СО–NH– пептидная (основная)
–S–S– дисульфидная (вспомогательная).

Вторичная – способ укладки полипептидной цепи (двухмерная).
Связь водородная
(α-спираль – внутримолекулярная,
β-структура – межмолекулярная).


α-спираль β-структура
Рис. 13. Вторичная структура белков
Третичная – способ укладки пролипептидной цепи в пространст-
ве (трёхмерная).
Связи: ковалентные –S–S– , водородные, гидрофобные, ионные, диполь-дипольные взаимодействия.
водородные связи
гидрофобные
взаимодействия
электростатические
взаимодействия
электростатические
взаимодействия








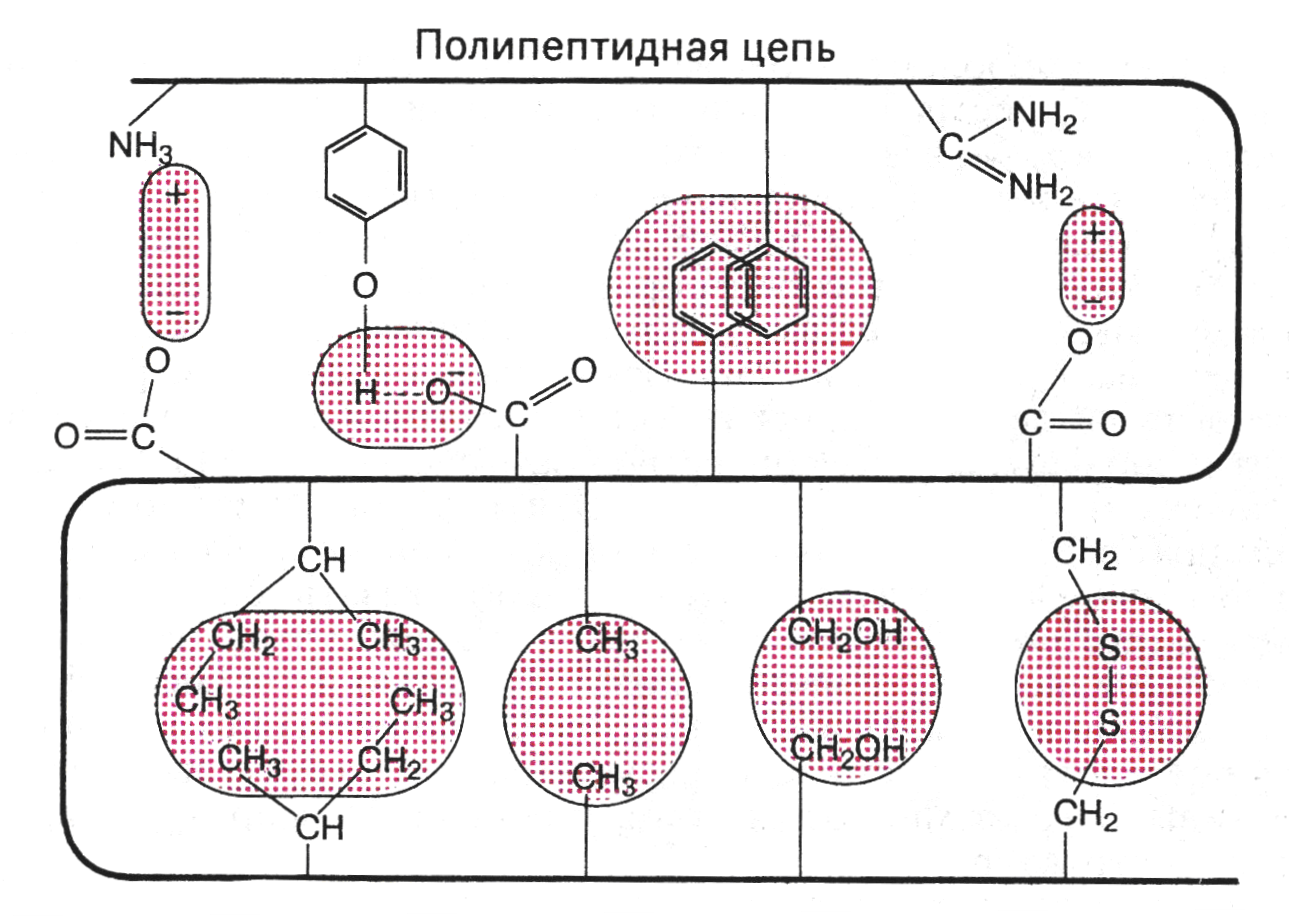
гидрофобные
взаимодействия
диполь-дипольные
взаимодействия
дисульфидные
связи
Рис. 14. Связи, стабилизирующие третичную структуру белков
четвертичная – способ укладки в пространстве отдельных субъединиц, имеющих собственную первичную, вторичную и третичную структуры. При этом формируется единое в структурном и функциональном отношении образование.
Связи: гидрофобные взаимодействия, водородные и ионные связи.

Рис. 15. Четвертичная структура гемоглобина
Нуклеиновые кислоты (полинуклеотиды)
Нуклеиновые кислоты (полинуклеотиды) – полимеры, структурной единицей которых являются мононуклеотиды, соединённые между собой фосфодиэфирными связями.
Схема 9. Состав мононуклеотидов
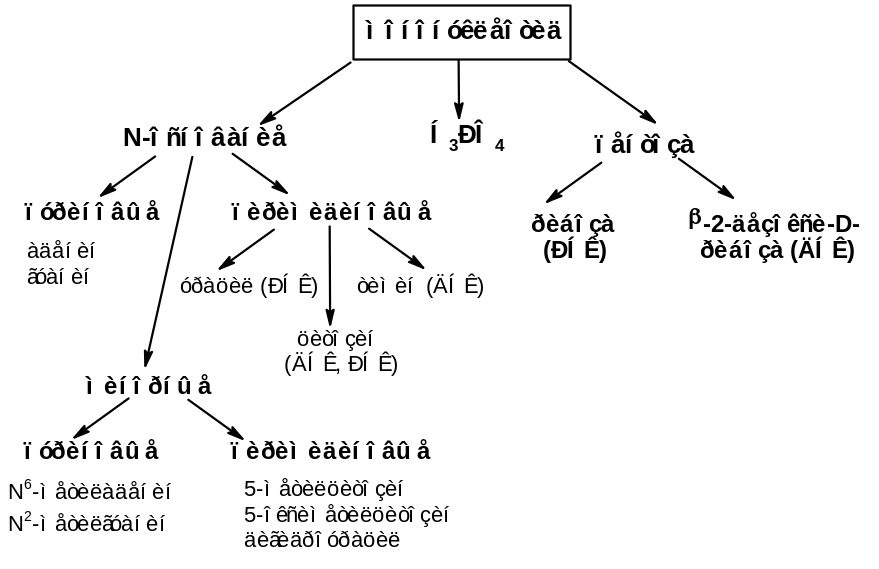
Строение азотистых оснований
Пиримидиновые


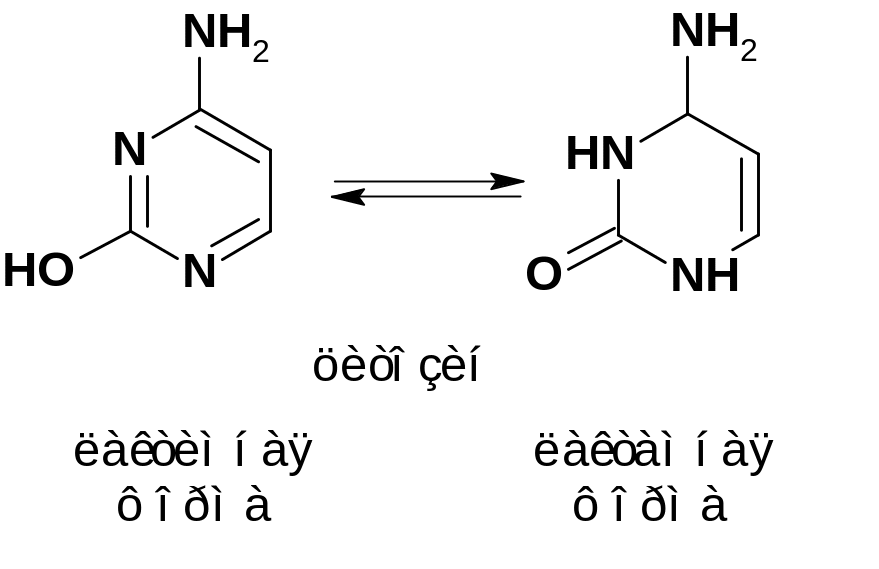
Пуриновые

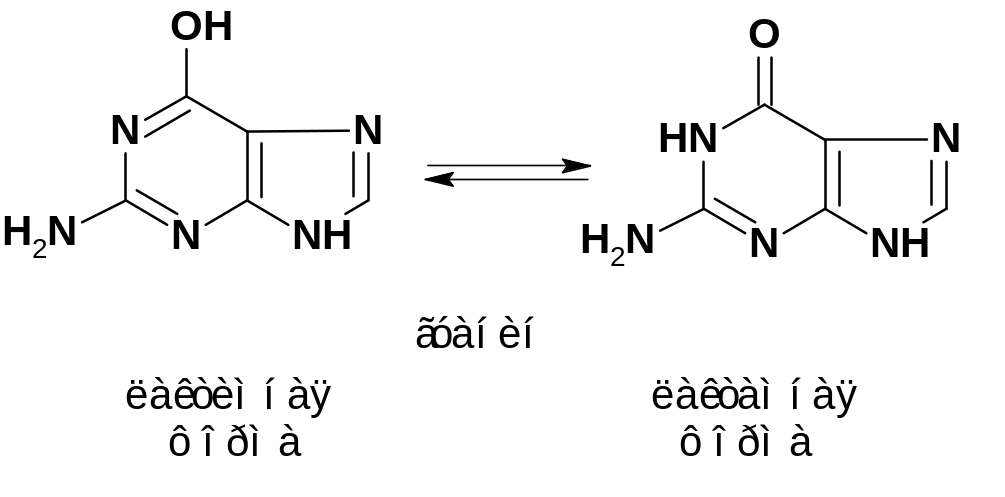
Минорные азотистые основания


Пентозы

N-основание + пентоза = нуклеозид
нуклеозид + остаток фосфорной кислоты = нуклеотид
Таблица 22. Номенклатура основных нуклеозидов
