
- •Министерство образования и науки российской федерации
- •Содержание:
- •Кинематика поступательного и вращательного движения
- •Динамика поступательного и вращательного движения.
- •Работа. Энергия
- •Законы сохранения в механике
- •Элементы специальной теории относительности
- •Средняя энергия молекул
- •Распределения Максвелла и Больцмана
- •Первое начало термодинамики
- •Второе начало термодинамики. Энтропия.
- •Электростатическое поле в вакууме
- •Законы постоянного тока
- •Магнитостатика
- •Явление электромагнитной индукции
- •Электрические и магнитные свойства вещества
- •Свободные и вынужденные колебания
- •Сложение гармонических колебаний
- •Волны. Уравнение волны
- •Энергия волны. Перенос энергии волной
- •Уравнения Максвелла
- •Интерференция и дифракция света
- •Поляризация и дисперсия света
- •Тепловое излучение. Фотоэффект
- •Эффект Комптона. Световое давление
- •Дуализм свойств микрочастиц. Соотношение неопределенностей Гейзенберга
- •Спектр атома водорода. Правило отбора
- •Уравнение Шредингера
- •Ядерные реакции
- •Ядро. Элементарные частицы
- •Фундаментальные взаимодействия.
Распределения Максвелла и Больцмана
№1
 На
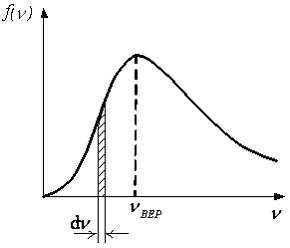
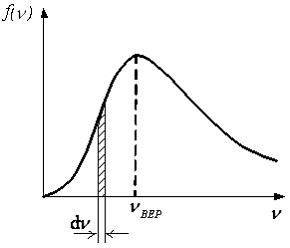
рисунке представлен график функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
На
рисунке представлен график функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
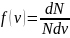 - доля молекул, скорости которых заключены
в интервале скоростей от v
до
- доля молекул, скорости которых заключены
в интервале скоростей от v
до
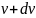 в
расчете на единицу этого интервала.
в
расчете на единицу этого интервала.
Для этой функции неверными являются утверждения, что …
1.При понижении температуры величина максимума функции уменьшается
2.При понижении температуры площадь под кривой уменьшается
Решение:
Полная
вероятность равна:
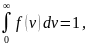 то есть площадь, ограниченная кривой
распределения Максвелла, равна единице
и при изменении температуры не
изменяется. Из формулы наиболее вероятной
скорости,
то есть площадь, ограниченная кривой
распределения Максвелла, равна единице
и при изменении температуры не
изменяется. Из формулы наиболее вероятной
скорости,
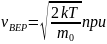 и
которой функция
и
которой функция
 максимальна,
следует, что при повышении температуры
максимум функции сместится вправо,
следовательно, высота максимума
уменьшится.
максимальна,
следует, что при повышении температуры
максимум функции сместится вправо,
следовательно, высота максимума
уменьшится.
№ 2
На рисунке представлен график функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
–
доля молекул, скорости которых заключены
в интервале скоростей от
2
На рисунке представлен график функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
–
доля молекул, скорости которых заключены
в интервале скоростей от
![]() до
до
![]() в
расчете на единицу этого интервала.
Для
этой функции верными
являются утверждения, что …
в
расчете на единицу этого интервала.
Для
этой функции верными
являются утверждения, что …
1.С увеличением температуры максимум кривой смещается вправо
2.При изменении температуры площадь под кривой не изменяется
№3
З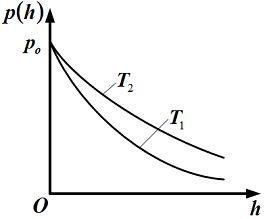 ависимости
давления
ависимости
давления
 идеального
газа во внешнем однородном поле силы
тяжести от высоты
для двух разных температур представлены
на рисунке.
Для графиков этих функций
неверными
являются утверждения, что …
идеального
газа во внешнем однородном поле силы
тяжести от высоты
для двух разных температур представлены
на рисунке.
Для графиков этих функций
неверными
являются утверждения, что …
1.Температура Т1 выше температуры Т2
2.Давление газа на высоте h равно давлению на «нулевом уровне» (h = 0), если температура газа стремиться к абсолютному нулю
Решение:
Зависимость
давления идеального газа от высоты
![]() для
некоторой температуры
определяется
барометрической формулой:
для
некоторой температуры
определяется
барометрической формулой: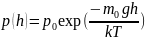 ,
где
,
где давление на высоте h=0,
давление на высоте h=0,
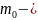 масса
молекулы, g
– ускорение свободного падения, k
– постоянная Больцмана. Из формулы
следует, что при постоянной температуре
давление газа уменьшается с высотой по
экспоненциальному закону тем медленнее,
чем больше температура
.
Давление
масса
молекулы, g
– ускорение свободного падения, k
– постоянная Больцмана. Из формулы
следует, что при постоянной температуре
давление газа уменьшается с высотой по
экспоненциальному закону тем медленнее,
чем больше температура
.
Давление
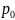 определяется
весом всего газа и не меняется при
изменении температуры.
определяется
весом всего газа и не меняется при
изменении температуры.
№4
Н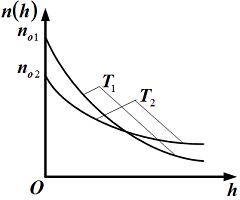 а
рисунке представлены графики зависимости
концентрации молекул идеального газа
а
рисунке представлены графики зависимости
концентрации молекул идеального газа
 от высоты
над уровнем моря для двух разных
температур –
от высоты
над уровнем моря для двух разных
температур –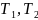 (распределение
Больцмана).
Для графиков этих
функций верными являются утверждения,
что …
(распределение
Больцмана).
Для графиков этих
функций верными являются утверждения,
что …
1.Температура
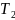 выше температуры
выше температуры

2.Концентрация молекул газа на «нулевом уровне» (h=0) с повышением температуры уменьшается
Решение:
Зависимость
концентрации молекул идеального газа
от высоты для некоторой температуры Т
определяется распределением Больцмана:
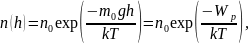 где
где
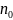 концентрация молекул на высоте h=0,
концентрация молекул на высоте h=0,
 масса
молекулы, g
- ускорение свободного падения, k
- постоянная Больцмана. Из формулы
следует, что при постоянной температуре
концентрация газа больше там, где меньше
потенциальная энергия его молекул
,
и уменьшается с высотой по экспоненциальному
закону тем медленнее, чем больше
температура: T2
>T1.
С повышением температуры из-за увеличения
энергии хаотического теплового движения
молекулы более равномерно распределяются
по высоте, и поэтому концентрация молекул
газа на «нулевом уровне» h=0
уменьшается, а на высоте h
увеличивается.
масса
молекулы, g
- ускорение свободного падения, k
- постоянная Больцмана. Из формулы
следует, что при постоянной температуре
концентрация газа больше там, где меньше
потенциальная энергия его молекул
,
и уменьшается с высотой по экспоненциальному
закону тем медленнее, чем больше
температура: T2
>T1.
С повышением температуры из-за увеличения
энергии хаотического теплового движения
молекулы более равномерно распределяются
по высоте, и поэтому концентрация молекул
газа на «нулевом уровне» h=0
уменьшается, а на высоте h
увеличивается.
№ 5
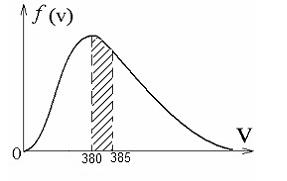
На
рисунке представлен график функции
распределения молекул кислорода по
скоростям(распределение Максвелла)для
температуры Т=273 К, при скорости 380 м/с
функция достигает максимума. Здесь
5
На
рисунке представлен график функции
распределения молекул кислорода по
скоростям(распределение Максвелла)для
температуры Т=273 К, при скорости 380 м/с
функция достигает максимума. Здесь
 плотность
вероятности или доля молекул, скорости
которых заключены в интервале скоростей
плотность
вероятности или доля молекул, скорости
которых заключены в интервале скоростей
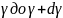 в
расчете на единицу этого интервала. Для
распределения Максвелла справедливы
утверждения, что…
в
расчете на единицу этого интервала. Для
распределения Максвелла справедливы
утверждения, что…
Решение:
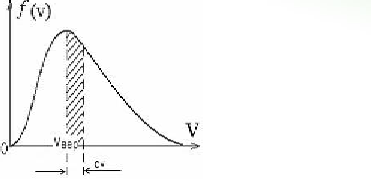 Функция
распределения Максвелла f(
Функция
распределения Максвелла f( имеет смысл плотности вероятности
имеет смысл плотности вероятности
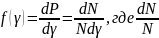 доля
молекул, скорости которых заключены в
интервале от
доля
молекул, скорости которых заключены в
интервале от
 до
до
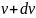 .
В нашем случае d
.
В нашем случае d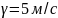 вблизи
вблизи
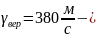 наиболее
вероятной скорости молекул, близкой к
которой движется большее число молекул
dN-число
молекул, скорости которых заключены в
интервале от 380 м/с до 385 м/с, N-число
молекул газа. Площадь заштрихованной
полоски
наиболее
вероятной скорости молекул, близкой к
которой движется большее число молекул
dN-число
молекул, скорости которых заключены в
интервале от 380 м/с до 385 м/с, N-число
молекул газа. Площадь заштрихованной
полоски
 определяет
долю молекул ,скорости которых заключены
в интервале от 380 м/с до 385 м/с. С ростом
температуры максимум кривой смещается
вправо, высота максимума убывает.
Наиболее вероятная скорость
определяет
долю молекул ,скорости которых заключены
в интервале от 380 м/с до 385 м/с. С ростом
температуры максимум кривой смещается
вправо, высота максимума убывает.
Наиболее вероятная скорость
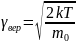 зависит
от температуры газа: она увеличивается
с повышением температуры. Вероятность
того,что величина скорости может принять
хотя бы какое-нибудь значение (достоверное
событие), равна единице
зависит
от температуры газа: она увеличивается
с повышением температуры. Вероятность
того,что величина скорости может принять
хотя бы какое-нибудь значение (достоверное
событие), равна единице
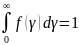 поэтому
при изменении температуры площадь под
кривой остается равной единице. Если
точно задана скорость
поэтому
при изменении температуры площадь под
кривой остается равной единице. Если
точно задана скорость
 следовательно
следовательно
 .
.
№6
Формула
Больцмана
 характеризует распределение
частиц,находящихся в состоянии
хаотического теплового движения ,в
потенциальном силовом поле,в частности
распределение молекул по высоте в
изотермической атмосфере.Соотнесите
рисунки и соответствующие им утверждения…
характеризует распределение
частиц,находящихся в состоянии
хаотического теплового движения ,в
потенциальном силовом поле,в частности
распределение молекул по высоте в
изотермической атмосфере.Соотнесите
рисунки и соответствующие им утверждения…
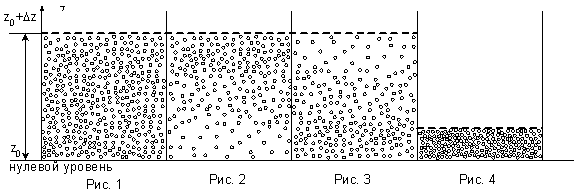
Утверждения:
Распределение молекул по кинетическим энергиям Рис.1.
Распределение молекул воздуха в атмосфере Земли Рис.3.
Распределение
молекул не является больцмановским и
описывается функцией
 Рис.2.
Рис.2.
Распределение молекул в силовом поле при очень высокой температуре, когда энергия хаотического теплового движения значительно превосходит потенциальную энергию молекул. Рис.1.
Распределение
молекул в силовом поле при температуре
T .
Рис.4.
.
Рис.4.
Решение:
Концентрация
молекул в однородном поле силы тяжести
убывает с высотой по закону
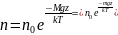 (распределение Больцмана на рис.3), где
n-концентрация
молекул на высоте
(распределение Больцмана на рис.3), где
n-концентрация
молекул на высоте
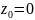 ,
М-молярная масса, m-
масса молекулы, g-
ускорение свободного падения, R-
универсальная газовая постоянная,
k-постоянная
Больцмана,T-
температруа. В предельных случаях: если
,
М-молярная масса, m-
масса молекулы, g-
ускорение свободного падения, R-
универсальная газовая постоянная,
k-постоянная
Больцмана,T-
температруа. В предельных случаях: если
 и молекулы равномерно распределяются
по высоте (рис.1); если
и молекулы равномерно распределяются
по высоте (рис.1); если
 и молекулы располагаются на нулевом
уровне (рис.4). Если число молекул,имеющих
большую потенциальную энергию,увеличивается
по экспоненциальному закону
,то
такое распределение можно назвать
«антибольцмановским», или инверсным.
и молекулы располагаются на нулевом
уровне (рис.4). Если число молекул,имеющих
большую потенциальную энергию,увеличивается
по экспоненциальному закону
,то
такое распределение можно назвать
«антибольцмановским», или инверсным.
№ 7
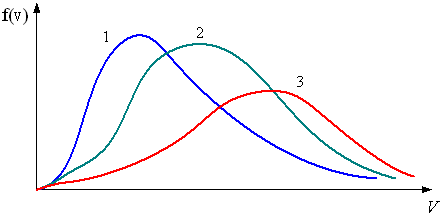
На
рисунке представлены графики функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
–
доля молекул, скорости которых заключены
в интервале скоростей от
до
в расчете на единицу этого интервала.
Для этих функций верными являются
утверждения, что …
7
На
рисунке представлены графики функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
–
доля молекул, скорости которых заключены
в интервале скоростей от
до
в расчете на единицу этого интервала.
Для этих функций верными являются
утверждения, что …
Решение:
Функция
Максвелла имеет вид
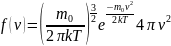 Полная вероятность равна:
Полная вероятность равна:
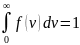 ,
то есть площадь, ограниченная кривой
распределения Максвелла, равна единице
и при изменении температуры не
изменяется. Из формулы наиболее вероятной
скорости
,
то есть площадь, ограниченная кривой
распределения Максвелла, равна единице
и при изменении температуры не
изменяется. Из формулы наиболее вероятной
скорости
 ,
при которой функция
,
при которой функция
 максимальна,
следует, что при повышении температуры
максимум функции сместится вправо,
следовательно, высота максимума
уменьшится. Если сравнивать распределения
Максвелла по скоростям различных газов
при одной и той же температуре, то при
увеличении массы молекулы газа максимум
функции сместится влево, следовательно,
высота максимума увеличится.
максимальна,
следует, что при повышении температуры
максимум функции сместится вправо,
следовательно, высота максимума
уменьшится. Если сравнивать распределения
Максвелла по скоростям различных газов
при одной и той же температуре, то при
увеличении массы молекулы газа максимум
функции сместится влево, следовательно,
высота максимума увеличится.
Ответ: распределение 1 соответствует газу, имеющему наибольшую массу молекул (при одинаковой температуре
