
- •Министерство образования и науки российской федерации
- •Содержание:
- •Кинематика поступательного и вращательного движения
- •Динамика поступательного и вращательного движения.
- •Работа. Энергия
- •Законы сохранения в механике
- •Элементы специальной теории относительности
- •Средняя энергия молекул
- •Распределения Максвелла и Больцмана
- •Первое начало термодинамики
- •Второе начало термодинамики. Энтропия.
- •Электростатическое поле в вакууме
- •Законы постоянного тока
- •Магнитостатика
- •Явление электромагнитной индукции
- •Электрические и магнитные свойства вещества
- •Свободные и вынужденные колебания
- •Сложение гармонических колебаний
- •Волны. Уравнение волны
- •Энергия волны. Перенос энергии волной
- •Уравнения Максвелла
- •Интерференция и дифракция света
- •Поляризация и дисперсия света
- •Тепловое излучение. Фотоэффект
- •Эффект Комптона. Световое давление
- •Дуализм свойств микрочастиц. Соотношение неопределенностей Гейзенберга
- •Спектр атома водорода. Правило отбора
- •Уравнение Шредингера
- •Ядерные реакции
- •Ядро. Элементарные частицы
- •Фундаментальные взаимодействия.
Средняя энергия молекул
№1
Средняя
кинетическая энергия молекул газа при
температуре
 зависит от их конфигурации и структуры,
что связано с возможностью различных
видов движения атомов в молекуле и самой
молекулы. При условии, что имеет место
только поступательное и вращательное
движение молекулы как целого, средняя
кинетическая энергия молекул азота
зависит от их конфигурации и структуры,
что связано с возможностью различных
видов движения атомов в молекуле и самой
молекулы. При условии, что имеет место
только поступательное и вращательное
движение молекулы как целого, средняя
кинетическая энергия молекул азота
 равна …
равна …
№2
В соответствии с законом равномерного
распределения энергии по степеням
свободы средняя кинетическая энергия
молекулы идеального газа при температуре
T
равна:
 .
.
 Здесь
Здесь
 ,
где
,
где ,
, и
и –
число степеней свободы поступательного,
вращательного и колебательного движений
молекулы соответственно. Для гелия (He)
число i
равно …
–
число степеней свободы поступательного,
вращательного и колебательного движений
молекулы соответственно. Для гелия (He)
число i
равно …
№3
В соответствии с законом равномерного
распределения энергии по степеням
свободы средняя кинетическая энергия
молекулы идеального газа при температуре
T
равна:
.
Здесь
,
где
,
и
–
число степеней свободы поступательного,
вращательного и колебательного движений
молекулы соответственно. Для
азота
 средняя кинетическая энергия
колебательного движения молекулы
равна …
средняя кинетическая энергия
колебательного движения молекулы
равна …
№4 Средняя кинетическая энергия молекулы идеального газа при температуре T равна . Здесь , При условии, что имеют место только поступательное и вращательное движение, для водяного пара (Н2O) число i равно …
№5
Средняя
кинетическая энергия молекул газа при
температуре
![]() зависит
от их конфигурации и структуры, что
связано с возможностью различных видов
движения атомов в молекуле и самой
молекулы. При условии, что имеет место
поступательное, вращательное движение
молекулы как целого и колебательное
движение атомов в молекуле, средняя
кинетическая энергия молекулы кислорода
(
зависит
от их конфигурации и структуры, что
связано с возможностью различных видов
движения атомов в молекуле и самой
молекулы. При условии, что имеет место
поступательное, вращательное движение
молекулы как целого и колебательное
движение атомов в молекуле, средняя
кинетическая энергия молекулы кислорода
( )
равна …
)
равна …
№6 Если не учитывать колебательные движения в молекуле водяного пара, то отношение кинетической энергии вращательного движения к полной кинетической энергии молекулы равно …
№7
При
комнатной температуре отношение
 молярных теплоемкостей при постоянном
давлении и постоянном объеме равно
молярных теплоемкостей при постоянном
давлении и постоянном объеме равно
 для …
для …
№8
На каждую степень свободы движения
молекулы проходится одинаковая энергия,
равная
 постоянная Больцмана,
постоянная Больцмана,
 температура по шкале Кельвина). Средняя
кинетическая энергия атомного водорода
равна …
температура по шкале Кельвина). Средняя
кинетическая энергия атомного водорода
равна …
Распределения Максвелла и Больцмана
№ 1
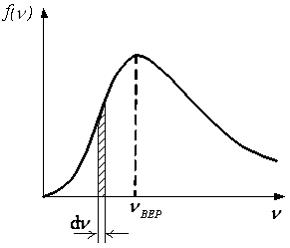
На
рисунке представлен график функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
1
На
рисунке представлен график функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
 - доля молекул, скорости которых заключены
в интервале скоростей от v
до
- доля молекул, скорости которых заключены
в интервале скоростей от v
до
 в
расчете на единицу этого интервала.
в
расчете на единицу этого интервала.
Для этой функции неверными являются утверждения, что …
1.При понижении температуры величина максимума функции уменьшается
2.При понижении температуры площадь под кривой уменьшается
№ 2
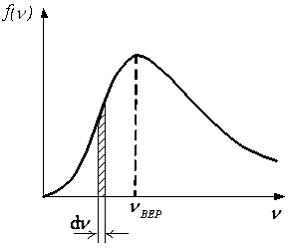
На рисунке представлен график функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
–
доля молекул, скорости которых заключены
в интервале скоростей от
2
На рисунке представлен график функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
–
доля молекул, скорости которых заключены
в интервале скоростей от
![]() до
до
![]() в
расчете на единицу этого интервала.
Для
этой функции верными
являются утверждения, что …
в
расчете на единицу этого интервала.
Для
этой функции верными
являются утверждения, что …
№ 3
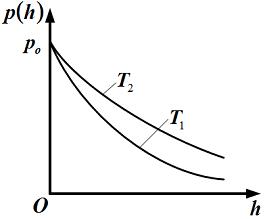
Зависимости
давления
3
Зависимости
давления
 идеального
газа во внешнем однородном поле силы
тяжести от высоты
для двух разных температур представлены
на рисунке.
Для графиков этих функций
неверными
являются утверждения, что …
идеального
газа во внешнем однородном поле силы
тяжести от высоты
для двух разных температур представлены
на рисунке.
Для графиков этих функций
неверными
являются утверждения, что …
1.Температура Т1 выше температуры Т2
2.Давление газа на высоте h равно давлению на «нулевом уровне» (h = 0), если температура газа стремиться к абсолютному нулю
№ 4
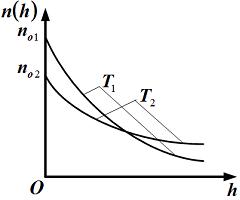
На
рисунке представлены графики зависимости
концентрации молекул идеального газа
4
На
рисунке представлены графики зависимости
концентрации молекул идеального газа
 от высоты
над уровнем моря для двух разных
температур –
от высоты
над уровнем моря для двух разных
температур – (распределение
Больцмана).
Для графиков этих
функций верными являются утверждения,
что …
(распределение
Больцмана).
Для графиков этих
функций верными являются утверждения,
что …
1.Температура
 выше температуры
выше температуры
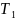
2.Концентрация молекул газа на «нулевом уровне» (h=0) с повышением температуры уменьшается
№ 5
На
рисунке представлен график функции
распределения молекул кислорода по
скоростям(распределение Максвелла)для
температуры Т=273 К, при скорости 380 м/с
функция достигает максимума. Здесь
5
На
рисунке представлен график функции
распределения молекул кислорода по
скоростям(распределение Максвелла)для
температуры Т=273 К, при скорости 380 м/с
функция достигает максимума. Здесь
 плотность
вероятности или доля молекул, скорости
которых заключены в интервале скоростей
плотность
вероятности или доля молекул, скорости
которых заключены в интервале скоростей
 в
расчете на единицу этого интервала. Для
распределения Максвелла справедливы
утверждения, что…
в
расчете на единицу этого интервала. Для
распределения Максвелла справедливы
утверждения, что…
№6
Формула
Больцмана
 характеризует распределение
частиц,находящихся в состоянии
хаотического теплового движения ,в
потенциальном силовом поле,в частности
распределение молекул по высоте в
изотермической атмосфере.Соотнесите
рисунки и соответствующие им утверждения…
характеризует распределение
частиц,находящихся в состоянии
хаотического теплового движения ,в
потенциальном силовом поле,в частности
распределение молекул по высоте в
изотермической атмосфере.Соотнесите
рисунки и соответствующие им утверждения…
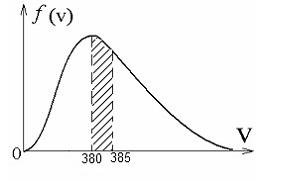
Утверждения:
Распределение молекул по кинетическим энергиям Рис.1.
Распределение молекул воздуха в атмосфере Земли Рис.3.
Распределение
молекул не является больцмановским и
описывается функцией
 Рис.2.
Рис.2.
Распределение молекул в силовом поле при очень высокой температуре, когда энергия хаотического теплового движения значительно превосходит потенциальную энергию молекул. Рис.1.
Распределение
молекул в силовом поле при температуре
T .
Рис.4.
.
Рис.4.
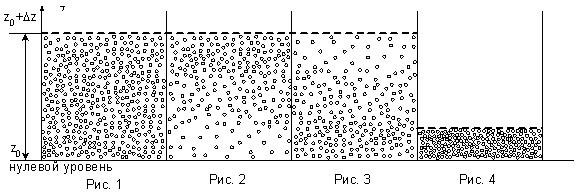
№ 7
На
рисунке представлены графики функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
–
доля молекул, скорости которых заключены
в интервале скоростей от
до
в расчете на единицу этого интервала.
Для этих функций верными являются
утверждения, что …
7
На
рисунке представлены графики функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
–
доля молекул, скорости которых заключены
в интервале скоростей от
до
в расчете на единицу этого интервала.
Для этих функций верными являются
утверждения, что …
