
- •Физическая химия
- •Москва 2008
- •Предисловие
- •Содержание
- •Работа № 1 определение молярной рефракции жидкостей.
- •Краткое теоретическое введение
- •Последовательность выполнения работы
- •Обработка и оформление результатов
- •Вопросы к работе
- •Последовательность выполнения работы
- •Обработка и оформление результатов
- •Вопросы к работе
- •Последовательность выполнения работы
- •Калибровка и проверка работы стеклянного электрода.
- •Определение константы диссоциации уксусной кислоты:
- •Обработка и оформление результатов
- •Вопросы к работе
- •Последовательность выполнения работы
- •Обработка и оформление результатов.
- •Вопросы к работе
- •Литература
- •Работа № 5 определение скорости разложения комплексного оксалата марганца.
- •Краткое теоретическое введение
- •Последовательность выполнения работы
- •Обработка и оформление результатов
- •Вопросы к работе
- •I метод.
- •I I метод ( графический).
- •III метод ( по периоду полупревращения).
- •Последовательность выполнения работы
- •Обработка и оформление результатов
- •Вопросы к работе
- •Литература.
- •Приложения
- •Атомные рефракции.
- •Изменение энтальпии при образовании водных растворов неорганических веществ и солей органических кислот.
- •Некоторые фундаментальные физико-химические константы.
- •Зимон Анатолий Давыдович, Павлов Андрей Николаевич физическая химия
Последовательность выполнения работы
Калибровка и проверка работы стеклянного электрода.
Н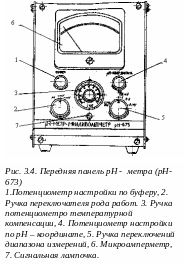 еобходимо
последовательно измерить рН 6 буферных
смесей, представленных в табл. 3.1, с
одновременным измерением э.д.с.
гальванического элемента, состоящего
из хлорсеребряного и стеклянного
электродов.
еобходимо
последовательно измерить рН 6 буферных
смесей, представленных в табл. 3.1, с
одновременным измерением э.д.с.
гальванического элемента, состоящего
из хлорсеребряного и стеклянного
электродов.
Для этого необходимо:
Подключить рН-673 к сети и прогреть его в течение 15 минут.
Поместить стеклянный и каломельный электроды в ячейку с исследуемым раствором. Электроды должны быть помещены в раствор полностью, на 15-20 мм.
Ручку 2 переключить на рН.
Шкала ручки 5 должна стоять на диапазоне 1 – 14.
При проверке рН по стандартным буферным смесям настройка должна производиться ручкой 4.
При измерении э.д.с. гальванической цепи, состоящей из стеклянного и хлорсеребряного электродов, погруженных в исследуемый раствор ручка 2 должна стоять в положении +mV, а затем (при измерении отрицательных э.д.с.) –mV. Все показания должны быть умножены на 100 и занесены в таблицу 3.2.
Перед каждым последующим измерением электроды необходимо промывать водой, а затем протирать фильтровальной бумагой.
Таблица 3.1.
Название буферной смеси |
Формула |
рН |
Калий тетраоксалат |
КНС2О4Н2С2О4×2Н2О |
1,68 |
Калий виннокислый кислый |
С4Н5О6К |
3,56 |
Калий фталевокислый кислый |
С8Н5О4К |
4,01 |
Смесь калия фосфорнокислого и фосфорнокислого натрия |
К2НРО4 Nа2НРО4 |
6,86 |
Натрий тетраборнокислый |
Nа2В4О7×10Н2О |
9,18 |
Затем стоят график в координатах E=f(pH), причем на оси ординат откладывают значения э.д.с., а на оси абсцисс - рН буферных растворов. Если в указанных координатах получается прямая линия, то это означает, что стеклянный электрод пригоден для измерений.
Определение константы диссоциации уксусной кислоты:
Производят измерение э.д.с. гальванического элемента, состоящего из хлорсеребряного и стеклянного электродов, опущенных в буферные растворы (СН3СООН + СН3СООNa) разных концентраций, заданных преподавателем и заносят эти данные в табл.3.2.
Значения рН буферных растворов (СН3СООН + СН3СООNa) находят по графику (рис. 3.2.) методом графической интерполяции по данным э.д.с. растворов.
Рассчитывают среднее значение
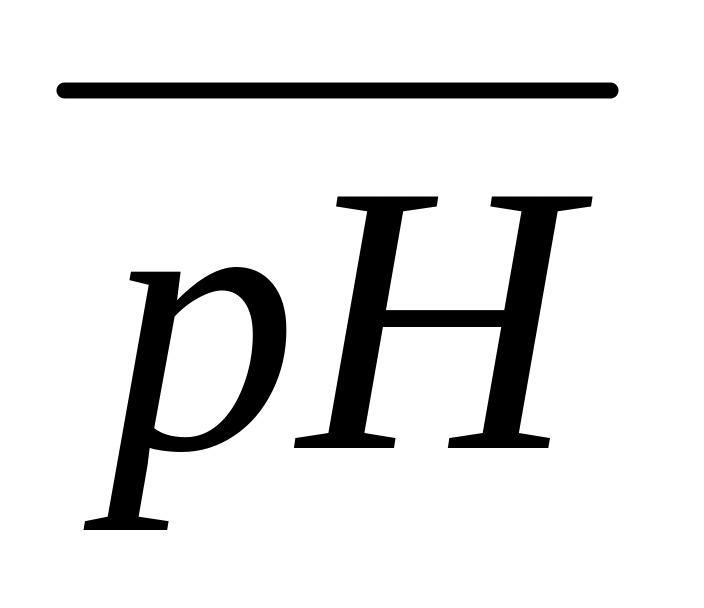 ацетатных
буферных растворов, определенных из
графика (рис.3.2)
=ΣрНi/n,
где n
- число измерений.
ацетатных
буферных растворов, определенных из
графика (рис.3.2)
=ΣрНi/n,
где n
- число измерений.
По формуле
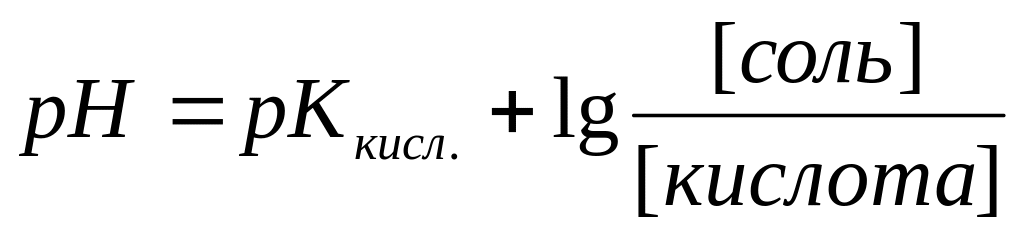 определяют lgКдис=-рН
уксусной кислоты и затем находят
Кдис.=
10-рН
.
определяют lgКдис=-рН
уксусной кислоты и затем находят
Кдис.=
10-рН
.
Обработка и оформление результатов
Таблица 3.2.
Стандарт. буферные растворы |
Ацетатные буферные растворы |
|||
рН стандарт. растворов |
э.д.с. элемента, Е, В. |
Концентрация уксусной кислоты и уксуснокислого натрия, М |
э.д.с. ацетатных буферных растворов, Е, В. |
рНi по графику |
|
|
|
|
|
|
|
|
|
|
