
- •Физическая химия
- •Москва 2008
- •Предисловие
- •Содержание
- •Работа № 1 определение молярной рефракции жидкостей.
- •Краткое теоретическое введение
- •Последовательность выполнения работы
- •Обработка и оформление результатов
- •Вопросы к работе
- •Последовательность выполнения работы
- •Обработка и оформление результатов
- •Вопросы к работе
- •Последовательность выполнения работы
- •Калибровка и проверка работы стеклянного электрода.
- •Определение константы диссоциации уксусной кислоты:
- •Обработка и оформление результатов
- •Вопросы к работе
- •Последовательность выполнения работы
- •Обработка и оформление результатов.
- •Вопросы к работе
- •Литература
- •Работа № 5 определение скорости разложения комплексного оксалата марганца.
- •Краткое теоретическое введение
- •Последовательность выполнения работы
- •Обработка и оформление результатов
- •Вопросы к работе
- •I метод.
- •I I метод ( графический).
- •III метод ( по периоду полупревращения).
- •Последовательность выполнения работы
- •Обработка и оформление результатов
- •Вопросы к работе
- •Литература.
- •Приложения
- •Атомные рефракции.
- •Изменение энтальпии при образовании водных растворов неорганических веществ и солей органических кислот.
- •Некоторые фундаментальные физико-химические константы.
- •Зимон Анатолий Давыдович, Павлов Андрей Николаевич физическая химия
Последовательность выполнения работы
Получить от лаборанта или преподавателя реактивы: хлорид калия и соль, теплоту растворения которой следует определить.
Во внутренний стакан калориметра налить 100 см3 дистиллированной воды и поместить якорь магнитной мешалки.
Вставить стакан с водой во внешний (имеющий теплоизоляцию) стакан и установить их на магнитную мешалку.
Тумблером "Вращение" (8) включить магнитную мешалку.
Термометр, закреплённый в штативе, погрузить в воду. Взаимное расположение частей калориметра должно быть таким, чтобы якорь магнитной мешалки находился (и вращался) в центре стакана; термометр должен быть погружён так, чтобы баллончик с ртутью был полностью покрыт водой.
Термометр должен быть смещён от центра, и не должен касаться стенок или дна стакана.
На лабораторных весах отвесить навеску хлорида калия с точностью 0,01 г.
Измерять температуру воды в течение 9 минут, через каждую минуту считывая показания термометра с максимальной точностью, которую допускает цена деления.
Во время, равное 10 минутам от начала измерений, всыпать хлорид калия в воду и продолжить измерения температуры с 11-ой минуты по 20-ую через каждую минуту.
Результаты измерений занести в таблицу 2.1.
Выключить магнитную мешалку. Разобрать калориметр. Внутренний стакан освободить от раствора хлорида калия, ополоснуть водопроводной и затем дистиллированной водой.
А
Выполнить п.п. 2-5.На лабораторных весах отвесить навеску исследуемой соли с точностью 0,01г.
 Выполнить
п.п. 8-11 для исследуемой соли.
Выполнить
п.п. 8-11 для исследуемой соли.
Обработка и оформление результатов
С
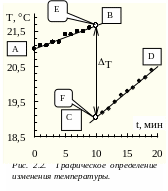
Для точного расчета изменения температуры при растворении соли вычерчивают график на миллиметровой бумаге, на оси абсцисс откладывают время в минутах, а на оси ординат температуру (рис. 2.2.).
На графике получаются две наклонные прямые линии, угол наклона которых будет зависеть от разности температур между калориметром и окружающей средой.
Линию АВ продолжают вправо, а линию СД влево. Через точку Е. соответствующую 10-ой минуте, проводят прямую параллельную оси ординат. Расстояние между точками пересечения этой прямой FЕ с линиями АВ и СД будет соответствовать изменению температуры DТ в результате растворения соли.
Определив во графику изменения температуры при растворении KCl значение DТ1, вычисляют постоянную калориметра К во уравнению:
К=(DHраств.×n)/DТ1, (2.4)
где DHраств определяется по табл.2 приложения с учетом числа молей воды на 1 моль растворённого вещества, n – количество вещества KCl.
По графику изменения температуры при растворении исследуемой соли определяется DТ2, а расчёт теплоты растворения проводится по формуле:
DHраств= (К×DТ2) /n, (2.5)
где К – постоянная калориметра,
DТ2 – изменение температуры при растворении исследуемой соли,
n – количество вещества исследуемой соли.
Таблица результатов измерений.
Таблица 2.1.
Хлористый калий |
Исследуемая соль |
||
Навеска, ______ г |
Навеска, ______ г |
||
Время от начала опыта в мин. |
Температура. 0С |
Время от начала опыта в мин. |
Температура. 0С |
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 |
------------- |
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 |
------------- |
