
- •5 Курс, 9 семестр 12 часов семинаров и 24 часа лабораторных занятий к.Х.Н., доцент н.Н.Бобров
- •Катализ как явление
- •Классификация каталитических процессов по фазовому принципу и специфика гетерогенных каталитических процессов
- •Свойства гетерогенных катализаторов
- •Влияние процессов переноса
- •Внешнедиффузионная область
- •Тестирование катализаторов
- •Проточные методы
- •Вопросы к работе
Свойства гетерогенных катализаторов
Основными свойствами катализатора, определяющими экономику каталитического процесса, являются активность, селективность, стабильность, иногда потребители рассматривают способность катализаторов к регенерации.
Каталитические свойства:
Каталитическая активность характеризует, в какой мере данное вещество или определенная композиция веществ является катализатором. В общем случае мерой каталитической активности должно служить изменение скорости химической реакции в результате введения в систему катализатора:
a = wк - w0(1 - φ),
где wк – скорость реакции в присутствии катализатора, моль/(см3∙с); w0 - скорость реакции без катализатора, моль/(см3∙с); φ – доля объема системы, занимаемого катализатором и не доступного для реагирующих веществ. В подавляющем большинстве случаев второй член соотношения настолько мал, что им можно пренебречь. Таким образом, под каталитической активностью подразумевают скорость реакции в присутствии катализатора, т.е. количество исходного реагента, которое данное количество катализатора способно переработать в единицу времени при заданных составе реакционной среды и температуре. При этом чаще всего скорость каталитической реакции относят к единице массы m
a = wк/m
или единицы объема катализатора Vк
a = wк/Vк.
При исследовании твердых катализаторов целесообразно определять удельную каталитическую активность – скорость каталитической реакции, отнесенная к единице поверхности катализатора S
a = wк/S
или, относя скорость каталитической реакции к числу активных центров на поверхности N, определять «число оборотов» t.n. (turnover number) – число каталитических актов на активном центре в секунду при данной температуре, давлении, отношении реагентов, степени превращения
t.n. = wк/N.
Селективность характеризует способность катализатора осуществлять процесс в направлении образования определенных продуктов реакции. При определении различают дифференциальную и интегральную селективность.
Дифференциальная селективность равна отношение скорости накопления соответствующего продукта к сумме скоростей всех реакций, протекающих на данном катализаторе в тех же условиях с участием реагентов:
S = w/∑wi.
Интегральная селективность – отношение общего количества определенного продукта, образовавшегося при конечном изменении степени превращения исходного вещества, к теоретически возможному (при образовании только данного продукта):
S = mпр./mтеор.
- стабильность
- способность к регенерации
Влияние процессов переноса
Гетерогенные катализаторы обычно характеризуются очень развитой внутренней поверхностью, площадь которой может составлять десятки и даже сотни квадратных метров на грамм катализатора. Активные центры катализатора располагаются преимущественно на внутренней поверхности, внутри зерен, катализатора. Поэтому изменения концентраций и температуры у поверхности катализатора может очень сильно исказить наблюдаемую скорость реакции.
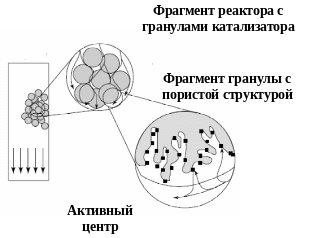
В случае гетерогенной каталитической реакции в общем случае можно выделить следующие этапы ее протекания:
диффузия реагентов к поверхности катализатора (внешняя диффузия);
диффузия реагентов в порах катализатора (внутренняя диффузия);
адсорбция реагентов на активном центре;
реакция;
десорбция продуктов;
диффузия продуктов в порах катализатора;
диффузия продуктов от поверхности.
Изменения концентраций и температуры зависят от соотношения скоростей химической реакции и процессов переноса. Скорость суммарного каталитического процесса будет определяться скоростью самой медленной стадии. В связи с этим различают следующие области протекания каталитического процесса:
кинетическая область, когда скорость суммарного процесса определяется химическими процессами: (адсорбцией, реакцией на поверхности, десорбцией);
внешнедиффузионная область, когда скорость суммарного процесса лимитируется скоростью переноса массы реагентов или тепла из газовой (жидкой) фазы к внешней поверхности зерна катализатора;
внутридиффузионная область, когда скорость суммарного процесса лимитируется диффузией реагентов в порах зерна катализатора.
Обычно условия эксперимента при исследовании каталитических свойств выбирают таким образом, чтобы процессы транспорта не являлись лимитирующими, то есть скорость всего процесса определялась только скоростью химической реакции.
