
- •Ахметов м. А.
- •Оглавление
- •Введение
- •Стандарт основного общего образования по химии
- •Обязательный минимум содержания основных образовательных программ
- •Требования к уровню подготовки выпускников
- •I. Первоначальные химические понятия
- •II. Основные классы неорганических веществ
- •III. Периодический закон. Химическая связь
- •6. В ряду химических элементов с а1 Са число электронных слоев в их атомах
- •IV. Электролитическая диссоциация. Окислительно-восстановительные реакции
- •V. Химия неметаллов спецификация теста
- •VI. Химия металлов
- •1) Fe2o3 2) FeO 3) Fe3o4 4) смесь Fe2o3 и FeO
- •VII. Первоначальные представления об органических веществах спецификация теста
- •16. Объем кислорода, затраченный на сжигание 5,6 л этана, составит (л) …. (ответ округлите до целых)
- •VIII. Итоговый тест за курс химии основной школы
- •Литература
- •Стандарты школьного химического образования/ http://ug.Ru
Требования к уровню подготовки выпускников
В результате изучения химии ученик должен
знать / понимать
химическую символику: знаки химических элементов, формулы химических веществ и уравнения химических реакций;
важнейшие химические понятия: химический элемент, атом, молекула, относительные атомная и молекулярная массы, ион, химическая связь, вещество, классификация веществ, моль, молярная масса, молярный объем, химическая реакция, классификация реакций, электролит и неэлектролит, электролитическая диссоциация, окислитель и восстановитель, окисление и восстановление;
основные законы химии: сохранения массы веществ, постоянства состава, периодический закон;
уметь
называть: химические элементы, соединения изученных классов;
объяснять: физический смысл атомного (порядкового) номера химического элемента, номеров группы и периода, к которым элемент принадлежит в периодической системе Д.И. Менделеева; закономерности изменения свойств элементов в пределах малых периодов и главных подгрупп; сущность реакций ионного обмена;
характеризовать: химические элементы (от водорода до кальция) на основе их положения в периодической системе Д.И.Менделеева и особенностей строения их атомов; связь между составом, строением и свойствами веществ; химические свойства основных классов неорганических веществ;
определять: состав веществ по их формулам, принадлежность веществ к определенному классу соединений, типы химических реакций, валентность и степень окисления элемента в соединениях, тип химической связи в соединениях, возможность протекания реакций ионного обмена;
составлять: формулы неорганических соединений изученных классов; схемы строения атомов первых 20 элементов периодической системы Д.И.Менделеева; уравнения химических реакций;
обращаться с химической посудой и лабораторным оборудованием;
распознавать опытным путем: кислород, водород, углекислый газ, аммиак; растворы кислот и щелочей, хлорид-, сульфат-, карбонат-ионы;
вычислять: массовую долю химического элемента по формуле соединения; массовую долю вещества в растворе; количество вещества, объем или массу по количеству вещества, объему или массе реагентов или продуктов реакции;
использовать приобретенные знания и умения в практической деятельности и повседневной жизни для:
безопасного обращения с веществами и материалами;
экологически грамотного поведения в окружающей среде;
оценки влияния химического загрязнения окружающей среды на организм человека;
критической оценки информации о веществах, используемых в быту;
приготовления растворов заданной концентрации.
I. Первоначальные химические понятия
СПЕЦИФИКАЦИЯ ТЕСТА
№ задания |
Требование к уровню подготовки выпускников |
Виды деятельности |
||
Воспроизведение знаний |
Применение знаний и умений |
|||
В знакомой ситуации |
В измененной ситуации |
|||
1 |
Правила работы в школьной лаборатории |
+ |
|
|
2. |
Лабораторная посуда и оборудование. Очистка веществ |
+ |
|
|
3. |
Знаки химических элементов |
+ |
|
|
4. |
Атомы и молекулы |
|
+ |
|
5. |
Очистка веществ. Разделение смесей |
+ |
|
|
6. |
Вещества и тела
|
+ |
|
|
7. |
Чистые вещества и смеси |
+ |
|
|
8. |
Моль |
|
+ |
|
9. |
Правила безопасности |
|
+ |
|
10. |
Химический элемент |
|
+ |
|
11. |
Относительные атомная и молекулярная массы. Молярный объем |
|
+ |
|
12. |
Молярная масса. |
|
+ |
|
13. |
Молярный объем |
|
|
+ |
14 |
Вещество и химический элемент |
|
|
+ |
15 |
Массовая доля химического элемента по формуле соединения |
|
|
+ |
16. |
Приготовление растворов. Массовая доля вещества в растворе |
|
|
+ |
ВАРИАНТ 1
В химической лаборатории нельзя
проводить опыты
смешивать жидкости
принимать пищу
работать в халате
Жидкости фильтруют с помощью
выпарительной чашки и спиртовки
воронки и фильтровальной бумаги
ступки и пестика
кристаллизатора и стеклянной палочки
Знак химического элемента железо
1) |
F |
2) |
Fe |
3) |
Ge |
4) |
Cu |
Атомы различных элементов различаются
только по массе
только по цвету
по массе и по цвету
по массе и по объему
Для разделения несмешивающихся жидкостей используют
делительную воронку
обычную воронку
ступку и пестик
круглодонную колбу и холодильник
Вещество
стакан
гвоздь
железо
конверт
Смесь
вода
сахар
соляная кислота
медь
Моль.
число частиц, содержащихся в 1 г любого вещества
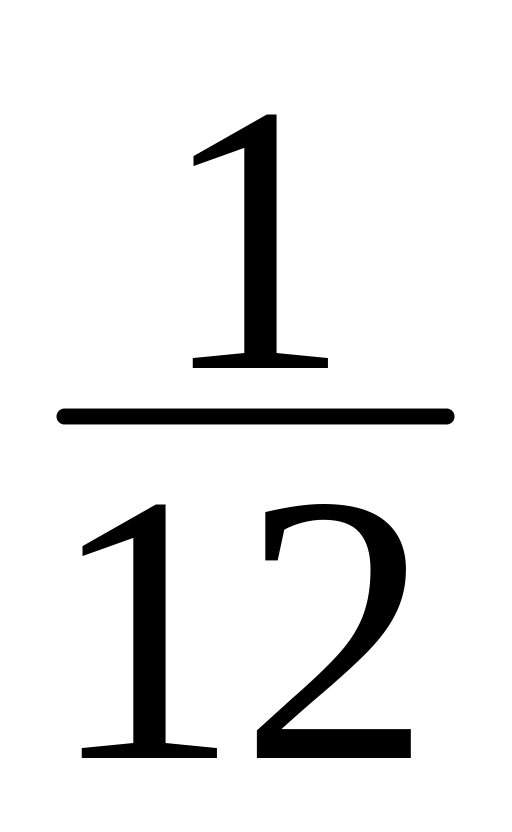 часть
массы изотопа углерода 12С
часть
массы изотопа углерода 12Сединица, которой в химии измеряют количество вещества
число молекул, содержащихся в 22,4 л газа при нормальных условиях
Если воду добавить к серной кислоте, то
вода не будет смешиваться с серной кислотой
произойдет сильное охлаждение воды
возможно вскипание и разбрызгивание раствора серной кислоты
серная кислота, как водопоглощающее вещество, быстро прореагирует с водой
Химический элемент - это
1) разновидность атомов
2) тип вещества
3) класс молекул
4) то же, что и простое вещество
Относительная атомная единица массы эквивалентна
1 грамму
массе атома водорода
1/12 массы атома углерода
1/16 массы атома кислорода
Молярная масса кислорода О2 составляет (г/моль)
1) |
8 |
2) |
16 |
3) |
32 |
4) |
48 |
Два моля воды при комнатной температуре занимают объем около
1) 18 мл 2) 22,4 мл 3) 36 мл 4) 44,8 мл
Во фразе «зубная паста с фтором» под словом «фтор» понимается
химический элемент
простое вещество
атомы фтора
молекулы фтора
Массовая доля кислорода в диоксиде серы SO2 составляет, %...
20 г сахара растворили в чашке чая (180 г). Массовая доля сахара в полученном растворе составит (%)
ВАРИАНТ 2
В химической лаборатории МОЖНО
употреблять пищу
склоняться для лучшего обзора над приборами при проведении опыта
выливать реактивы в раковину
выполнять опыты согласно инструкции
Вещества в химической лаборатории растирают с помощью
ступки и пестика
стеклянной палочки и кристаллизатора
любых подручных средств
выпарительной чашки и штатива
3. Знак химического элемента гелий
1) |
Ge |
2) |
He |
3) |
Ga |
4) |
Hg |
4. Газообразные вещества, такие как кислород, азот, водород состоят из мельчайших частиц, называемых
1) |
атомы |
2) |
молекулы |
3) |
химические элементы |
4) |
ионы |
5. Для разделения смешивающихся жидкостей используют
круглодонную колбу, холодильник, приемник, штатив, электрическую плитку
делительную воронку
обычную воронку, фильтровальную бумагу и стакан
плоскодонную колбу, дефлегматор, холодильник, спиртовку, приемник
6. Тело
1) графит
2) алмаз
3) бумага
4) гвоздь
7. Смесь, которую можно разделить с помощью магнита
1) сера и сахар
2) медь и стекло
3) песок и мел
4) медные и стальные опилки
8. Одинаковые количества различных веществ имеют
1) равные массы
2) равные объемы
3) равное число структурных единиц
4) равное число атомов
9. Емкости с кислотой вместимостью более 3 л категорически запрещено переносить в
1) металлическом ведре 3) корзине с прокладками из поролона или стружек
2) руках 4) пластмассовом ведре
10. Химический элемент
1) то же, что и простое вещество 3) то из чего состоит вещество
2) наименьшая химически неделимая частица 4) вид атомов
11. Молярный объем.
объем 1 г любого вещества
объем часть массы изотопа углерода 12С
объем, занимаемый одним молем вещества при данных условиях
число молекул, содержащихся в 22,4 л газа при нормальных условиях
12. Масса двух молей газообразного кислорода составляет, г
1) |
16 |
2) |
32 |
3) |
48 |
4) |
64 |
13. Один моль воды при комнатной температуре занимает объем около
1) 18 мл 2) 22,4 мл 3) 36 мл 4) 44,8 мл
14. Во фразе «йодированная соль» под словом «йодированная» понимается
1) химический элемент
2) простое вещество
3) атомы йода
4) молекулы йода
15. Массовая доля углерода в метане СН4 составляет, (%)….
16. 11 г соли растворили в 99 г воды. Массовая доля соли в полученном растворе составляет…
