
- •Текст лекций по курсу: «Металлургия редких металлов»
- •2. Металлургия лития, рубудия и цезия
- •2.1 История открытия лития, рубидия и цезия
- •2.2 Химические свойства лития, рубидия и цезия, а также их важнейших химических соединений
- •2.3 Применение лития, рубидия, цезия, и их соединений
- •2.4 Сырьевые источники лития, рубидия и цезия
- •2.5 Методы обогащения сырья лития, рубидия и цезия
- •2.6 Технология получения первичных соединений лития
- •2.6.1 Переработка сподумена
- •2.6.2 Переработка лепидолита
- •2.6.3 Переработка рассолов
- •2.7 Технология получения первичных соединений рубидия и цезия
- •2.7.1 Переработка поллуцита
- •2.7.2 Переработка лепидолита
- •2.7.3 Переработка карналлита
- •2.7.4 Получение рубидия и цезия из рассолов
- •2.8 Технология получения металлических лития, рубидия и цезия
- •2.8.1 Получение металлического лития
- •2.8.2 Получение металлических рубидия и цезия
- •2.9 Литература по металлургии лития, рубидия и цезия
2.6 Технология получения первичных соединений лития
В связи с низким содержанием лития в минералах, а тем более в их концентратах, современные методы переработки литиевого сырья типично гидрометаллургические. В гидрометаллургической переработке можно выделить два основных технологических этапа: 1) разложения сырья, в результате которого литий переводится в водорастворимое или летучее соединение, и 2) концентрирование лития химическими методами и отделение его от сопутствующих примесей. Определяющей стадией технологической схемы является разложение концентрата. По типу используемых для этой цели реагентов все способы переработки литиевых концентратов можно разделить на кислотные, щелочные, щелочно-солевые и способы, основанные на взаимодействии со средними солями.
Кислотные методы. Наибольшее значение для переработки литиевых концентратов имеет серная кислота. Она позволяет проводить разложение минералов при относительно высокой температуре, когда ее действие наиболее эффективно. Использование фтористоводородной кислоты связано с большими техническими (аппаратурными) трудностями и, кроме того, экономически нецелесообразно. Применение сильнолетучих кислот не дает положительных результатов, так как минералы лития (в основном силикаты и алюмосиликаты) требуют для разложения достаточно высокой температуры.
Щелочные методы. В щелочных методах переработки литийсодер-жащих концентратов используют оксиды и гидроксиды металлов, а также карбонаты щелочных и щелочноземельных металлов. В результате разложения минералов выделяется оксид лития, который в дальнейшем обычно извлекается в виде гидроксида.
Щелочно-солевые методы. Эта группа методов предусматривает использование смеси оксидов (карбонатов) или гидроксидов и средних солей; анион последних определяет природу образующегося при разложении соединения лития. Из возможных компонентов таких смесей практическое значение имеют соли и оксид кальция. При этом обычно используют известково-сульфатные и известково-хлоридные смеси.
2.6.1 Переработка сподумена
Для разложения концентрата сподумена возможно использование всех перечисленных выше методов разложения литиевых минералов. Наиболее распространенными среди них являются сернокислотный и щелочной методы переработки.
Сернокислотный метод переработки сподумена. Сернокислотный метод переработки предполагает использование модификации минерала, которая химически значительно более активна. Это определяется тем, что силикатная структура сподумена переходит в алюмосиликатную
(Li, Na)Al[Si2О6] → Li(Na)[AlSi2О6].
Образующийся β-сподумен обрабатывают небольшим избытком серной кислоты при 250°С. Подробное исследование реакции сульфатизации β‑cподумена позволило установить схему взаимодействия последнего с серной кислотой^
Li[AlSi2О6] + H2SО4 → Li2SO4 + Н[AlSi2О6].
При сульфатизации происходит ионный обмен между алюмосиликатным ядром β‑сподумена и серной кислотой, в результате которого литий в сподумене замещается водородом, причем структура минерала практически не нарушается. Принципиальная технологическая схема сернокислотного способа представлена на рисунке 2.7.
Исходным сырьем служит концентрат сподумена с содержанием 3–5 % Li2O. Перед сульфатизацией концентрат подвергают обжигу в трубчатой печи. При 1100 °С за 10–20 мин степень перехода в β–сподумен составляет 99–100 %. Из печи материал поступает в холодильник, где охлаждается до 95–120°С, а затем на измельчение до 0,074 мм.

'Рисунок 2.7 — Принципиальная технологическая схема переработки сподумена сернокислотным способом.
Измельченный спек смешивается с 93 %-ной серной кислотой, взятой с 35–40% избытком по отношению к теоретическому. Температура сульфатизации 250°С. Затем реакционную массу выщелачивают водой в реакторе при непрерывном перемешивании; там же производится нейтрализация избытка серной кислоты карбонатом кальция до рН 6,0–6,5. Нейтрализованная масса поступает на фильтр, на котором нерастворимый остаток промывают водой, а промывные воды используются для выщелачивания новой порции спека. Затем остаток выводят из процесса как отвальный продукт, потери лития с ним не превышают 1 %.
Раствор после выщелачивания содержит около 100 г/л сульфата лития и примеси (Mg, Са, Al, Fe), которые до выделения лития должны быть удалены. Вначале раствор очищают от магния, который обычно сопутствует литию в руде. Для выделения магния в виде гидроксида раствор нейтрализуют известью до рН 12–14. Затем осаждают кальций в виде СаСОз при обработке раствора кальцинированной содой.
После удаления осадков Mg(OH)2 и СаСОз фильтрованием раствор остается загрязненным алюминием (из рудного сырья) и железом (в результате коррозии стальных трубопроводов). Поэтому при последующем упаривании в выпарной аппарат подается серная кислота до рН 7 для осаждения гидроксидов железа и алюминия.
Упаривание раствора проводят до, содержания сульфата лития ~200 г/л. После упаривания в раствор, добавляется некоторое количество газовой сажи (с целью обесцвечивания раствора), которая удаляется вместе с осадком гидроксидов. Концентрированный раствор перекачивают в реактор, в котором литий осаждается в виде карбоната насыщенным раствором кальцинирован ной соды при 90°С. Карбонат лития осаждается в виде мелких белых легкофильтрующихся кристаллов. После отделения маточного раствора кристаллы промывают деионизированной водой; две промывки дают 96—97 %-ный карбонат лития. Для получения сухого технического продукта влажный карбонат подвергается вакуумной сушке (70—85 кПа).
При переработке концентратов, содержащих 4–5 % Li2O, извлечение лития 85–90 %; выход лития в карбонат из руды 50–55 %.
Щелочной способ переработки сподумена. В основу способа положено спекание литиевых минералов с известью или известняком (принципиального различия в химизме взаимодействия СаО и СаСОз со сподуменом нет, так как при высоких температурах СаСОз диссоциирует с образованием СаО, с последующим выщелачиванием спека водой. По аналогии с хорошо изученным взаимодействием алюмосиликата натрия с оксидом кальция процесс можно представить следующим уравнением:
Li[AlSi2О6] + 4CaO → LiAlO2 +2Ca2SiO4.
Таким образом, при спекании образуется не свободный оксид лития, а малорастворимый алюминат. Для перевода алюмината лития в раствор необходим избыток оксида кальция в шихте, который при обработке водой образует Са(ОН)2, последний же взаимодействует с алюминатом лития^
2LiAlO2 + Са(ОН)2 → 2LiOH + СаАl2O4
В сподумене в качестве примесей содержатся алюмосиликаты натрия и калия, которые при спекании дают соответствующие алюминаты, а при обработке известью — гидроксиды натрия и калия и алюминат кальция. Выделение гидроксида лития из такого раствора происходит в процессе упаривания, при этом вначале выделяется моногидрат гидроксида лития, имеющий наименьшую растворимость. Известковая схема переработки сподумена представлена на рисунке 2.8.
Исходным сырьем служат богатые сподуменовые концентраты, содержащие 5–6 % оксида лития. Для спекания применяется известняк с минимальным количеством кремния. Перед шихтованием концентрат и известняк (соотношение 1:3) измельчаются до минус 0,25 мм в шаровой мельнице, а затем они совместно доизмельчаются при шихтовании до 0,074 мм. Спекание проводится в трубчатых вращающихся печах при 1150—1200 °С, причем необходим жесткий контроль за температурой.
Выходящий из печи спек охлаждается водой или оборотными растворами; при этом происходит его частичное выщелачивание. Затем спек измельчают до 0,147 мм и выщелачивают в три стадии (противоток) при Т : Ж = 1 : 3 и температуре 90°С. Остаток от выщелачивания (шлам) отфильтровывается и поступает на многократную промывку по принципу противотока. Содержание оксида лития в отвальном шламе не превышает 0,10—0,15 %.
Раствор выщелачивания (10 г/л Li2O) направляется на вакуумное упаривание, которое проводится в две стадии. На первой стадии раствор упаривается до уменьшения объема в 8–10 раз. При этом выпадает осадок кальциевых соединений и карбоната лития, который отфильтровывают и направляют на выщелачивание. Затем раствор упаривается до 1,17—1,20 г/см3 и охлаждается до 40–50°С; при этом выделяется моногидрат гидроксида лития. Кристаллы гидроксида отделяют центрифугированием и промывают. Для получения более чистого продукта его очищают перекристаллизацией. Для этого кристаллы растворяют в дистиллированной воде при нагревании до содержания оксида лития - 160 г/л. Горячий раствор фильтруют и кристаллизуют моногидрат гидроксида лития при 40°С. Маточный раствор используют для растворения новой порции кристаллов. Извлечение лития — около 70 %; с учетом потерь при обогащении — не более 50 %.
Известковая схема обладает рядом несомненных достоинств. Это, прежде всего, возможность прямого получения гидроксида лития, так как никакая другая схема такой возможности не дает. Другие достоинства — универсальность, доступность и дешевизна применяемых реагентов.
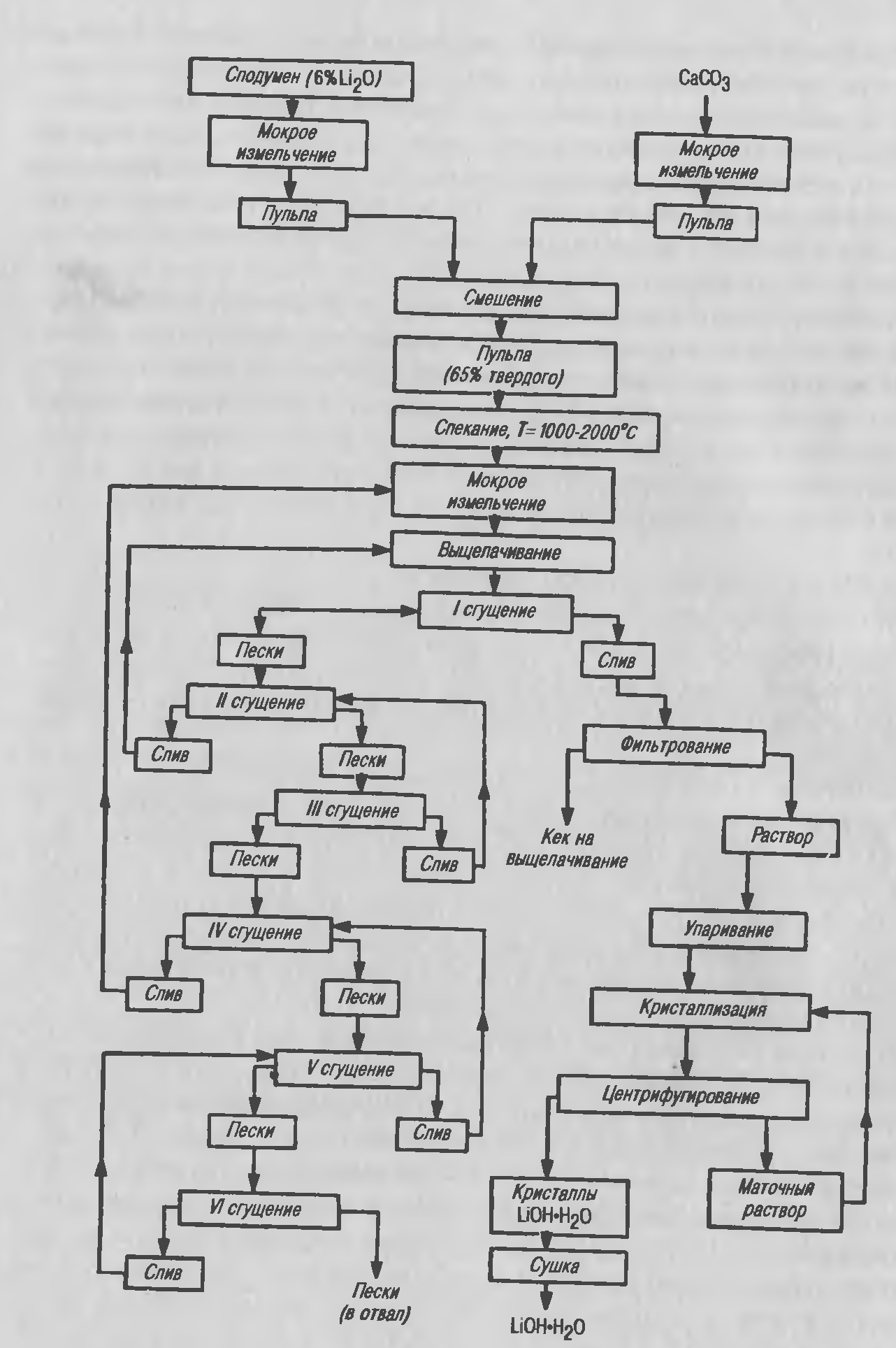
'Рисунок 2.8 — Принципиальная технологическая схема переработки сподумена щелочным способом.
