
- •I.6.2.2.Реакции присоединения к ароматическому ядру.
- •I.6.2.3. Реакции боковых цепей, связанных с ароматическими ядрами.
- •I.6.2.4. Реакции окисления и восстановления.
- •Глава II. Галогенпроизводные углеводородов
- •II.1. Способы получения галогенопроизводных.
- •Физические свойства
- •Химические свойства
- •II.2. Химические свойства галогенпроизводных со связью с(sp3)-Hal
- •II.2.1. Реакции нуклеофильного замещения
- •1. Мономолекулярное нуклеофильное замещение
- •2. Бимолекулярное нуклеофильное замещение
- •II.2.2. Реакции -элиминирования (дегидрогалогенирования)
- •II.2.3. Реакции -элиминирования (образование карбенов).
- •II.3. Химические свойства галогенпроизводных со связью с(sр2)-Hal
- •II.3.1. Галогеналкены
- •II.3.2. Галогенарены
- •II.4. Практическое использование галогенпроизводных
II.2.3. Реакции -элиминирования (образование карбенов).
 Реакции
-элиминирования
протекают для некоторых полигалогенпроизводных.
Наиболее типичный пример – реакция,
протекающая при действии сильных
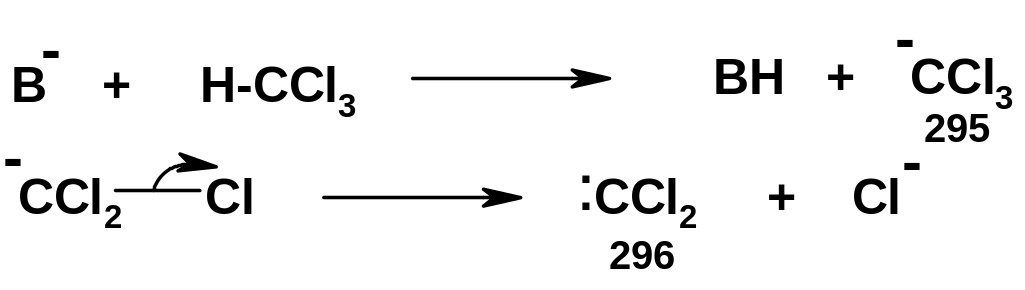
оснований на хлороформ:
Реакции
-элиминирования
протекают для некоторых полигалогенпроизводных.
Наиболее типичный пример – реакция,
протекающая при действии сильных
оснований на хлороформ:
Сильное основание (щелочь или трет-бутилат калия) отрывает протон от хлороформа с образованием карбаниона (295) (сопряженное основание хлороформа); на второй стадии карбанион (295) отщепляет хлорид-анион с образованием дихлоркарбена (296). Механизм этой реакции аналогичен ранее рассмотренному механизму Е1сВ с той разницей, что обе группы (Н и Сl) отщепляются от одного атома углерода; поэтому иногда его обозначают индексом 1,1Е1сВ.
Дихлоркарбен относится к высокореакционноспособным активным частицам – карбенам; их общая формула :СX2 или :СХY, где Х,Y = Н, Alk, Ar, Hal, CN и др.). Карбенный атом углерода образует две ковалентные связи и имеет два несвязывающих электрона; таким образом, вокруг атома углерода находится шесть электронов, что и приводит к малой устойчивости и чрезвычайно большой реакционной способности карбенов.
 Два
несвязывающих электрона в карбенах
могут быть спаренными или неспаренными.
В первом случае карбены называют
синглетными,
во втором – триплетными:
Два
несвязывающих электрона в карбенах
могут быть спаренными или неспаренными.
В первом случае карбены называют
синглетными,
во втором – триплетными:
Синглетный Триплетный
В синглетном карбене оба несвязывающих электрона находятся на одной несвязывающей орбитали; такой карбен является электрофильной частицей. В триплетном карбене два несвязывающих электрона находятся на двух взаимно перпендикулярных несвязывающих орбиталях; такой карбен проявляет свойства бирадикала (его можно изобразить в виде •СХ2•). Триплетное состояние энергетически более выгодно, чем синглетное; однако во многих вариантах получения карбенов они в момент возникновения имеют синглетное состояние (в частности, и приведенный выше дихлоркарбен); далее они могут перейти в триплетное состояние, если успеют это сделать до вступления в реакцию с другой молекулой.
Карбены, особенно синглетные, чрезвычайно реакционноспособны; они вступают в разнообразные реакции, в частности, в реакции присоединения. Из них наиболее известно присоединение карбенов к алкенам с образованием производных циклопропана:
Е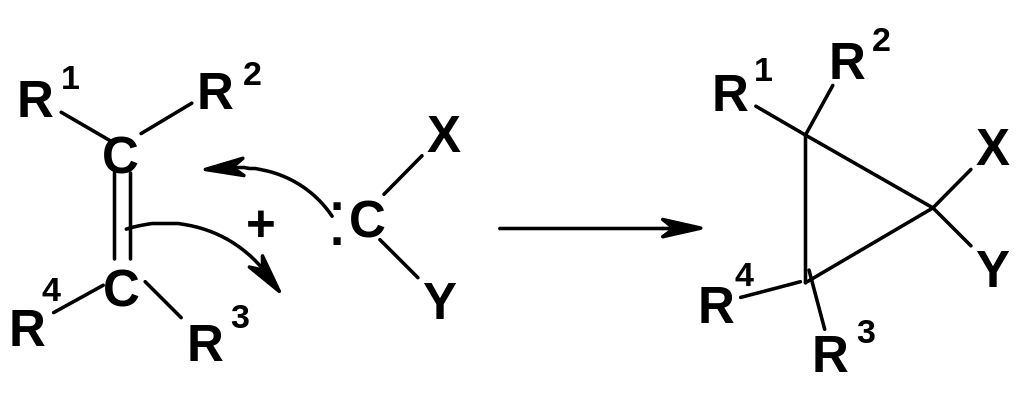 сли
карбен реагирует в синглетном
состоянии,
присоединение идет стереоселективно,
сли
карбен реагирует в синглетном
состоянии,
присоединение идет стереоселективно,
т.е. образуется один стереоизомер производного циклопропана; если в триплетном – то нестереоселективно: образуются два стереоизомера.
Присоединение карбенов к алкенам – один из важнейших способов синтеза производных циклопропана.
Реакции -элиминирования – один из наиболее распространенных способов генерации карбенов, но отнюдь не единственный. В дальнейшем будет рассмотрен еще один способ – из алифатических диазосоединений.
Известен ряд аналогов карбенов, где подобная электронная структура имеется не у атома углерода, а у атома другого элемента; в частности, достаточно часто встречаются нитрены, имеющие вид R-Ň:, - с одноковалентным атомом азота, обладающим двумя неподеленными парами электронов.
 Выше были
рассмотрены реакции галогенпроизводных,
относящиеся к нуклеофильному замещению
и элиминированию. Большое значение
имеют также реакции галогенпроизводных
с металлами; они будет рассмотрены в
разделе «Металлорганические соединения».
Выше были
рассмотрены реакции галогенпроизводных,
относящиеся к нуклеофильному замещению
и элиминированию. Большое значение
имеют также реакции галогенпроизводных
с металлами; они будет рассмотрены в
разделе «Металлорганические соединения».
