
- •8. Важнейшие методы исследования органических соединений
- •Глава I. Углеводороды
- •I.1Ациклические предельные углеводороды (алканы)
- •I.1.1. Основные источники алканов и методы их получения
- •Гораздо большие возможности предоставляет взаимодействие галогенпроизводных с металлорганическими соединениями – диалкиллитийкупратами:
- •I.1.2. Электронное и пространственное строение алканов
- •I.1.3. Свойства алканов
- •I.2. Циклические насыщенные углеводороды (циклоалканы)
- •I.2.1. Классификация, номенклатура, стереоизомерия.
- •I.2.2. Источники циклоалканов и способы их получения
- •I.2.3. Электронное и пространственное строение циклоалканов.
- •I.2.4. Свойства циклоалканов
8. Важнейшие методы исследования органических соединений
Первоначально органические соединения выделяли из природных объектов, в основном растительного происхождения; и сейчас природные объекты (растения, животные, микроорганизмы) являются важнейшими их источниками – из них выделяют достаточно большое количество соединений, обладающих, как правило, высокой биологической активностью. Наибольшее же количество органических соединений получают в результате органического синтеза. Исходными веществами для органического синтеза являются продукты переработки нефти, природного газа, каменного угля.
При экспериментальном исследовании органических соединений обычно приходится решать следующие задачи:
Выделение, разделение и очистка органических соединений (из природных источников или из реакционных смесей).
Контроль за ходом реакций.
Установление строения и идентификация органических соединений (выделенных из природных источников или вновь синтезированных).
Среди важнейших экспериментальных методов органической химии – различные варианты перегонки и кристаллизации; иногда используется возгонка. Особо стоит выделить хроматографические методы; их разнообразные варианты позволяют решать весьма широкий круг задач, включая качественный и количественный анализ смесей веществ, качественный и количественный контроль за ходом реакций, препаративное разделение сложных смесей соединений, а также идентификацию. В биоорганической химии, особенно при исследовании биополимеров, весьма эффективно использование электрофореза; именно этот метод сделал возможными современные успехи в расшифровке первичной структуры белков и особенно ДНК. Описание упомянутых выше методов содержится в разнообразных руководствах.
Исключительно важной задачей является установление строения органических соединений, учитывая, что большинство из них построены достаточно сложно. Для установления строения используется большой набор методов –как химических, так и физических.
Ранее (примерно до 40-х годов 20 века) использовались почти исключительно химические методы.
А. Простейшим химическим методом является элементный анализ – определение процентного содержания элементов, входящих в состав соединения.
Б. Проведение качественных реакций на различные фрагменты органических молекул (прежде всего на функциональные группы). Существуют достаточно надёжные качественные реакции на большинство функциональных групп, позволяющие быстро протестировать соединение на их наличие.
В. Проведение химических реакций, позволяющих из неизвестного соединения получить известное (или известные), т.е. «свести неизвестное к известному». Среди таких реакций наиболее часто используются окислительные и гидролитические; в качестве «школьного» примера можно привести установление строения жиров (триглицеридов), при гидролизе которых образуются глицерин и известные жирные кислоты. Используется и обратный приём – встречный синтез – синтез неизвестного вещества из известных.
В качестве более развернутой иллюстрации использования химических методов рассмотрим установление строение некоего неизвестного соединения Х. По данным элементного анализа и определения молекулярной массы для него вычислена брутто-формула С9Н10О. Такой состав указывает на значительную формальную ненасыщенность, однако качественная реакция на двойные связи (реакция с бромной водой) дает отрицательный результат; это означает, что соединение содержит бензольное ядро (как известно, в большинстве случаев не реагирующее с бромной водой). Другие качественные реакции показывают: а. В соединении имеется кетонная группа, потому что соединение дает положительную реакцию на карбонильную группу с 2,4-ди6нитрофенилгидразином:
н о
не дает реакцию серебряного зеркала на
альдегидную группу.
о
не дает реакцию серебряного зеркала на
альдегидную группу.
б. Соединение дает качественную реакцию на метилкетоны, т.е. на фрагмент СН3СО (так называемую «иодоформную реакцию» – образование иодоформа при действии иода и щелочи).
 Исходя
из состава и результатов качественных
реакций, можно сделать вывод, что
соединение Х включает бензольное ядро,
содержащее две боковые цепи: СН3СО
и СН3.
Остается выяснить вопрос о взаимном
расположении этих двух цепей. Задача
решается путем окисления соединения Х
сильными окислителями; известно, что
при этом многие боковые цепи окисляются
до карбоксильных групп. В данном случае
образуется известная
изофталевая кислота; это указывает на
мета-положение боковых цепей, т.е.
позволяет установить окончательную
формулу соединения Х как 1-ацетил-3-метилбензола
(мета-метилацетофенона)
(70).
Исходя
из состава и результатов качественных
реакций, можно сделать вывод, что
соединение Х включает бензольное ядро,
содержащее две боковые цепи: СН3СО
и СН3.
Остается выяснить вопрос о взаимном
расположении этих двух цепей. Задача
решается путем окисления соединения Х
сильными окислителями; известно, что
при этом многие боковые цепи окисляются
до карбоксильных групп. В данном случае
образуется известная
изофталевая кислота; это указывает на
мета-положение боковых цепей, т.е.
позволяет установить окончательную
формулу соединения Х как 1-ацетил-3-метилбензола
(мета-метилацетофенона)
(70).
Разумеется, здесь приведен простой пример; тем не менее, используя подобные методы, удавалось установить строение достаточно сложно построенных соединений; можно вспомнить, например, установление структур бициклических терпенов и продуктов их превращений, проведенное еще в 90-е годы 19-го столетия. Тем не менее, химические методы приводят к успеху не во всех случаях, особенно при расшифровке сложных структур; к тому же для их использования требуется иметь достаточно большое количество исследуемого соединения (даже при использовании полумикро- и микрометодов); исследователь же далеко не всегда имеет требуемое количество вещества.
Ближе к середине 20-го века начали интенсивно развиваться физические методы установления строения; использование этих методов позволило достичь огромного прогресса: удается расшифровать весьма сложные структуры, причем для этого во многих случаях достаточно иметь лишь несколько миллиграммов (а иногда и доли миллиграмма) вещества.
Ниже будут весьма кратко изложены самые общие сведения о наиболее распространенных физических методах установления строения. Физические основы этих методов и достаточно подробная информация об их использовании являются содержанием соответствующего общего курса.
К наиболее широко используемым физическим методам относятся: 1.Электронная спектроскопия; 2. Инфракрасная спектроскопия; 3. Спектроскопия ядерного магнитного резонанса; 4. Масс-спектрометрия; 5. Рентгеноструктурный анализ.
Первые три метода относятся к абсорбционной спектроскопии: они исследуют поглощение электромагнитного излучения при его взаимодействии с веществом. Поглощение происходит тогда, когда частота излучения совпадает с частотой какого-либо волнового процесса в исследуемом соединении; поскольку частоты этих волновых процессов зависят от строения соединения, то изучение поглощения дает информацию, часто весьма тонкую, о строении изучаемого вещества.
Электронная спектроскопия исследует поглощение веществом излучения в ультрафиолетовой и видимой областях (UV-vis, 200 – 1000 нм). Поглощение излучения происходит при переходе валентных электронов со связывающих орбиталей на разрыхляющие; при этом, чем легче происходит переход, тем больше длина волны поглощаемого излучения. Наиболее характерные полосы поглощения связаны с переходами -электронов*) и р-электронов (р р*); для сопряженных структур с легко поляризуемыми - и р-электронными системами поглощаются более длинные волны, интенсивность поглощения возрастает. Для исследования поглощения используются приборы – спектрометры UV-vis (УФ-спектрометры). Поглощение проявляется обычно в виде небольшого числа довольно широких полос; отмечаются длины волн, соответствующие максимумам этих полос (рис.1.)



 ,
нм
,
нм
240 400

Рис.1. Электронный спектр азобензола С6Н5-N=N-C6H5 (- величина, характеризующая интенсивность поглощения).
Электронные спектры используются для обнаружения ненасыщенных и, особенно, сопряженных фрагментов органических молекул. Они позволяют определить степень и характер сопряжения; на рис.1 интенсивная полоса около 320 нм относится к связи N=N, сопряженной с двумя бензольными ядрами.
Инфракрасная спектроскопия (ИК спектроскопия) исследует поглощение излучения в инфракрасной области спектра ( 2500- 25000 нм); обычно фиксируется не длина волны, а частота поглощения, выраженная в обратных сантиметрах; указанному выше интервалу длин волн соответствует диапазон частот 4000-400 см-1). При поглощении инфракрасного излучения происходят изменения колебательных уровней атомов, образующих ту или иную связь; происходит переход с более низкого уровня на более высокий. Для каждого типа связи (как простой, так и кратной) имеются собственные колебательные уровни и значит свои специфические полосы поглощения; для целого ряда связей полосы весьма характеристичны и позволяют легко обнаружить эти связи. В частности, легко обнаруживаются связи О-Н (гидроксильные группы, N-Н (аминогруппы), С=О (карбонильные группы), СN (нитрильная группа) и ряд других. При этом частота поглощения связи часто зависит от ее окружения; например, различаются частоты поглощения группы С=О в кетонах, сложных эфирах, амидах и ангидридах кислот. Для изучения используют приборы – ИК-спектрометры; поглощение инфракрасного излучения проявляется в виде достаточно большого количества довольно узких полос (рис.2):
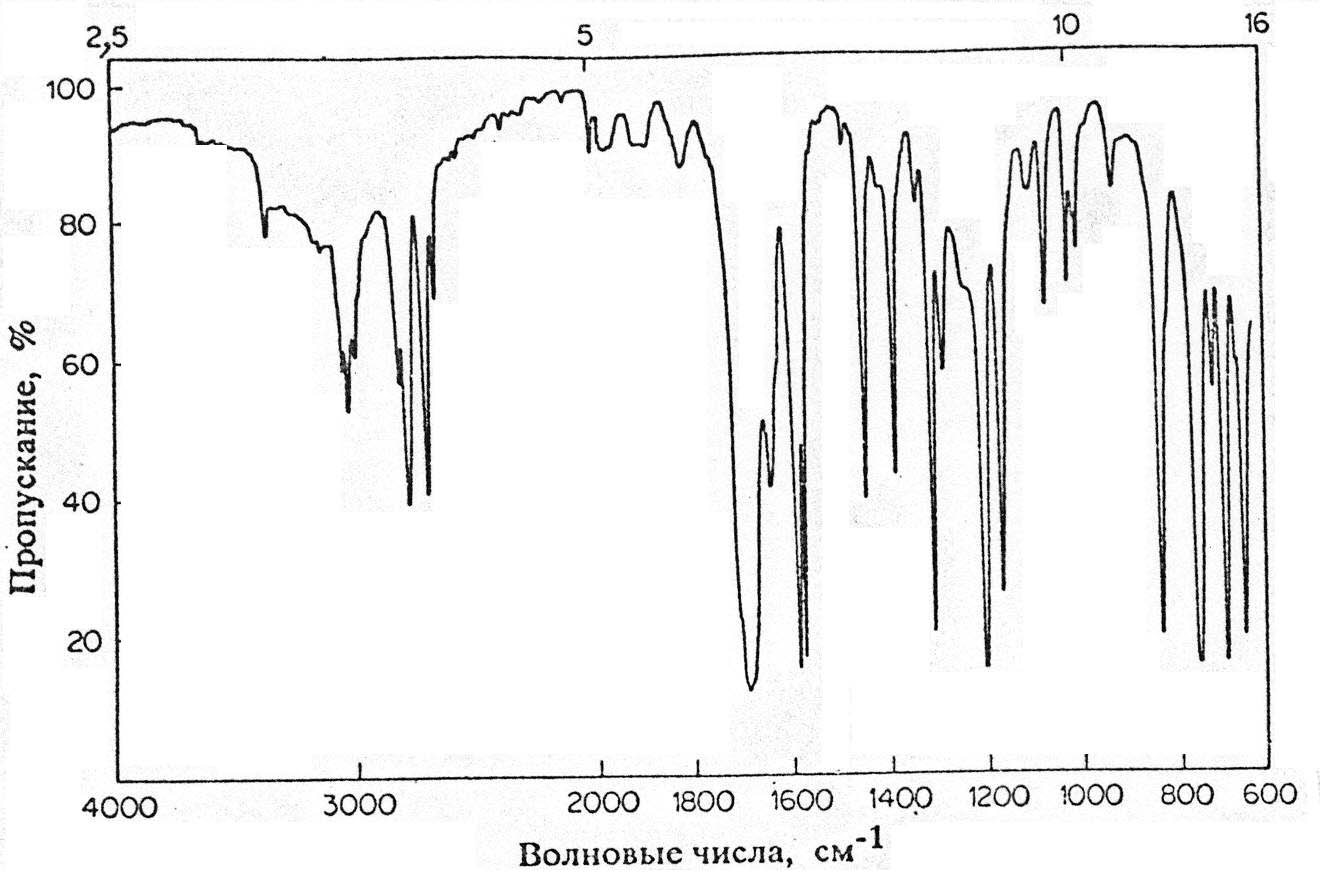
Рис.2. Инфракрасный спектр бензальдегида С6Н5СНО.
Таким образом, ИК спектроскопия позволяет обнаруживать различные типы химических связей, в частности, обнаруживать различные функциональные группы. Например, в спектре, приведенном на рис.2., легко обнаруживаются ароматическая структура (две полосы поглощения около 1500 и1600 см-1) и группа С=О (полоса поглощения при 1690 см-1); сходные полосы имеются в спектре приведенного выше соединения (66).
ИК спектроскопия – один из наиболее эффективных методов идентификации органических соединений. Картина поглощения инфракрасного излучения (ИК спектр) содержит множество полос и является специфичной для каждого индивидуального соединения подобно отпечаткам пальцев для каждого человека. Поэтому, если ИК спектр исследуемого соединения идентичен спектру известного соединения, можно уверенно считать, что и сами эти соединения идентичны.
Спектроскопия ядерного магнитного резонанса (спектроскопия ЯМР) исследует поглощение веществом излучения в радиочастотном диапазоне. Это поглощение соответствует переходу атомных ядер с одного магнитного энергетического уровня на другой. Поглощение наблюдается для ядер со спиновым квантовым числом, отличным от нуля; наиболее пригодны ядра с полуцелым спином. Чаще всего используется спектроскопия на ядрах 1Н (протонный магнитный резонанс, ЯМР 1Н), 13С, 15N, 19F, 31P; в органической химии преимущественно используются протонные и углеродные спектры. Соответствующие приборы, используемые для получения спектров ЯМР, – спектрометры ЯМР. Поглощение обнаруживается в виде сигналов, которые обычно четко проявляются в спектре.
Энергия переходов между разными магнитными уровнями ядер, а значит и частота поглощения весьма чувствительны к магнитному окружению ядер, прежде всего, к природе атомов, непосредственно связанных с данным атомом. В принципе, каждый атом, не эквивалентный другим, дает собственный сигнал поглощения. Во многих случаях сигналы имеют тонкую структуру, т.е. являются мультиплетными (особенно это характерно для протонных спектров); мультиплетность сигналов также зависит от окружения – от числа соседних атомов и их характера. Для протонных спектров (спектров ЯМР 1Н) интенсивность сигнала пропорциональна числу атомов, которые дают этот сигнал. Таким образом, анализируя картину поглощения, можно сделать вывод о характере атомов, входящих в состав молекулы, и о числе одинаковых (эквивалентных) атомов. При анализе спектра отмечают химический сдвиг – положение сигнала данного ядра относительно сигнала стандартного соединения (обычно тетраметилсилана), мультиплетность сигнала (дублет, триплет, квартет и т.д.), а для спектров ЯМР 1Н – также интенсивность сигнала. Простой пример спектра ПМР приведен на рис.3.
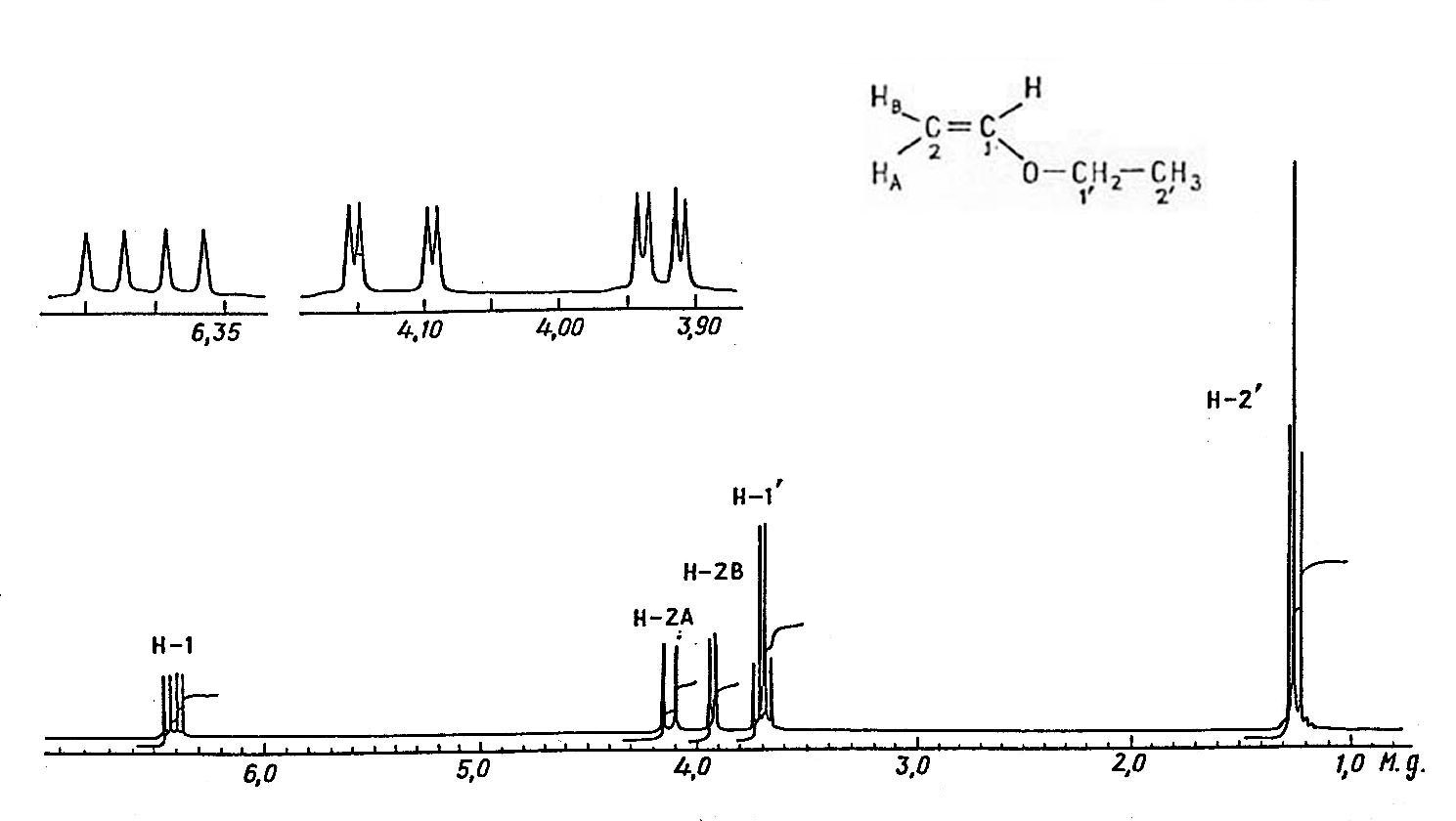
Рис.3. Спектр ЯМР 1Н (спектр ПМР) винилэтилового эфира СН2=СН-О-С2Н5; – химический сдвиг (выражен в м.д. - миллионных долях рабочей частоты прибора); J – константы спин-спинового взаимодействия.
Из представленного рисунка видно, что каждый протон приведенного соединения дает свой собственный специфический сигнал (в верхней части рисунка представлены три сигнала в укрупненном масштабе, что позволяет количественно оценить специфическую мультиплетность каждого из них).
Спектроскопия ЯМР является одним из наиболее информативных методов установления строения. Здесь во многих случаях удается получить информацию о большинстве атомов, входящих в состав молекулы, а в целом ряде случаев – о всех атомах. В частности, для приведенного выше соединения (66) протоны двух групп СН3 и четыре ароматических протона дают свои легко интерпретируемые сигналы в спектре ЯМР 1Н, атом углерода карбонильной группы легко обнаруживается в спектре ЯМР 13С, т.е. сразу определяется строение. Спектры ЯМР, в особенности протонные спектры, содержат информацию также и о стереохимических особенностях молекул, позволяют во многих случаях определить конфигурации и конформации молекул.
Масс-спектрометрия построена на иных принципах, нежели три предыдущих метода: она изучает не поглощение электромагнитного излучения веществом, а ионизацию соединения. Ионизация может быть достигнута разными путями: путем электронного удара, химической ионизации, бомбардировки ускоренными атомами и др. Самый традиционный и до сих пор широко используемый метод - ионизация путем электронного удара – воздействия на вещество пучка электронов, ускоренных в электрическом поле. При ионизации вначале образуется молекулярный ион – заряженная частица, имеющая ту же массу, что и исходная молекула. Далее молекулярный ион обычно подвергается фрагментации, т.е. распадается с образованием ионов меньшей массы – осколочных ионов. Для получения масс-спектров используются масс-спектрометры. Как молекулярный, так и осколочные ионы фиксируются специальным регистрирующим устройством; при этом определяются массы ионов (точнее отношение их массы к заряду, m/z); результаты регистрации отражаются в виде набора пиков, каждый из которых отвечает какому-либо иону; измеряется также интенсивность этих пиков. Типичный вид масс-спектра представлен на рис.4.
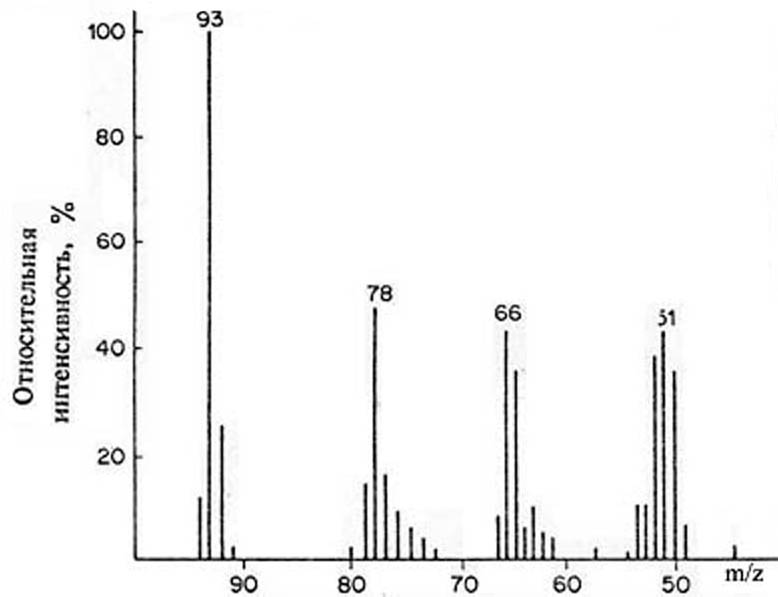
Рис.4. Графическое представление масс-спектра; 93- масса молекулярного иона, 78, 66, 61 – массы осколочных ионов.
Масс-спектрометрия позволяет: А. Точно определить молекулярную массу соединения (она, естественно, равна массе молекулярного иона). Появившиеся сравнительно недавно масс-спектрометры высокого разрешения позволяют определять молекулярную массу с точностью до четвертого знака после запятой; такая точность позволяет сразу определить брутто-формулу соединения, что делает излишним элементный анализ; Б. Исследуя фрагментацию, сделать выводы о строении соединения, так как фрагментация молекулярных ионов сильно зависит от строения и характеристична для различных типов органических соединений.
Масс-спектрометрический анализ часто совмещен с разделением смесей методами газо-жидкостной и высокоэффективной жидкостной хроматографии (хромато-масс-спектрометры), что позволяет исследовать смеси соединений.
Рентгеноструктурный анализ (РС-анализ) исследует рассеяние рентгеновских лучей (длины волн порядка 0,1 нм) кристаллическим образцом вещества. Соответствующие приборы называются рентгеновскими дифрактометрами. Рентгеновские лучи рассеиваются на электронных оболочках атомов; анализируя дифракционную картину, можно определить распределение электронной плотности, а, следовательно, координаты атомов; иначе говоря, итогом РС-анализа является полная формула исследуемого соединения, включая длины связей, величины валентных углов и пространственную структуру, т.е. полная информация о строении соединения.
Метод пока является значительно более трудоёмким, чем ранее упомянутые; кроме того, для получения качественной дифракционной картины необходимы правильные кристаллы соединения; получение таких кристаллов не всегда является простым делом. Тем не менее, рентгеноструктурный анализ все шире используется; особо ценным является его применение для определения пространственной организации биополимеров, прежде всего белков.
Было бы ошибочным думать, что сейчас для установления строения органических соединений применяются почти исключительно физические методы, а химические методы представляют лишь исторический интерес. Действительно, физические методы используются практически всегда и в ряде случаев играют главную роль; однако во многих случаях наилучшие результаты дает сочетание физических и химических методов, дополняющих друг друга.
Далее будут систематически рассмотрены наиболее важные классы органических соединений; основное внимание будет уделено их химической специфике. Вначале будут рассмотрены углеводороды, далее – их функциональные производные.
