
- •Оглавление
- •Практическая работа № 4 «Изучение способов обработки металлов давлением»
- •Процессы обработки давлением
- •Свободная ковка металлов
- •1. Электрическая дуговая сварка.
- •1.1 Ручная дуговая сварка плавящимися толстопокрытыми электродами.
- •1.2 Ручная дуговая сварка угольным электродом дугой прямого действия.
- •1.3 Ручная дуговая сварка угольными электродами дугой косвенного действия.
- •1.4. Автоматическая и полуавтоматическая сварка под флюсом
- •1.6 Плазменная сварка.
- •1.7 Сварка в углекислом газе.
- •2. Электрошлаковая сварка.
- •3. Электроннолучевая сварка.
- •4. Лазерная сварка.
- •5. Газовая (газо-кислородная) сварка.
- •6. Термитная сварка.
- •7. Холодная сварка пластичных металлов.
- •8. Электрическая контактная сварка.
- •9. Ультразвуковая сварка.
- •10. Кузнечно-горновая сварка.
- •11. Газопрессовая сварка.
- •12. Диффузионная сварка в вакууме.
- •13. Сварка трением.
- •14. Сварка взрывом.
- •15. Индукционная высокочастотная сварка.
- •1. Сварка низкоуглеродистых сталей.
- •2. Сварка углеродистых сталей.
- •3. Сварка легированных сталей.
- •3.1 Низколегированные стали.
- •3.2. Среднелегированные стали.
- •3.3 Высоколегированные стали.
- •3.4 Хромистые стали.
- •3.5 Высокомарганцовистые стали.
- •3.6 Инструментальные стали
- •1. Сварка алюминия и его сплавов.
- •1. Подготовка под сварку.
- •2. Ручная дуговая сварка.
- •3. Автоматическая сварка.
- •4. Аргонодуговая сварка.
- •5. Газовая сварка.
- •6. Термическая обработка.
- •1.Сварка меди.
- •1.1. Дуговая сварка.
- •1.2. Сварка в среде защитных газов.
- •3.2. Газовая сварка.
- •3.3. Термическая обработка.
- •1. Сварка титана.
- •2. Аргонодуговая сварка.
- •2.1 Автоматическая сварка под флюсом.
- •2.2. Термическая обработка.
- •3. Сварка никеля.
- •1. Свойства чугуна.
- •2. Способы сварки чугуна.
- •1. Холодная сварка.
- •2. Полугорячая сварка.
- •3. Горячая сварка.
- •1. Требования к сварным соединениям.
- •2. Классификация сварных соединений.
- •1.1 Классификация строительных материалов и изделий
- •1.2. Физические свойства
- •1.3. Механические свойства
- •1.4. Химические свойства
- •1.5. Надежность
- •1.6. Технологические свойства
- •2.1. Композиционные материалы с алюминиевой матрицей
- •2.2. Композиционные материалы с никелевой матрицей
- •3. Композиционные материалы с одномерными наполнителями
- •3.1. Упрочнение волокнами
- •3.2. Армирующие материалы и их свойства
- •3.3. Получение композиционных материалов на металлической основе, армированных волокнами
- •3.4. Композиционные материалы с алюминиевой матрицей
- •3.5. Композиционные материалы на никелевой матрице
- •4. Эвтектические композиционные материалы
- •4.1. Эвтектические композиционные материалы на алюминиевой основе
- •4.2. Эвтектические композиционные материалы на основе никеля
- •5. Композиционные материалы на неметаллической основе
- •5.1. Свойства композиционных материалов с полимерной матрицей
- •5.2. Обработка и соединение композиционных материалов
- •1. Полимеры и полимерные материалы
- •1.1 Общая характеристика и классификация
- •1.2 Пластики
- •1.3 Эластомеры
- •1.4 Волокна
- •2. Переработка полимеров
- •2.1 Компаундирование
- •2.2 Технология переработки
- •2.3 Каландрование
- •2.4 Литье
- •2.5 Прямое прессование
- •2.7 Экструзия
- •2.8 Вспенивание
- •2.9 Армирование
- •2.10 Прядение волокон
- •1. Классификация вяжущих веществ
- •2. Воздушные вяжущие вещества
- •2.1. Гипсовые и ангидритовые вяжущие вещества
- •2.2. Известь строительная воздушная
- •2.3. Магнезиальные вяжущие вещества
- •2.4. Жидкое растворимое стекло
- •3. Гидравлические вяжущие вещества
- •3.1. Гидравлическая известь
- •5.3.2. Романцемент
- •3.3. Гидравлические известесодержащие и шлакощелочные вяжущие вещества
- •3.4. Цементы на основе портландцементного и глиноземистого клинкеров
- •3.4.1. Классификация цементов
- •3.4.2. Цементы на основе портландцементного клинкера
- •5.3.4.3. Цементы на основе глиноземистого клинкера
- •5.3.5. Гипсоцементно-пуццолановое и гипсошлакоцементное вяжущее
- •5.3.6. Кислотоупорные цементы
- •Список использованной литературы
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО РЫБОЛОВСТВУ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
МУРМАНСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
А.А. Иваней
ПРАКТИКУМ
по дисциплине
«Материаловедение и технологии конструкционных материалов»
для специальностей
2701202.65 «Промышленное и гражданское строительство»;
270112.65 «Водоснабжение и водоотведение»
130403.65 «Открытые горные работы»;
130404.65 «Подземные разработки месторождений полезных ископаемых»
Мурманск
2010
Составитель |
– Иваней Александр Антонович, к.т.н., доцент кафедры технологии металлов и судоремонта Мурманского государственного технического университета.
|
Рецензент |
|
Рецензент |
|
|
|
Практикум состоит из 9 практических работ по материаловедению и технологии конструкционных материалов. Каждая работа включает теоретическое изложение материала, описание методики проведения работы и контрольные вопросы для самоподготовки.
Практикум предназначен для выполнения практических работ по дисциплине: «Материаловедение. Технология конструкционных материалов» для студентов специальности 2701202 (ПГС); 270112 (ВВ); 130403 (ОГР); 130404 (ПРМПИ)
Оглавление
|
лист |
Введение………………………………………………………………… |
4 |
Практическая работа № 1«Связь между свойствами сплава и типом диаграммы состояния»………………………………………………….... |
5 |
Практическая работа № 2«Термическая обработка сталей»……..…… |
24 |
Практическая работа № 3 «Изучение технологии литейного производства»…………………………………………………………… |
49 |
Практическая работа № 4 «Изучение способов обработки металлов давлением»……………………………………………………………… |
60 |
Практическая работа № 5 «Изучение технологии сварочного производства и пайки металлов»…………………………………..……. |
81 |
Практическая работа № 6 «Изучение способов производства строительных материалов»……………………………..……………….. |
128 |
Практическая работа № 7 «Композиционные материалы с металлической и не металлической матрицей».................................... |
146 |
Практическая работа № 8 «Изучение технологии получения полимерных пластических материалов»……...………………………… |
191 |
Практическая работа № 9 «Изучение минеральных неорганических вяжущих веществ и материалов на их основе»………………………… |
233 |
Список использованной литературы…………………………………… |
272 |
Введение
Практикум составлен в соответствии с рабочей программой курса “Материаловедение и технология конструкционных материалов” для специальностей 2701202 «Промышленное и гражданское строительство»; 270112 «Водоснабжение и водоотведение»; 130403 «Открытые горные работы»; 130404 «Подземные разработки месторождений полезных ископаемых».
Целью практикума является практическое изучение основных свойств материалов, основных технологических процессов.
В результате выполнения практических работ студент приобретает знания по методам определения основных свойств материалов и их переработке, прогрессивных технологий, умения и навыки обработки результатов эксперимента, устанавливает связь между теоретическими основами и их практическим воплощением.
В каждой работе приведены относящиеся к ней основные сведения, порядок выполнения работы, содержание отчёта, контрольные вопросы для самопроверки. В конце пособия приведен рекомендуемый библиографический список.
Практическая работа № 1
«Связь между свойствами сплава и типом диаграммы состояния»
Цель работы - ознакомиться с методикой построения диаграмм состояния двухкомпонентных сплавов, изучить изменение свойств сплавов в зависимости от изменения концентрации их компонентов для основных типов диаграмм состояния.
Задачи:
Изучить теоретические сведения о строении металлических сплавов.
Усвоить методику экспериментального построения диаграмм состояния двухкомпонентных сплавов.
Научиться практическому использованию правила фаз и правила отрезков.
Изучить связь между свойствами сплавов и типом диаграмм состояния.
Наглядные пособия и материала. Плакаты с диаграммами состояния двухкомпонентных систем, карандаши, линейки.
Краткие теоретические сведения
Строение металлических сплавов
Основными конструкционными материалами являются металлические сплавы - вещества, полученные сплавлением двух или более элементов (компонентов).
К основным понятиям в теории сплавов относятся; система, компонент, фаза.
Система - группа тел, выделяемый для наблюдения и изучения. В металловедении системами являются металлы и металлические сплавы. Чистый металл является простой (однокомпонентной) системой.
Компонентами называют вещества, образующие систему (сплав). В металлических сплавах компонентами могут быть элементы (металлы и неметаллы) и химические соединения (не диссоцирующие при нагревании).
Фазой называется однородная часть системы, отделенная от другой части системы (фазы) поверхностью раздела, при переходе через которую химический состав или структура вещества изменяется скачком,
Следовательно, однородная жидкость является однофазной системой, а механическая смесь двух видов кристаллов - двухфазной, так как каждый кристалл отличается от другого по составу или по строению и они отделены один от другого поверхностью раздела. В твердых сплавах фазами могут быть зерна чистого металла, зерна твердого раствора и зерна химического соединения. Механическая смесь двух компонентов А и В образуется тогда, когда они не способны к взаимному растворению в твердом состоянии и не вступают в химическую реакцию с образованием соединения. При этих условиях сплав будет состоять из кристаллов А и В, отчетливо выявляемых на микроструктуре. Рентгенограмма сплава покажет наличие двух решеток компонентов А и В.
Твердыми растворами называют такие твердые фазы, в которых соотношения между компонентами могут изменяться. Рентгеновский анализ обнаруживает в твердом растворе, как и у чистого металла, только один тип решетки. Следовательно, в отличие от механической смеси твердый раствор является однофазным, состоит из одного вида кристаллов, имеет одну кристаллическую решетку; в отличие от химического соединения твердый раствор существует не при определенном соотношении компонентов, а в интервале концентраций. В твердом растворе одно из входящих в состав сплава веществ сохраняет присущую ему кристаллическую решетку, a второе вещество, утратив свое кристаллическое строение, в виде отдельных, атомов распределяется в кристаллической решетке первого. Первое вещество является растворителем, второе - растворимым.
В зависимости от характера распределения атомов растворимого элемента различают твердые растворы внедрения, замещения и вычитания. Независимо от типа твердого раствора общим для них является то, что они однофазны и существуют в интервале концентраций. Для твердых растворов характерен металлический тип связи. В твердых растворах внедрения атомы растворимого элемента распределяются в кристаллической решетке металла-растворителя, занимая места между его атомами.
В твердых растворах замещения атомы растворимого элемента занимают места атомов основного металла. Посторонние атомы могут замещать атомы растворителя в любых местах, поэтому такие растворы называют неупорядоченными твердыми растворами.
Твердые растворы замещения могут быть ограниченными и неограниченными. Одно из условий неограниченной растворимости - размерный фактор: чем больше различие в атомных радиусах, тем меньше растворимость.
Неограниченная растворимость компонентов присуща системам, в которых атомные радиусы элементов различаются не более чем на 8...15%.
С понижением температуры в твердых растворах замещения может произойти перераспределение атомов, в результате которого атомы растворенного элемента займут строго определенные места в решетке растворителя. Такие твердые растворы называют упорядоченными твердыми растворами, а их структуру - сверхструктурой. Температуру перехода неупорядоченного состояния в упорядоченное называют точкой Kyрнакова.
Твердые растворы вычитания образуются на основе некоторых химических соединений, когда к химическому соединению добавляется один из входящих в его формулу элементов. Атомы этого элемента занимают нормальное положение в решетке соединения, а места, где должны были бы находиться атомы второго компонента, оказываются незаполненными, пустыми (поэтому эти растворы иногда называют растворами с дефектной решеткой).
Образование любого типа твердых растворов сопровождается изменением параметров решетки металла-растворителя. Это важный момент, определяющий изменение свойств твердого раствора.
Химическое соединение чаще всего образуется между элементами, расположенными далеко друг от друга в таблице Д.И. Менделеева, т. е. существенно различающимися по строению и свойствам, если сила взаимодействия между разнородными атомами больше, чем между атомами однородными.
Химические соединения имеют ряд особенностей, отличающих их от твёрдых растворов:
а) соотношение чисел атомов элементов, образующих соединение, строго определенное, соответствующее стехиометрической пропорции, выраженной формулой вида AnВm;
б) они имеют свою кристаллическую решетку, отличную от решеток элементов, образовавших это соединение, с правильным упорядоченным расположением атомов компонентов в кристаллической решетке;
в) свойства соединения заметно отличаются от свойств исходных элементов;
г) как и чистые металлы, они имеют постоянную температуру плавления (диссоциаций). Как правило, химические соединения обладают большой твердостью и очень хрупки.
Понятие о диаграммах состояния
Диаграмма состояния - графическое изображение состояния любого сплава изучаемой системы в зависимости от его концентрации и температуры.
Диаграмма состояния показывает равновесные, устойчивые состояния, т.е. такие, которые при данных условиях обладают минимальной свободной энергией. Они имеют большое теоретическое и практической значение, так как изучение любого сплава начинается с построения и анализа диаграммы состояния с целью изучения фаз и структурных поставляющих сплава.
С помощью диаграммы состояния можно установить возможность проведения термической обработки и ее режимы, температуры литья, горячей пластической деформации и т.д.
В любой системе число фаз, находящихся в равновесии, зависит от внутренних и внешних условий. Закономерности всех изменений, происходящих в система, подчинены общему закону равновесия, который называется правилом фаз или законом Гиббса, который выражает зависимость между числом степеней свободы С (вариантностью) системы, числом компонентов К и числом фаз системы Ф, находящихся в равновесии. Правило фаз записывают в виде: С = К - Ф + 1 (при постоянном атмосферном давлении).
Под числом степеней свободы (вариантностью) системы понимают число внешних и внутренних факторов (температура, давление и концентрация), которое можно изменять без изменения числа фаз в системе.
Построение диаграмм состояния осуществляют различными экспериментальными методами. Чаще всего используют метод термического анализа, сущность которого заключается в отборе нескольких сплавов данной системы с различным соотношением масс входящих в них компонентов. Сплавы помещают в огнеупорные тигли и нагревают в печи. После расплавления сплавов тигли со сплавами медленно охлаждают и фиксируют скорость охлаждения. По полученным данным строят кривые охлаждения в координатах время - температура.
В результате измерений получают серию кривых охлаждения, на которых при температурах фазовых превращений наблюдаются точки перегиба и температурные остановки.
Температуры, соответствующие фазовым превращениям, называются критическими точками. Точки, отвечающие началу кристаллизации, называют точками ликвидус (жидкий), а конца кристаллизации - точками солидус (твердый).
По полученным кривым охлаждения (критическим точкам) для различных сплавов изучаемой системы строят диаграмму состояния в координатах; по оси абсцисс - концентрация компонентов, по оси ординат - температура.
Рассмотрим диаграмму состояния для сплавов, образующих механические смеси из чистых компонентов (1 рода).
В этом случае оба компонента в жидком состоянии неограниченно растворимы, а в твердом состоянии нерастворимы и не образуют химических соединений. С некоторым приближением можно принять, что такими компонентами могут быть свинец - сурьма, образующие данную систему (рис. 1).
Для построения этой диаграммы выбирают три-четыре сплава различной концентрации, перенасыщенных либо свинцом, либо сурьмой, и на вспомогательной диаграмме температура – время (рис. 1 слева) наносят, пользуясь данными наблюдений температуры кристаллизации чистого свинца и чистой сурьмы, а также нижеперечисленных сплавов:
95 % Pb; 5 % Sb;
90 % Pb; 10 % Sb;
87 % Pb; 13 % Sb;
60 % Pb; 40 % Sb.
Вначале вычерчивают кривые кристаллизации Pb и Sb (1 и 6).
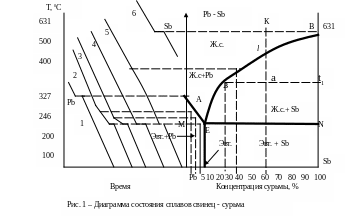
Свинец кристаллизуется при 327 0С, сурьма – при 631 0С. Их кристаллизация отмечена горизонтальным участком кривой. Первый сплав (кривая 2) начинает кристаллизоваться при 300 0С с выделением избыточных кристаллов свинца. Оставшаяся часть сплава бедна свинцом, значит, концентрация сурьмы в ней возрастает, и, когда она достигает 13 %, при 246 0С происходит окончательная кристаллизация (см. горизонтальный участок кривой). Второй сплав (кривая 3) кристаллизуется аналогично первому, но точка начала кристаллизации у него ниже, а кончается кристаллизация также при 246 0С, когда концентрация сурьмы достигает 13 %. Третий сплав (кривая 4) кристаллизуется полностью при одной температуре (246 0С) с одновременным выпадением кристаллов свинца и сурьмы. Четвертый сплав (кривая 5) начинает кристаллизоваться при 400 0С с выделением избыточных кристаллов сурьмы. В жидком сплаве сурьмы становится все меньше, и, когда ее содержание снизится до 13 %, при 246 0С произойдет окончательная кристаллизация.
Все точки начала и конца кристаллизации свинца, сурьмы и указанных четырех сплавов перенесем на основную диаграмму. Соединив все точки начала кристаллизации, получают линию АЕВ. Эта линия называется ликвидусом. Все сплавы, лежащие выше ликвидуса, находятся в жидком состоянии. Линия МЕN называется солидусом. Ниже этой линии все сплавы находятся в твердом состоянии. В интервале между ликвидусом и солидусом имеется две фазы: жидкий сплав (ж.с.) и кристаллы одного из компонентов. В области МАЕ – жидкий сплав и кристаллы свинца, а в области ЕВN – жидкий сплав и кристаллы сурьмы.
Сплав, содержащий 13 % сурьмы, кристаллизующийся при одной температуре, называется эвтектическим. Он имеет самую низкую температуру кристаллизации и отличается равномерной структурой. Сплавы, содержащие менее 13 % сурьмы, лежащие влево от эвтектики, называются доэвтектическими, а более 13 % сурьмы – заэвтектическими. Структуры эвтектического, доэвтектического и заэвтектического сплавов сильно различаются между собой. Эвтектика – структура с равномерно распределенными компонентами. В доэвтектических сплавах наряду с эвтектикой имеются кристаллы свинца, в заэвтектических – наряду с эвтектикой кристаллы сурьмы.
Различие структур определяет различие свойств сплавов. Для определения состояния сплава при любой температуре и нахождения точек кристаллизации с помощью диаграммы нужно из точки концентрации данного сплава восстановить перпендикуляр до пересечения с линиями ликвидуса и солидуса. Точки пересечения перпендикуляра укажут начало и конец кристаллизации.
Практическое применение диаграммы свинец – сурьма находят, например, при выборе подшипникового сплава. Пользуясь этой диаграммой, установили, что наиболее пригодными для подшипниковых сплавов являются заэвтектические сплавы, состоящие из мягкой эвтектики и твердых вкраплений сурьмы. Мягкая основа несколько изнашивается, а твердые кристаллы сурьмы сохраняются, и поэтому в микроуглублениях мягкой основы хорошо удерживается смазка. Наиболее подходящими сплавами для подшипников из всех заэвтектическими оказались сплавы с содержанием 15- 20 % Sb, так как температуры кристаллизации (плавления) этих сплавов (340-360 0С) соответствуют температурам, при которых происходит заливка подшипников.
Итак, по диаграмме состояния первого типа затвердевают те сплавы, компоненты которых в жидком состоянии неограниченно растворяются друг в друге, а в твердом состоянии образуют простую механическую смесь кристаллов обоих компонентов. По диаграмме состояния второго типа затвердевают сплавы, компоненты которых обладают неограниченной растворимостью как в жидком, так и в твердом состоянии.
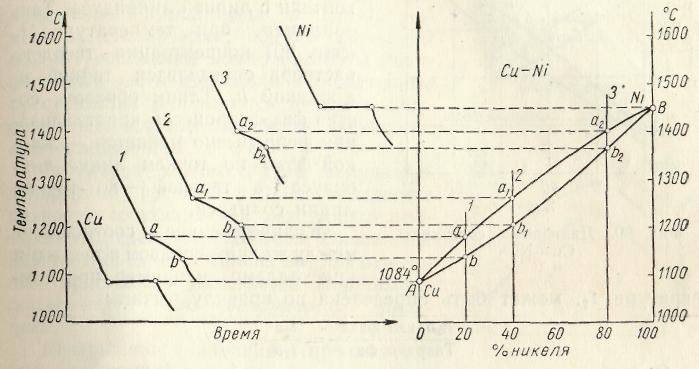
Диаграмма 2-го рода соответствует сплавам, у которых компоненты и в жидком и в твердом состоянии образуют раствор. К ним относятся сплавы медь – никель, железо – никель и др. Диаграмма состояния медь – никель приведена на рис. 2.

Кривая 1 относится к чистой меди, точка кристаллизации которой 1083 0С, а кривая 5 – к никелю, точка кристаллизации которого 1452 0С. Кривая 2 характеризует кристаллизацию 20 %-го сплава никеля (или 80 %-го сплава меди). Началу кристаллизации этого сплава соответствует точка а, когда кристаллизуется решетка меди, в которой имеется 20 % никеля. В точке b кристаллизация заканчивается.
Аналогично кристаллизуется 40 %-ный (кривая 3) и 80 %-ный (кривая 4) сплавы никеля, однако точки начала (а1 и а2) и конца (b1 и b2) кристаллизации у первого сплава ниже, чем у второго.
Перенеся все точки начала и конца кристаллизации меди и никеля и указанных выше сплавов на основную диаграмму (рис. 9 справа) и соединив эти точки, получим линии ликвидуса АаВ и линию солидуса АbВ. Выше линии АаВ сплавы меди с никелем находятся в жидком состоянии, а ниже линии АbB – в твердом. В зоне между АаВ и АbB имеются две фазы: жидкий сплав и кристаллы твердого раствора никеля в меди. Диаграмма 2-го рода отличается от диаграммы 1 –го рода тем, что здесь образуется одна кристаллическая решетка, а значит, нет и эвтектического сплава, как это наблюдается у сплавов, образующих механическую смесь. Подавляющее число металлов в жидком состоянии образует однородные жидкие растворы.
При переходе в твердое кристаллическое состояние во многих сплавах сохраняется однородность, следовательно, сохраняется взаимная растворимость. Такая однородная фаза называется твердым раствором.
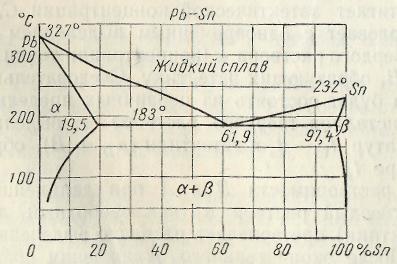
Диаграмма состояния третьего типа рассматривает случай, когда два металла обладают полной взаимной растворимостью в жидком состоянии и ограниченной растворимостью в твердом состоянии; при этом растворимость в твердом состоянии уменьшается с понижением температуры (например, свинец - олово).
На рис. 3 приведена диаграмма состояния для этого случая в общем виде. Линии АС и СВ соответствуют линии ликвидуса. По линии АС из жидкого сплава кристаллизуется твердый раствор компонента В в компоненте А (α), по линии СВ – чистый компонент В.

Линия ADCF отвечает линии солидуса. Точка D характеризует предельную растворимость В и А при эвтектической температуре tэ, а точка Е – предельную растворимость компонента В в компоненте А при нормальной комнатной температуре. Следовательно, линия DE показывает изменение растворимости В и А с понижением температуры; каждая точка линии DE указывает на предел растворимости В и А (предел насыщения) при соответствующей температуре.
В точке С одновременно из жидкой фазы кристаллизуется твердый раствор В в А (α) предельной растворимости (точка D) и компонент В с образованием эвтектики, т.е. механической смеси обеих фаз.
Рассмотрим процесс кристаллизации сплавов 1, 2, 3. Кристаллизация сплава 1 начинается при температуре t1 и заканчивается при температуре t2. После затвердевания сплав состоит только из твердого раствора α (В и А) и при дальнейшем понижении температуры никаких превращений не испытывает. Процесс кристаллизации сплава 2 начинается при температуре t3 и заканчивается при температуре t5.
Состав жидкой фазы в процессе кристаллизации меняется по линии ликвидуса, а твердой фазы по линии солидуса. Так, например, при температуре t4 состав жидкой части сплава определяется точкой а, а кристаллов твердого раствора точкой b. После окончания кристаллизации сплав 2 будет состоять только из твердого раствора α. После достижения температуры t6 твердый раствор этого состава оказывается насыщенным, а при более низких температурах – пересыщенным, что влечет за собой его распад с выделением избыточного количества металла В. Следовательно, при температуре ниже t6 сплав состоит из двух фаз: α +В. Состав α –раствора с понижением температуры изменяется по точкам линии DE и при нормальной комнатной температуре сплав будет состоять из кристаллов твердого раствора α состава, отвечающего точке Е, и кристаллов металла В.
Сплав 3 начинает затвердевать при достижении температуры t7 и окончательно затвердевает при температуре tэ.
В процессе кристаллизации состав жидкой части сплава непрерывно меняется по линии ликвидуса, стремясь к эвтектическому составу (точка С), а состав твердой фазы изменяется по линии солидуса в сторону предельной растворимости (точка D). Соотношение между жидкой и твердой фазой в процессе кристаллизации сплава определяется по правилу отрезков. По достижении температуры tэ состав жидкой фазы достигает эвтектической концентрации С, и сплав окончательно затвердевает с одновременным выделением из жидкой фазы кристаллов твердого раствора α (концентрации точки D) и кристаллов компонента В, образующих эвтектику. Следовательно, после затвердевания сплав будет состоять из первичных предельно насыщенных (точка D) кристаллов твердого раствора α, выделившихся в интервале температур t7 – tэ и эвтектики (αD +В), образовавшейся при температуре tэ.
Вследствие изменения растворимости В в А при дальнейшем понижении температуры твердый раствор α (как свободный, так и входящий в состав эвтектики) претерпевает распад с выделением избыточного металла В. После окончательного охлаждения состав α – фазы определится точкой Е.
Сплав, имеющий концентрацию, соответствующую точке С, после затвердевания будет состоять из одной эвтектики (α+В).
Кристаллизация заэвтектических сплавов будет протекать совершенно аналогично сплаву 3, только вместо первичных кристаллов α будет выделяться кристаллы чистого компонента В.
Свойства сплавов, как это показал Н.С. Курнаков, изменяются в области однородных твердых растворов по кривой, а в области смеси фаз - по прямой; крайние точки на прямой соответствуют свойствам предельно насыщенных твердых растворов. Как показал академик А.А. Бочвар, чем больше интервал температур, в котором происходит процесс кристаллизации, тем меньше жидкотекучесть сплава, т.е. тем хуже сплав заполняет форму, тем большее развитие получает рассеянная по всему мелкая пористость и тем выше склонность сплава к образованию горячих трещин. Наилучшими литейными свойствами обладают сплавы, затвердевающие в небольшом интервале температур, в частности эвтектический состав. Сплавы, имеющие структуру однородного твердого раствора, обладают высокой пластичностью и легко деформируются как в холодном, так и в горячем состоянии. Пластическая деформация сплавов, имеющих двухфазное строение, связана со значительно большими трудностями. Особенно снижается пластичность при появлении в структуре эвтектики.
Поэтому в сплавах, предназначенных для обработки давлением, максимум растворимости при эвтектической температуре является верхним пределом содержания компонентов. Наоборот, для обеспечения высоких литейных свойств концентрация компонентов в литейных сплавах обычно превышает максимальную растворимость в твердом состоянии при эвтектической температуре. Сплавы, обладающие ограниченной растворимостью в твердом состоянии, могут быть упрочнены путем термической обработки.
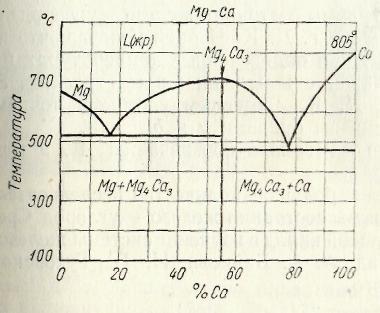
По диаграмме состояния четвертого типа (рис. 4) затвердевают сплавы, компоненты которых в жидком состоянии неограниченно растворяются друг в друге, а при затвердевании образуют химическое соединение.
Химическое соединение представляет собой фазы постоянного состава, обычно имеющие свою особую кристаллическую решетку, отличную от решеток образующих его компонентов. Поэтому свойства химического соединения самостоятельны и не зависят от свойств компонентов.
На базе химических соединений могут образовываться твердые растворы. При образовании твердого раствора кристаллическая решетка химического соединения сохраняется, а избыточное количество атомов, например компонента В, замещает в решетке часть атомов компонента А.
Нормальные валентные соединения типа Mg2Si, Mg2Sn (станнум), Mg2Pb в металлических сплавах образуются редко. В большинстве случаев образующиеся в металлических системах химические соединения не подчиняются нормальным правилам валентности.
В металлических системах большое значение имеют электронные соединения.
Соединения этого типа имеют совершенно определенное отношение числа валентных электронов к числу атомов, входящих в соединение. Так, существует ряд соединений, у которых это отношение равно 3:2, у других 21:13, у третьих 7:4. Каждому из этих соотношений соответствует и определенный тип кристаллической решетки. Все соединения, имеющие отношение числа валентных электронов к числу атомов, равное 3:2, имеют кристаллическую решетку центрированного куба. К этому типу относятся такие соединения, как CuZn (цинкумат), Cu3Al, Cu5Sn и другие, известные под названием β-фаз.
Соединениям Cu5Zn8, Cu9Al4 и другим, имеющим отношение 21:13, свойственна сложная кубическая решетка; эти соединения носят название γ-фазы.
Наконец, таким соединениям, как CuZn3, Cu3Sn, Cu3Si и другим, имеющим отношение 7:4, свойственна гексагональная решетка. Эти соединения носят название ε-фазы. Большая группа металлов (Fe, Cr, Mo, W, Ti и др.) образуют с углеродом, азотом, водородом, и бором, имеющими малый атомный радиус, химические соединения, которые носят название фазы внедрения. Эта группа соединений образуется при условии, если отношение атомного радиуса металлоида к атомному радиусу металла меньше или равно 0,59. В этом случае образуется соединение, имеющее формулу М4Х (Mn4N, Fe4N и т.д.), М2Х (W2N, Fe2N), MX (TiN, TiC, WC, VC) или (ZrH2).
Металлические атомы в фазах внедрения образуют одну из наиболее простых кристаллических решеток (кубическую, гексагональную), в которую внедряются атомы металлоидов, занимая в ней свободные поры.

Диаграмма состояния для случая, когда два компонента обладают полной взаимной растворимостью в жидком состоянии, не растворимы в твердом состоянии и образуют устойчивое химическое соединение, представлена на рис. 4.
Процесс кристаллизации сплавов А-АnВm начинается при температурах, отвечающих линии АС1D; при этом по линии АС1 кристаллизуется металл А, а по линии C1D – химическое соединение АnВm. Окончание процесса кристаллизации соответствует эвтектической температуре (линия ЕС1F).
Кристаллизация сплавов АnВm – В начинается при температурах, соответствующих линии DC11B; при этом по линии DC11 кристаллизуется соединение АnВm , а по линии C11B – чистый металл В. Конец кристаллизации соответствует эвтектической линии GC11K. Как видно из рис. 11, в данной системе образуются две эвтектики; одна С1, состоящая из смеси кристаллов А и соединения АnВm , и другая С11, состоящая из смеси соединения АnВm и кристаллов В.
В первой системе А - АnВm доэвтектические сплавы состоят из первичных кристаллов компонента А и эвтектики С1, а заэвтектические сплавы – из кристаллов соединения АnВm и эвтектики С1. Во второй системе АnВm – В доэвтектические сплавы содержат, кроме эвтектики С11, первичные кристаллы соединения АnВm и заэвтектические сплавы – кристаллы чистого металла В.
Однако следует иметь в виду, что в подавляющем большинстве случаев чистые компоненты и химическое соединение образуют области твердых растворов в ограниченных пределах. В этом случае диаграмму следует рассматривать как сложную, состоящую из двух диаграмм эвтектического типа с ограниченной растворимостью в твердом состоянии.
Правило отрезков
В любой точке диаграммы, когда в сплаве одновременно существуют две фазы, можно определить концентрацию обеих фаз и их количество. Для этого служит так называемое правило отрезков или правило рычага.
В точке а, показывающей состояние сплава К при температуре t1 (риc. 1), сплав состоит из кристаллов сурьмы и жидкости. Выше точки l сплав находится в однофазном состоянии, и концентрация компонентов в этой фазе (т.е. в жидкости) определяется проекцией точки a. При охлаждении из, сплава выделяются кристаллы сурьмы, и состав жидкости изменяется в сторону увеличения в ней свинца. При температуре t1 концентрация сурьмы в жидкости определяется проекцией точки в; это максимальное количество сурьмы, которое может содержать жидкость при t1.
По достижении эвтектической температуры жидкость принимает эвтектическую концентрацию. Следовательно, при охлаждении сплава К концентрация жидкости меняется по кривой 1с. Выделяющиеся кристаллы свинца имеют постоянный состав - это чистый свинец, концентрация которого лежит на вертикальной оси BN.
Первое положение правила отрезков формулируется следующим образом: чтобы определить концентрацию компонентов в фазах, через данную точку, характеризующую состояние сплава, проводят горизонтальную линию до пересечений с линиями, ограничивающими данную область: проекции точек пересечения на ось концентраций показывают составы фаз.
Второе положение правила отрезков формулируется так; для того чтобы определить количественное соотношение фаз, через заданную точку проводят горизонтальную линию. Отрезки этой линии между заданной точкой и точками, определяющими составы фаз, обратно пропорционально количествам этих фаз.
В качестве примера определим концентрацию (состав) фаз и количественное соотношение фаз для сплава с содержанием 60 % Sb и 40 % Pb при 350 °С.
В соответствии с первым положением правила отрезков, концентрация твердой фазы определится проекцией точки а на ось абсцисс, т.е. она равна 100 % Sb, состав жидкой фазы определится проекцией точки в на ось абсцисс, что соответствует 30 % Sb.
В соответствии со вторым положением правила отрезков весовое количество фаз сплава при температуре 350 °С определится отрезками: ва - вес кристаллов Sb, ас - вес жидкой фазы, вс - вес всего сплава.
Спроектировав концентрационные отрезки на ось абсцисс, получим: ва = 60 - 30 = 30 %; ас =100 - 60 = 40 %; ВE=100-30=70 %.
Следовательно, весовое количество сурьмы QSb и жидкости Ql, определится соотношением отрезков:
QSb ва Qс ▪ ва
— = ----- ,откуда QSb = ------ ▪100 %;
Qс BE BE
Ql ac Qc ▪ ac
— = —; Ql = —— ▪100 %;
Qc BE BE
Qс - количеcтво всего сплава.
Вид диаграммы определяется характером взаимодействий, которые возникают между компонентами в жидком и твердом состояниях.
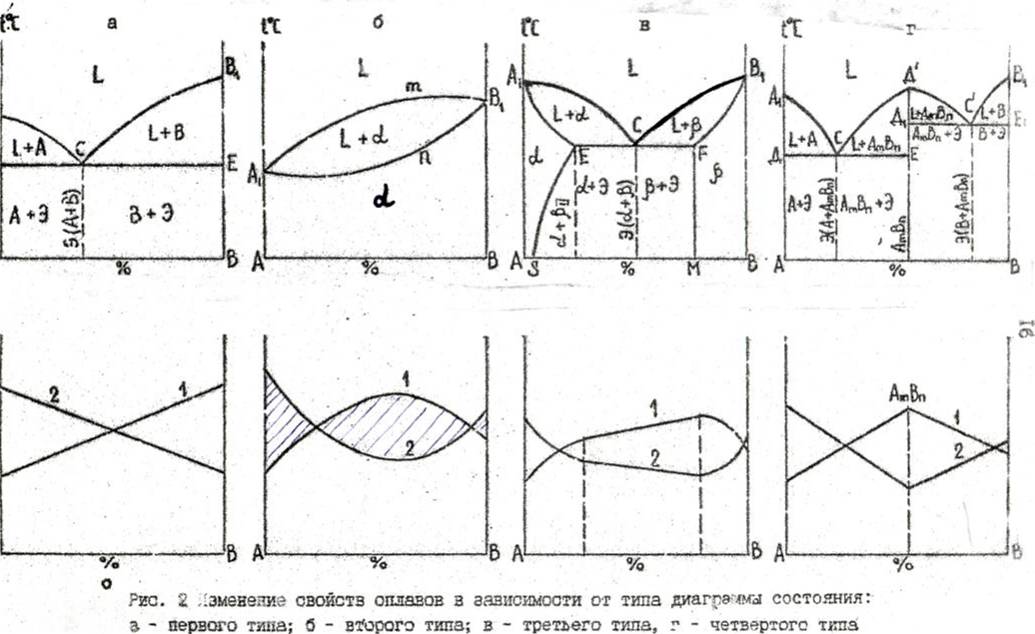
Наиболее типичные диаграммы состояния металлических систем приведены на рис. 5.
1. Диаграмма состояния для сплавов, образующих механические смеси из чистых компонентов (I типа, риc. 5,а).
Оба компонента в жидком состоянии неограниченно растворимы, а в твердом - нерастворимы и не образуют химических соединений,
Компоненты: А и В (К = 2). Фазы: жидкость L, кристаллы А и кристаллы В (Ф = 3).
Линия A1CB1 является линией ликвидус, линия ДСЕ - линией солидус и линией эвтектического превращения. На линии ДСЕ из жидкости концентрации точки С одновременно выделяются кристаллы А состава точки Д и кристаллы В состава точки Е. т.е.
Lc = кр.Ад + кр.ВЕ
Эта механическая смесь называется эвтектикой.
Сплавы, лежащие левее точки С, называют доэвтектическими, а сплавы, лежащие правее точки С, - заэвтектическими.
Доэвтектические сплавы состоят из смеси кристаллов А и эвтектики (кр.А + Э), заэвтектические - из смеси кристаллов В и эвтектики (кр.В + Э).
2. Диаграмма состояния для сплавов с неограниченной растворимостью компонентов в твердом состояния (II типа, рис.5,б).
Оба компонента неограниченно растворимы в жидком и твердом состоянии и не образуют химических соединений.
Компоненты: А,В (К - 2). Фазы: L, кристаллы α (Ф=2),
линия АmВ -линия ликвидус, линия АnВ - линия солидус.
Если два компонента неограниченно растворяются в жидком и твердом состояниях, то возможно существование только двух фаз -жидкого раствора L и твердого α-раствора. Следовательно, трех фаз быть не может, кристаллизации при постоянной температуре не наблюдается и горизонтальной линии на диаграмме нет. Диаграмма состоит из трех областей: жидкость, жидкость - твердый раствор и твердый раствор.
При двух компонентах и двух фазах система моновариантна (С=K-f + l = 2-2+l=l), т.е. если изменяется температура, то изменяется и концентрация компонентов в фазах; каждой температуре соответствуют строго определенные составы Фаз.
Концентрация и количество фаз у сплава, лежащего между линиями ликвидус и солидус, определяется правилом отрезков.
Следует обратить внимание на то, что во всем интервале кристаллизации (между линиями ликвидус и солидус) из жидкого сплава выделяются кристаллы, более богатые тугоплавким компонентом.
3. Диаграмма состояния для сплавов с ограниченной растворимостью в твердом состоянии (III типа, рис. 5,в).
Оба компонента неограниченно растворимы в жидком состоянии, ограниченно - в твердом и не образуют химических соединений.
Компоненты А и В (К = 2), Фазы ( L, кристаллы α, кристаллы β (Ф = 3), кристаллы α - твердый раствор компонента В в компоненте А, кристаллы β - твердый раствор компонента А в компоненте В.
Линия A1CB1 - линия ликвидус.
Линия A1ECFB1 - линия солидус.
Линия ECF - линия эвтектического превращения:
Lc = кр.αЕ + кр. βЕ
└ эвтектика ┘
Линия ES - линия ограниченной растворимости в твердом состоянии компонента В в компоненте А.
Линия FM - линия ограниченной растворимости в твердом состоянии компонента А в компоненте В.
Структурные составляющие, образующиеся в процессе охлаждения сплавов данной системы, показаны на рис 5,в.
4. Диаграмма состояния для сплавов, образующих химическое соединение (IV типа, рис. 5,г).
Если компоненты А и В образуют химическое соединение AnBm, то, следовательно, на n + m его атомов приходится n атомов А и m атомов В.
Компоненты А и В (К =2).Фазы: кристаллы А, кристаллы AnBm и L или кристаллы АnBm кристаллы В и L.
Линия A1CДС'B1 - линия ликвидус
Линия ДCEД1E1 - линия солидус
Линия ДСЕ - линия эвтектического превращения:
Lc =кр.Ад + кр.АnВmЕ , (Ф = 3)
└ (эвтектика) ┘
Линия Д1C'E1 - линия эвтектического превращения:
Lc' = кр.АnBmД1. + кр.BЕ1 , (Ф = 3)
└ (эвтектика) ┘
Диаграмму состояния, приведенную на рис. 2,г. следует рассматривать как сложную, состоящую ив двух простых диаграмм:
Компонент А - химические соединение AnBm.
Компонент В - химическое соединение AnBm.
Точка Д' - сингулярная точка, где образуется химическое соединение AnBm.
Связь между свойствами сплавов и типом диаграмм состояния
Химический состав и структура определяют свойства металлического сплава. Структура, в свою очередь, зависит от характера взаимодействия компонентов, входящих в состав сплава, что и отражают диаграммы состояния. Следовательно, между диаграммами состояния и полученными свойствами сплавов существует определенная зависимость. Эта зависимость впервые была изучена Н.С. Курнаковым, который представил ее в виде диаграммы состав - свойства. На рис. 5 приведены четыре основных типа диаграмм состояния и соответствующие им закономерности изменения свойств сплава с изменением концентрации. По ординате на нижних диаграммах откладывают показатели свойств или обратные им числовые величины. В данном случае рассмотрены твердости (кривая I) и электропроводность (кривая 2). Крайний ординаты на диаграммах показывают свойства чистых компонентов.
Если компоненты сплава образуют механические смеси, то свойства сплавов
сконцентрированной усадочной раковиной.
Обработке давлением лучше поддаются однофазные сплавы - чистые металлы или однородные твердые растворы, обладающие меньшим сопротивлением пластическому деформированию.
Обрабатываемость режущим инструментом повышается c применением структурно-неоднородных сплавов. Наличие в сплаве твердых фаз способствует износу режущего инструмента. Это однофазные твердые растворы и химические соединения. Если в сплаве отсутствуют твердые фазы, то двухфазные сплавы легче обрабатываются резанием, чем однофазные, которые имеют более высокую коррозионную стойкость, чем двухфазные. Таким образом, характер образующихся фаз определяет свойства сплава и обусловливает вид диаграммы состояния.
Для усвоения материала необходимо:
Вычертить схемы четырех типов диаграмм состояния и построить графики изменения свойств сплавов в зависимости от их состава.
Охарактеризовать линии, точки и области диаграмм состояния указанных типов.
Для всех диаграмм состояния (по заданию преподавателя) построить кривую охлаждения сплава и определить при конкретной температуре концентрацию и количество фаз сплава, пользуясь правилом фаз и правилом отрезков.
Используя полученные данные описать изменение механических, физико-химических и технологических свойств сплавов в зависимости от изменения концентрации компонентов.
Вопросы для самопроверки:
Что понимают под системой?
Что называют компонентами?
Какая часть системы называется фазой?
Когда образуется механическая смесь?
Какие фазы называют твердыми растворами?
Чем отличаются твердые растворы внедрения от твердых растворов замещения?
Какие растворы называют неупорядоченными?
Назовите одно из условий неограниченной растворимости.
Какие твердые растворы называют упорядоченными?
Какую механическую смесь называют эвтектикой?
Что выражает закон Гиббса?
Что понимают под числом степеней свободы (вариантностью) системы?
Сформулируйте первую и вторую часть правила отрезков.
Какую температуру называют точкой Курнакова?
Литература:
1. Иваней А.А. Электронный конспект лекций.
2.Технология металлов и материаловедение: Учебник для вузов и техникумов /Под ред. Л.Ф. Усовой – Производственное издание. М.: Металлургия, 1987. – с.106-123;
3. Гуляев А.П. Металловедение: Учеб. пособие для вузов. – 6-е изд., перераб. и доп. – М.: Металлургия, 1986. – 542 с.89-141
Форма отчета
Практическая работа №1.
«Связь между свойствами сплава и типом диаграммы состояния»
Дать определение каждого типа диаграмм состояния.
Вычертить схемы четырех типов диаграмм состояния и построить графики изменения свойств сплавов в зависимости от их состава.
Охарактеризовать линии, точки и области диаграмм состояния указанных типов.
Для всех диаграмм состояния (по заданию) построить кривую охлаждения сплава и определить при конкретной температуре концентрацию и количество фаз сплава, пользуясь правилом фаз и правилом отрезков.
Используя полученные данные описать изменение механических, физико-химических и технологических свойств сплавов в зависимости от изменения концентрации компонентов.
Таблица заданий.
№ варианта |
Температура, 0С/ Концентрация |
|||||||
I тип |
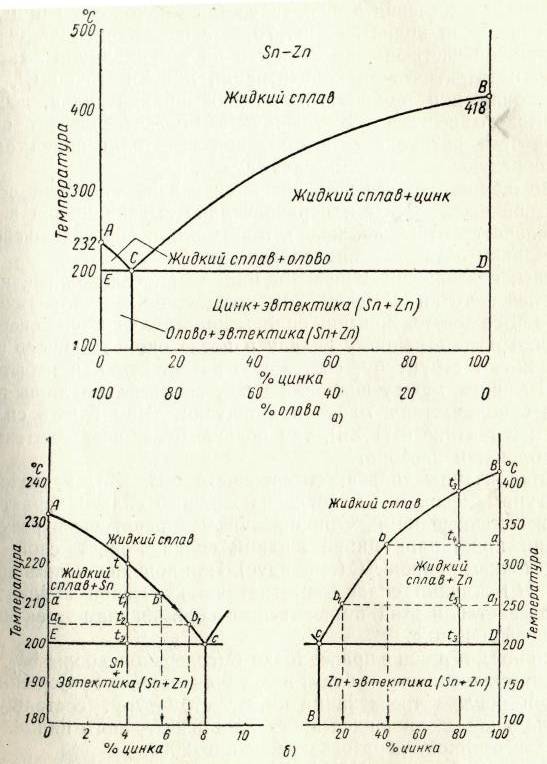
Sn-Zn |
II тип |
Cu-Ni |
III тип |
Pb-Sn |
IV тип |
Mg-Ca |
|
1 |
210 |
95-5 |
1490 |
95-5 |
190 |
95-5 |
635 |
95-5 |
2 |
220 |
90-10 |
1480 |
90-10 |
195 |
90-10 |
630 |
90-10 |
3 |
230 |
85-15 |
1470 |
85-15 |
200 |
85-15 |
625 |
85-15 |
4 |
240 |
80-20 |
1460 |
80-20 |
205 |
80-20 |
620 |
80-20 |
5 |
250 |
75-25 |
1450 |
75-25 |
210 |
75-25 |
615 |
75-25 |
6 |
260 |
70-30 |
1440 |
70-30 |
215 |
70-30 |
610 |
70-30 |
7 |
270 |
65-35 |
1430 |
65-35 |
220 |
65-35 |
605 |
65-35 |
8 |
280 |
60-40 |
1420 |
60-40 |
225 |
60-40 |
600 |
60-40 |
9 |
290 |
55-45 |
1410 |
55-45 |
230 |
55-45 |
595 |
55-45 |
10 |
300 |
50-50 |
1400 |
50-50 |
235 |
50-50 |
590 |
50-50 |
11 |
310 |
45-55 |
1300 |
45-55 |
240 |
45-55 |
585 |
45-55 |
12 |
320 |
40-60 |
1290 |
40-60 |
245 |
40-60 |
580 |
40-60 |
13 |
330 |
35-65 |
1280 |
35-65 |
250 |
35-65 |
575 |
35-65 |
14 |
340 |
30-70 |
1270 |
30-70 |
255 |
30-70 |
570 |
30-70 |
15 |
350 |
25-75 |
1260 |
25-75 |
260 |
25-75 |
560 |
25-75 |
16 |
360 |
20-80 |
1250 |
20-80 |
265 |
20-80 |
555 |
20-80 |
17 |
370 |
15-85 |
1240 |
15-85 |
270 |
15-85 |
550 |
15-85 |
18 |
380 |
10-90 |
1230 |
10-90 |
275 |
10-90 |
545 |
10-90 |
19 |
390 |
5-95 |
1220 |
5-95 |
280 |
5-95 |
530 |
5-95 |
20 |
400 |
5-95 |
1200 |
5-95 |
285 |
5-95 |
525 |
5-95 |
 Далее
представлены 4 типа диаграмм для
выполнения задания.
Далее
представлены 4 типа диаграмм для
выполнения задания.
![]()
![]()
![]()
![]()
Практическая работа № 2
«Термическая обработка сталей»
Цель работы - ознакомиться с методиками термической обработки сталей.
Задачи:
Изучить теоретические сведения термической обработки сталей.
Определить режим закалки образца стали в соответствии с заданием.
Определить режим низкого, среднего и высокого отпуска образцов стали в соответствии с заданием.
Указать твердость образцов после закалки.
Указать твердость образцов после отпуска.
Охарактеризовать структуру стали после выполненных различных видов термической обработки.
Сделать анализ влияния термической обработки стали на ее механические свойства.
Краткие теоретические сведения
ОСНОВЫ ТЕОРИИ ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ
Свойства сплава зависят от его структуры (внутреннего строения). Основным способом, позволяющим изменять структуру, а, следовательно, и свойства, является термическая обработка.
Основы термической обработки были разработаны великим русским ученым Д. К. Черновым. Дальнейшее развитие теория и практика термической обработки получила в работах С. С. Штейнберга, А. А. Бочвара, Г. В. Курдюмова, Н. А. Минкевича, А. П. Гуляева, Э. Бейна, Э. Давенпорта и других ученых.
Термическая обработка представляет собой совокупность операций нагрева, выдержки и охлаждения, проводимых в определенной последовательности с целью изменения внутреннего строения сплава и получения нужных свойств. Любой вид термической обработки может быть представлен графиком в координатах температура—время (рис. 1 а).
основные виды термической обработки стали
По классификации А. А. Бочвара различают четыре основных вида термической обработки: I) отжиг I рода; 2) отжиг II рода; 3) закалка; 4) отпуск.
Отжиг I рода. Этот вид термической обработки возможен для любых металлов и сплавов. Его проведение не обусловлено фазовыми превращениями в твердом состоянии. Нагрев при отжиге I рода, повышая подвижность атомов, частично или полностью устраняет химическую неоднородность, уменьшает внутренние напряжения, т. е. способствует получению более равновесного состояния. Основное значение при проведении такого отжига имеют температуры нагрева и время выдержки при этой температуре, так как именно эти параметры
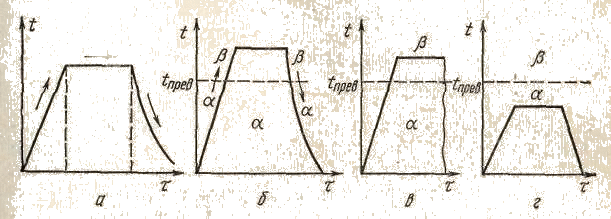
Рис. 1. Графики различных видов термической обработки: а — общая схема; б — отжиг II рода; в — закалка; г — отпуск
определяют скорость процессов, устраняющих отклонения от равновесного состояния. Скорость нагрева и охлаждения для отжига I рода имеет второстепенное значение.
Различают следующие разновидности отжига I рода:
Диффузионный отжиг (гомогенизирующий) используют для устранения химической неоднородности, возникающей при кристаллизации сплава (дендритной ликвации).
Выравнивание химического состава происходит благодаря диффузионным процессам, скорость которых зависит от температуры. Поэтому обычно температура такого отжига составляет 0,8—0,9Тпл. Время выдержки при этой температуре должно обеспечить выравнивание состава и растворение избыточных фаз.
Рекристаллизационный отжиг применяют после холодной пластической деформации (холодной обработки давлением) для снятия наклепа и получения равновесного состояния сплава. В результате рекристаллизации в деформированном металле образуются новые зерна, снимаются напряжения и восстанавливается пластичность металла.
Отжиг для снятия напряжений, возникающих при ковке, сварке, литье и т. п., которые могут вызвать коробление, т. е. изменение формы, размеров и даже разрушение изделий.
Отжиг II рода. Так называют отжиг металлов и сплавов, испытывающих фазовые превращения при нагреве и охлаждении. Графически такая термическая обработка представлена на рис. 1 б. При нагреве происходит фазовое превращение α→β, а при охлаждении обратное: β→α.
Весь процесс можно записать так:
|
нагрев |
|
охлаждение |
|
α |
→ |
β |
→ |
α |
Такую термическую обработку проводят для сплавов, в которых имеются полиморфные, эвтектоидные или перитектоидные превращения, а также может быть переменной растворимость в твердом состоянии. Практическая целесообразность фазовой перекристаллизации определяется тем, каково влияние структурных изменений на свойства сплава.
Закалка. Закалка, как и отжиг II рода, осуществляется только для металлов и сплавов, имеющих фазовые превращения в твердом состоянии. Главное различие этих видов термической обработки — скорость охлаждения. Все виды отжига проводят с медленным охлаждением, а закалку — с быстрым.
Графически закалка представлена на рис. 1 в. При закалке возможны два варианта структурных изменений: 1) α→β, т. е. быстрым охлаждением фиксируется высокотемпературное состояние; 2) α→β→α', где α' — метастабильная фаза, состав которой одинаков с составом исходной β фазы. В этом случае при охлаждении происходит бездиффузионное превращение, имеющее мартенситную кинетику. Для закалки основными параметрами являются температура нагрева, время выдержки и скорость охлаждения.
Отпуск. Этот вид термической обработки применим лишь к закаленным сплавам. При этом закаленные изделия нагревают ниже температуры фазового превращения (рис. 1 г).
Основные параметры отпуска — температура нагрева и время выдержки. В результате отпуска уменьшаются внутренние напряжения, сплавы переходят в более равновесное состояние.
Кроме этих основных видов термической обработки, имеются еще два принципиально различающихся способа обработки, представляющих сочетание термической обработки с металлургией или механической технологией.
Химико-термическая обработка (ХТО). При этом виде обработки обязательно изменяется химический состав поверхностных слоев изделия. При ХТО обрабатываемые изделия нагревают в каких-либо химически активных средах.
В результате диффузии происходит насыщение поверхностных слоев тем или иным элементом (обычно на небольшую глубину). Изменяя химический состав поверхностных слоев, тем самым изменяют их свойства (твердость, износоустойчивость, антикоррозионные свойства и т. д.).
Поскольку диффузионные процессы в твердом состоянии протекают медленно, ХТО обычно осуществляется за длительное время. Температуру процесса выбирают конкретно для каждого вида ХТО.
Термомеханическая обработка (ТМО). Этот вид обработки появился сравнительно недавно. При ТМО сочетают пластическую деформацию с термической обработкой таким образом, чтобы наклеп оказывал влияние на кинетику фазовых и структурных превращений, происходящих при термической обработке.
ПРЕВРАЩЕНИЯ В СТАЛИ ПРИ НАГРЕВЕ
В основе всех превращений, которые совершаются в стали при нагреве, лежит стремление системы к минимуму свободной энергии (рис. 2). Теоретически превращение перлита в аустенит должно совершаться при температуре А1, т. е. при 727° С. Фактически же для этого превращения нужен перегрев, так как экспериментально было установлено, что даже при обычных скоростях нагрева температура критических точек А1 и А3 повышается.
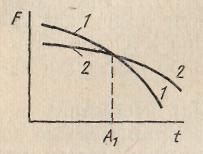
Рис. 2. Изменение свободной энергии аустенита (1) и перлита (2) в зависимости от температуры
Кроме того, чем выше температура, тем быстрее совершается превращение. Превращение перлита в аустенит сопровождается полиморфным превращением Feα ↔Feγ, а также растворением цементита Fе3С в аустените. Для исследования процессов, происходящих при нагреве стали, строят диаграммы изотермического образования аустенита. Для этого образцы нагревают до температуры выше А1 и выдерживают при ней, фиксируя начало и конец превращения. На рис. 3 приведена такая диаграмма для стали с 0,8% С.
Превращение начинается с зарождения центров аустенитных зерен на поверхности раздела феррит—цементит (рис. 3 А). Экспериментально аустенит обнаруживается уже при небольших перегревах (выше 727° С) и очень малых выдержках. (По данным некоторых исследователей, в процессе превращения перлита в аустенит инкубационный период отсутствует, т. е. превращение начинается сразу при нагреве до температуры несколько выше точки А1 (линия I на рис. 3). Это объясняется тем, что в стали поверхность раздела феррит — цементит сильно развита.
Время превращения перлита в аустенит при изотермической выдержке существенно зависит от температуры. Это наглядно показывают кривые начала (1) и конца (2) превращения (см. рис. 3). Объясняется это тем, что с увеличением степени перегрева относительно А1 уменьшается размер критического зародыша аустенита, увеличивается скорость возникновения зародышей и линейная скорость их роста.
Правее линии 1 происходит образование зародышей аустенита на поверхности раздела феррита и цементита в перлите (схема А). Образующиеся зерна аустенита вначале имеют такую же концентрацию углерода, как и исходная фаза — феррит, так как полиморфное превращение протекает с большей скоростью, чем диффузия углерода. Затем в аустените начинает растворяться вторая фаза перлита — цементит (см. рис. 3, область между линиями 2 и 3, схемы Б, В), содержание углерода в аустените увеличивается. К концу превращения в тех местах, где находились пластинки цементита, концентрация углерода в аустените становится более высокой по сравнению с участками, в которых до превращения был феррит. Поэтому для выравнивания состава аустенита требуется некоторое время, зависящее от температуры — чем выше температура, при которой совершалось превращение П→А, тем быстрее завершится диффузионный процесс перераспределения углерода в аустените (с ростом температуры нагрева уменьшается скачок концентраций на границе аустенит — феррит— линии GP и GS сближаются).
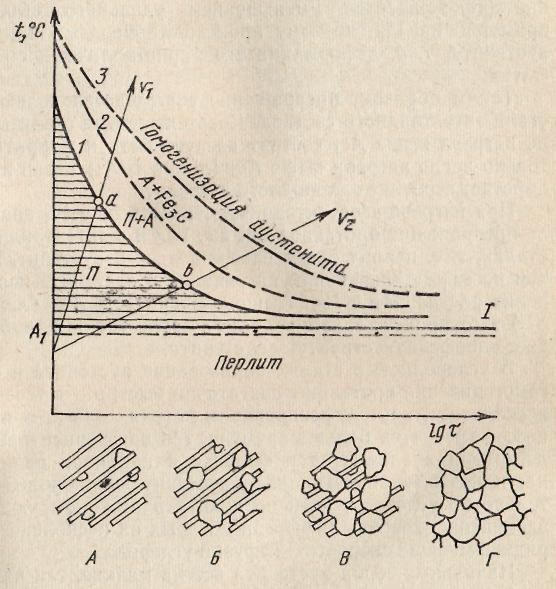
Рис. 3. Диаграмма изотермического образования аустенита:
1 — начало образования аустенита; 2 — конец превращения перлита в аустенит; 3 — полное растворение цементита; а, б — точки начала превращения перлита в аустенит при нагреве со скоростями υ1 и υ2 (υ1>υ2); А, Б, В, Г — последовательные стадии превращения перлита в аустенит
Влияние скорости нагрева на продолжительность превращения характеризуется лучами υ1 и υ2. При меньшей скорости нагрева (луч υ2) превращение П—А произойдет при более низких температурах по сравнению с более быстрым нагревом (луч υ1).
На скорость превращения перлита в аустенит влияет также степень дисперсности перлита — чем мельче пластинки цементита, тем быстрее образуется аустенит, так как в этом случае больше межфазная поверхность феррита с цементитом. Перлито-аустенитное превращение сопровождается уменьшением удельного объема примерно на 1%, поэтому происходит фазовый наклеп аустенита, т. е. деформация его кристаллической решетки.
Таким образом, превращение совершается только в стали эвтектоидного состава. Доэвтектоидные стали после нагрева выше Ас1 состоят из аустенита и феррита и только после нагрева выше Ас3 (линия GOS) сталь приобретает строение однородного аустенита.
При нагреве заэвтектоидных сталей выше Ас1 вначале превращение протекает так же, как и в эвтектоидных сталях, т. е. перлит будет превращаться в аустенит. Затем по мере дальнейшего нагревания в аустените постепенно растворяется ЦII. Выше температуры Аст (линия SE) этот процесс заканчивается, и сталь также приобретает однофазную структуру аустенита.
В углеродистых сталях образование аустенита и его гомогенизация протекают достаточно быстро — в течение нескольких минут. В легированных сталях для этих процессов требуется больше времени, так как концентрация легирующих элементов в феррите и карбидах различна, и поэтому образующийся аустенит неоднороден не только по углероду, но и по концентрации легирующих элементов, скорость диффузии которых на несколько порядков меньше скорости диффузии углерода.
Начальные зерна аустенита всегда мелкие, так как в каждой перлитной колонии одновременно зарождается несколько центров кристаллизации аустенита (см. схему на рис. 3). При дальнейшем нагреве зерна аустенита растут, причем в различных сталях с различной скоростью.
Стали различают по склонности к росту зерна аустенита при нагреве. Если зерно аустенита начинает быстро расти даже при незначительном нагреве выше A1 то сталь считают наследственно крупнозернистой; если зерно растет только при большом перегреве, то сталь является наследственно мелкозернистой. Даже стали одной марки, но разных плавок могут сильно различаться по склонности к росту аустенитного зерна. Это объясняется тем, что они содержат различное количество неметаллических включении (окислов, нитридов, сульфидов и т. п.), которые могут затруднять рост аустенитного зерна при нагреве. Таким образом, склонность к росту аустенитного зерна является плавочной характеристикой.
Такие элементы, как ванадий, титан, молибден, вольфрам, алюминий, уменьшают склонность к росту зерна аустенита, а марганец и фосфор увеличивают ее. Заэвтектоидные стали, как правило, менее склонны к росту зерна. Условия выплавки стали также имеют большое значение, например кипящая сталь обычно бывает наследственно крупнозернистой.
При последующем охлаждении зерна аустенита не измельчаются. Это следует учитывать при назначении режимов термической обработки, так как от размеров зерна существенно зависят механические свойства. Так, например, ударная вязкость мелкозернистой стали может в несколько раз превышать ударную вязкость крупнозернистой стали той же марки.
Различают величину зерна наследственного и действительного.
Для определения наследственного зерна образцы нагревают до 930°С (проявляется склонность стали к росту зерна) и затем определяют размер зерна. От размера зерна аустенита зависит поведение нагретой стали в различных процессах термической обработки и пластической деформации. Особенно чувствительна к размеру зерна аустенита ударная вязкость.
Действительная величина зерна — это размер зерна при обычных температурах, полученный после той или иной термической обработки.
Существует стандартная шкала величины зерна, согласно которой величину зерна характеризуют номером по восьмибалльной системе. Величину зерна определяют под микроскопом при увеличении в 100 раз и сравнивают с размерами зерна стандартной шкалы. Стали, имеющие зерно до номера 4, считают крупнозернистыми, а имеющие номер 5—8 — мелкозернистыми.
ПРЕВРАЩЕНИЯ В СТАЛИ ПРИ ОХЛАЖДЕНИИ
Если сталь охлаждать очень медленно, то происходящие превращения можно установить, пользуясь диаграммой состояния Fe — Fe3C. При 727°С (А1) должно происходить эвтектоидное превращение Feγ(C)→Feα (С) + Fe3C.
Термодинамическим условием этого превращения является некоторая степень переохлаждения (охлаждение ниже А1), когда свободная энергия перлита становится меньше свободной энергии аустенита (см. рис. 2).
При охлаждении стали с большей скоростью кинетику и механизм превращения аустенита выясняют с помощью постановки специальных экспериментов. Рассмотрим закономерность превращения переохлажденного аустенита стали эвтектоидного состава (0,8% С). Образцы из этой стали (так же, как и образцы из любой другой стали) нагревают до температуры, при которой ее структура состоит из однородного аустенита. Из диаграммы Fe — Fe3C видно, что это температура порядка 770°С. Затем образцы быстро переносят в термостаты с заданной температурой, меньшей A1(интервал между изотермами обычно 25—50° С), и в процессе изотермической выдержки наблюдают за происходящими в аустените превращениями. Наблюдения можно проводить, пользуясь различными методами: измеряя твердость, электросопротивление, магнитные характеристики и т. п.
Превращение аустенита можно легко обнаружить с помощью наблюдений за изменениями магнитных характеристик образца, так как аустенит парамагнитен, а образующаяся механическая смесь феррита и цементита обладает ферромагнитными свойствами.
В результате получают серию кинетических кривых (см. рис. 4 а). По оси абсцисс откладывают время, по оси ординат—процент превратившегося аустенита. Вначале наблюдается инкубационный или подготовительный период — время, в течение которого сохраняется переохлажденный аустенит (Оа1 Оа2 и т. д.). Точки а — это начало превращения, они соответствуют превращению 0,5—1% аустенита. Характер кривой показывает, что превращение протекает с различной скоростью и достигает максимума при образовании примерно 50% продуктов превращения. После получения около 70% продуктов превращения скорость начинает уменьшаться и постепенно затухает по мере приближения к 0% количества оставшегося аустенита (b1,b2, b3 и т. д.).
С увеличением степени переохлаждения устойчивость переохлажденного аустенита уменьшается (Oa1>Oa2>Оа3), но достигнув минимума при переохлаждении ниже А1 на 150—200°С, вновь увеличивается (Oa4< <Oа5<Oа6).
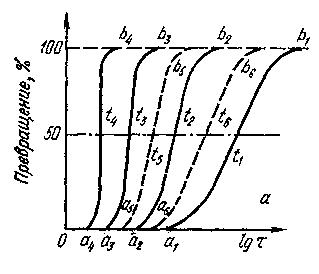
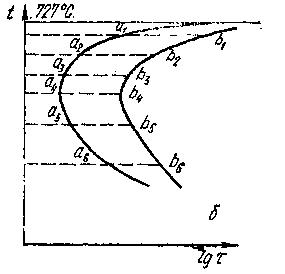
Рис. 4. Кинетические кривые изотермического превращения аустенита (а) и построенная по ним диаграмма (б)
По полученным экспериментальным точкам строят диаграмму изотермического превращения переохлажденного аустенита в координатах t — lgτ (см. рис. 4 б). На этой диаграмме левая кривая (а1 а2 а3 а4 а5 а6) является границей начала превращения переохлажденного аустенита, она показывает зависимость величины инкубационного периода от степени переохлаждения. Правая кривая (b1b2b3b4b5b6) показывает конец превращения аустенита, т. е. зависимость времени, необходимого для полного превращения аустенита, от степени переохлаждения.
Такие диаграммы обычно называют диаграммами изотермического превращения аустенита, а также С-образными диаграммами за сходство кривых начала и конца превращения аустенита с буквой С. (В переводе с англ. ТТТ-диаграммы — time — temperature — transformation (время — температура—превращение), что правильно отражает их сущность. Впервые диаграмма изотермического распада аустенита в стали была построена в 1930 г. Бейном и Давенпортом.
На рис. 5 приведена диаграмма изотермического превращения аустенита для эвтектоидной стали (0,8% С).
Перлитное превращение происходит в верхней части диаграммы (выше 500° С). Сущность превращения заключается в том, что в результате превращения аустенита образуется механическая смесь двух фаз — феррита и цементита, состав которых отличается от состава исходного аустенита. Исходный аустенит содержит 0,8% С, а образующиеся фазы — феррит ~0,02% С, цементит 6,67% С.
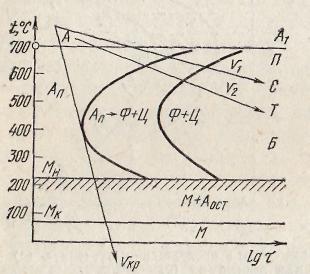
Рис. 5. Диаграмма изотермического превращения аустенита для эвтектоидной стали (0,8% С): А — устойчивый аустенит; Ап— аустенит, переохлажденный ниже А1, Ф — феррит; Ц — цементит
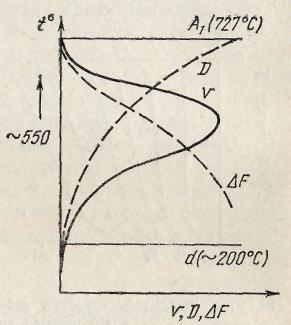
Рис. 6. Скорость распада аустенита v в зависимости от степени переохлаждения: D — скорость диффузии; ΔF — разность свободных энергий
Следовательно, это превращение является диффузионным. В то же время, как было показано, время устойчивости аустенита и скорость его превращения зависят от разности свободных энергий ΔF=FA— FП, т. е. от степени переохлаждения.
Скорость диффузии D и разность свободных энергий ΔF зависят от степени переохлаждения противоположно: скорость диффузии экспоненциально уменьшается по мере понижения температуры превращения, а разность свободных энергий увеличивается (рис. 6).
Максимальная скорость превращения соответствует переохлаждению ниже А1 на 150—200 град, т. е. соответствует минимальной устойчивости аустенита. При дальнейшем понижении температуры значительно уменьшается скорость диффузии, благодаря чему увеличивается устойчивость аустенита. Кривые начала и конца превращения сдвигаются вправо (см. рис. 4, б; 5).
Механизм перлитного превращения. При образовании из аустенита перлита ведущей фазой является цементит (в зерне аустенита всегда имеются флуктуационные обогащения углеродом, особенно вблизи границ зерна).
Зарождение цементитного зародыша облегчено на границе аустенитных зерен, так как здесь меньше работа образования критического зародыша. Образовавшаяся пластинка цементита растет, удлиняется и тем самым обедняет соседние участки аустенита углеродом. Поэтому рядом с пластинкой цементита — вдоль нее — образуется пластинка феррита. Такой кооперативный рост двухфазной колонии в результате диффузионного перераспределения компонентов — наиболее характерная особенность перлитного превращения. Перлит занимает объем больше, чем аустенит, поэтому по мере роста перлитной колонии в аустените возникают напряжения. Это вызывает образование пластинок перлита уже с другой ориентацией (рис. 7, 8).
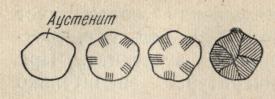
Рис. 7. Схема образования перлита

Рис. 8. Микроструктуры, характеризующие процесс образования перлита из аустенита при 705° С (Бейн), Х 500. Время превращения, с: а —400; б— 1150; в— 1320; г — 1450; д — 4000
Поскольку с увеличением степени переохлаждения растет число зародышей новых зерен, количество феррито-цементитных пластинок увеличивается, а их размеры и расстояния между ними сильно сокращаются. Дисперсность образующихся фаз увеличивается также и вследствие уменьшения скорости диффузии с переохлаждением.
Перлит, сорбит, троостит представляют собой механическую смесь феррита и цементита. Эти структуры различаются только степенью дисперсности карбидной составляющей, т. е. межпластиночным расстоянием, (средняя суммарная толщина соседних пластинок феррита и цементита) которое является важнейшей структурной характеристикой, определяющей механические свойства стали (рис. 9, а — е).
Резкой границы между П, С, Т не существует: по мере понижения температуры постепенно совершается переход от одной структуры к другой. Твердость феррито-цементитной смеси прямо пропорциональна площади поверхности раздела между ферритом и цементитом.
Поэтому с увеличением степени дисперсности фаз увеличивается их твердость (табл. 1).
Таблица. 1 Твердость фаз
tпревр, °C |
τпревр, °C |
Структура |
d, мкм |
Твердость, НВ |
700 |
600 |
П. п. |
1,0—0,77 |
200 |
675 |
30 |
Т.п. |
~0,5 |
250 |
650—600 |
10 |
С |
0,4—0,25 |
300 |
600—550 |
5 |
Т |
~0,1 |
400 |
Примечание. П.п. — пластинчатый перлит; Т.п. — тонкопластинчатый перлит; С — сорбит; Г — троостит (0,8% С)
Бейнитное превращение
Выше 500° С скорость диффузии достаточна для того, чтобы образовавшийся феррит содержал равновесное количество углерода. Если увеличить степень переохлаждения, то ниже изгиба С-образной кривой образуется игольчатая структура, называемая игольчатым трооститом или бейнитом.

Рис. 9. Структура эвтектоидной стали в зависимости от температуры распада аустенита. Х100: а—в — перлит; г — сорбит; д—е — троостит
Бейнитное превращение называют также промежуточным превращением, поскольку оно происходит при температурах между перлитным —диффузионным превращением и мартенситным — бездиффузионным (ниже линии Мн на диаграмме рис. 5).

Рис. 10. Микроструктуры, характеризующие процесс распада аустенита при температурах, лежащих ниже изгиба С-образной кривой. Температура превращения 260° С (Бейн). Х500. Время превращения, с: а — 400; б — 500; в — 850; г – 900; д — 2500
Главное отличие бейнита от перлитных структур — содержание углерода в феррите. При высоких температурах углерод успевает выделяться из раствора и феррит содержит около 0,01—0,02% С. При низких температурах (примерно 500—250° С) скорости диффузии малы, углерод не успевает полностью выделиться из раствора, поэтому феррит содержит ~ 0,1% С (400° С) и даже ~ 0,2% С (300° С).
Вблизи границы с областью перлитного превращения образуется «верхний» или перистый бейнит («верхний» перистый троостит). Он состоит из чередующихся не всегда параллельных друг другу коротких пластинок цементита и феррита. При температурах порядка 300° С образуется «нижний» или игольчатый бейнит («нижний» игольчатый троостит), напоминающий по своему строению мартенсит.
При больших увеличениях (электронный микроскоп) можно увидеть, что иглы состоят из мельчайших пластинок цементита и феррита. Размер частичек около 0,09— 0,08 мкм. Частицы цементита ориентированы вдоль октаэдрических плоскостей исходного аустенита. Твердость бейнита около HB500.
На рис. 10 показан процесс превращения переохлажденного аустенита в бейнит.
Свойства бейнита «верхнего» и «нижнего» существенно различаются. В первом случае наблюдается плохое сочетание механических свойств — недостаточная прочность при низких значениях б и ап. Нижний бейнит, образующийся при температурах Мн+(50ч – 110° С), обладает высокой прочностью при хорошем сочетании с пластичностью и вязкостью.
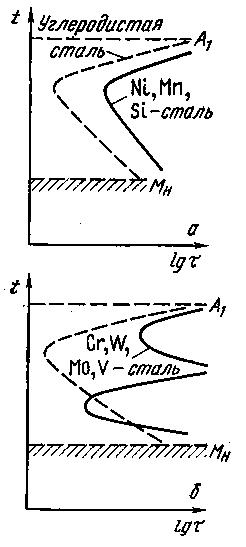
Рис. 11. Диаграммы изотермического превращения аустенита углеродистых и легированных сталей: а — легирующие элементы не образуют карбидов; б — легирующие элементы образуют карбиды
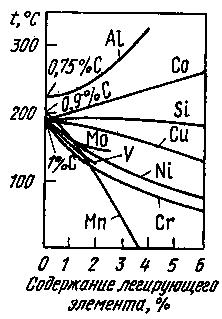
Рис. 12. Зависимость температуры начала мартенситного превращения от содержания легирующих элементов
Для различных марок сталей С-образные диаграммы отличаются расположением линий, т. е. такую диаграмму строят для каждой марки стали.
Легирующие элементы, не образующие карбидов, увеличивают устойчивость переохлажденного аустенита: на диаграмме изотермического превращения таких сталей линии начала и конца превращения сдвигаются вправо (рис. 11, а) по сравнению с углеродистыми сталями (при одинаковом содержании углерода).
По-разному влияют легирующие элементы и на температуру начала мартенситного превращения. Как правило, они понижают температуру Мн (за исключением кобальта и алюминия, рис. 12).
Карбидообразующие элементы оказывают более сложное влияние на изотермическое превращение аустенита. В этом случае возможны две области минимальной устойчивости аустенита, замедляется образование перлитных структур и ускоряется бейнитное превращение (рис. 11, б).
Кроме приведенных на рис. 12 принципиально различных диаграмм, при введении легирующих элементов в сталь возможны и другие, более сложные диаграммы.
Диаграммы изотермического превращения аустенита, построенные в координатах время — температура, имеют большое практическое значение при назначении режимов термической обработки на практике.
Хотя диаграммы построены в результате изучения изотермического превращения, с их помощью можно анализировать процессы фазовых превращений, протекающие при непрерывном охлаждении. На рис. 5 на диаграмму изотермического превращения аустенита нанесены кривые охлаждения, соответствующие различным режимам. Так, например, для получения структуры сорбита следует проводить охлаждение со скоростью υ1, а для получения троостита υ2. Увеличивая скорость охлаждения, можно получить в детали структуру мартенсита.
МАРТЕНСИТНОЕ ПРЕВРАЩЕНИЕ
При больших степенях переохлаждения, например при 230°С для эвтектоидной стали, аустенит находится в неустойчивом состоянии. При этих температурах аллотропическое превращение Feγ→Feα происходит в условиях, когда скорость диффузии углерода очень мала (см. рис. 6). При бездиффузионном превращении Feγ (С) —Feα(C) весь углерод, растворенный в решетке аустенита, остается в решетке феррита. Так как максимальная растворимость углерода в α-железе не превышает 0,02%, а в исходной фазе — аустените — может содержаться до 2,14%С, то образуется пересыщенный твердый раствор, называемый мартенситом.
Мартенсит — это пересыщенный твердый раствор внедрения углерода в Feα. Атомы углерода находятся в междоузлиях: либо в центре оснований тетраэдров, либо посредине их длинных ребер (рис. 13). При образовании мартенсита решетка Feα сильно искажается, превращаясь из кубической в тетрагональную (с/а>1) решетку.
С увеличением содержания углерода степень тетрагональности решетки мартенсита увеличивается (рис. 14): c/a=1 +0,046р, где р — содержание углерода, % (по массе).

Рис. 13. Схема перестройки решетки аустенита в решетку мартенсита (X — атом углерода)

Рис. 14. Изменение степени тетрагональности мартенсита от содержания углерода (по данным разных авторов)
Наименьшая скорость охлаждения, необходимая для образования структуры мартенсита, называется критической скоростью закалки υкр (см. рис. 5).
Механизм мартенситного превращения имеет ряд особенностей, отличающих его от диффузионных превращений. Большой вклад в исследование этого превращения внесли советские ученые С. С. Штейнберг, Г. В. Курдюмов, В. Д. Садовский, А. П. Гуляев.
Как было отмечено ранее, первая основная особенность мартенситного превращения — его бездиффузионный характер. (Под бездиффузионностью превращения следует понимать не отсутствие всяких перемещений атомов, а отсутствие диффузионного перемещения атомов углерода).
Г. В. Курдюмов указывал: «Мартенситное превращение состоит в закономерной перестройке решетки, при которой атомы не обмениваются местами, а лишь смещаются друг относительно друга на расстоянии, не превышающие межатомные». Атомы перемещаются в определенных направлениях единообразно и взаимосвязано, т. е. происходит кооперативное одновременное перемещение атомов, расположенных в одной или нескольких смежных кристаллографических плоскостях.
Необходимая для этого процесса энергия получается за счет разности свободных энергий аустенита и мартенсита.
Рис. 15. Схема строения когерентной границы между кристаллами фаз α и β
Объем образующегося мартенсита больше объема исходного аустенита, поэтому в процессе роста новой фазы возрастает величина упругой энергии до тех пор, пока не будет превзойден предел упругости в переходной зоне. После этого в ней произойдет пластическая деформация (сдвиг), нарушится сопряженность кристаллов, прекратится рост кристалла мартенсита (в этих условиях невозможно кооперативное направленное смещение атомов). Кристаллическая решетка образующегося мартенсита закономерно ориентирована по отношению к решетке аустенита.
В процессе роста мартенситного кристалла на границе между ним и аустенитом имеется непрерывный переход от решетки аустенита к решетке мартенсита, т. е. имеется когерентность (упругая связь) двух решеток (рис. 15). При когерентном росте новой фазы атомы перемещаются только на небольшие близкие расстояния. Это означает, что соседи любого атома в исходной фазе остаются соседями этого же атома в новой фазе. Поверхностная энергия при таком росте очень мала.
В результате — низкое значение энергии активации, а линейная скорость роста новой фазы должна быть очень большой. Это подтверждается экспериментально. Энергия активации такого процесса составляет 1000 кал/г·атом, а скорость роста кристалла мартенсита примерно 1000 м/с. Он образуется практически мгновенно (за 10-7 с).

Рис. 16. Структура мелкоигольчатого (а) и крупноигольчатого (б) мартенсита стали У10. Х500
Итак, вторая особенность мартенситного превращения — ориентированность кристаллов мартенсита.
Ориентированное смещение атомов при мартенситном превращении приводит даже к образованию на полированной поверхности рельефа. Как показано экспериментально А. П. Гуляевым, кристаллы мартенсита имеют форму пластин. В плоскости шлифа видны обычно их сечения, поэтому мартенситная структура под микроскопом выглядит как игольчатая (рис. 16). Образуясь мгновенно (со скоростью взрыва), пластины мартенсита растут либо до границы зерна аустенита, либо до дефекта. Образующиеся следующие мартенситные пластины расположены к первым под углами 60 или 120° и размеры их ограничены участками между первыми пластинами (В этой закономерной ориентировке проявляется принцип структурного соответствия между образующимся мартенситом и исходной фазой — аустенитом). Чем крупнее исходное зерно аустенита, тем крупнее и пластинки мартенсита, т. е. он будет грубоигольчатым (рис. 16,б).
Третья особенность мартенситного превращения— оно происходит только при непрерывном охлаждении, т. е. в интервале температур, начинаясь и заканчиваясь для каждой стали при определенной температуре независимо от скорости охлаждения. Температуру начала мартенситного превращения называют мартенситной точкой и обозначают Мн, а температуру окончания обозначают Мк (см. рис. 5).
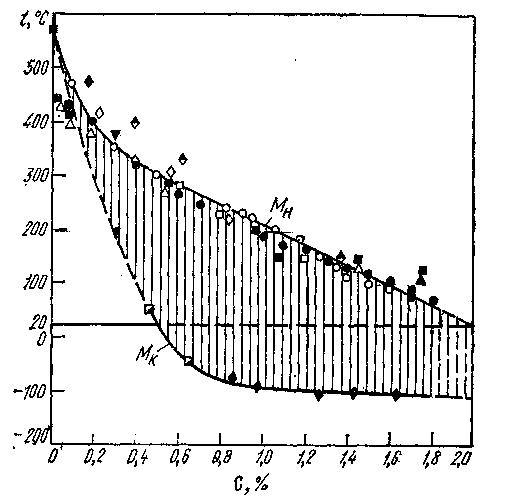
Рис. 17. Зависимость температуры начала (Мн) и конца (Мк) мартенситного превращения от содержания углерода в стали по данным различных авторов
Положение точек Мн и Мк зависит от содержания углерода в стали (рис. 17) и присутствия легирующих элементов и не зависит от скорости охлаждения. Поэтому на С-образной диаграмме Мн и Мк — горизонтальные линии.
Если изотермическую выдержку проводить в интервале Мн—Мк, то, несмотря на имеющееся иногда даже большое количество аустенита, мартенситное превращение прекращается. Причина такого явления пока еще окончательно не выяснена, но практически оно имеет большое значение: если для какой-либо стали Мк находится в области отрицательных температур (например, для стали, содержащей больше 0,6% С), то при комнатной температуре в структуре наряду с мартенситом будет сохраняться какое-то количество аустенита. Такой аустенит называют остаточным А ост.( Небольшое количество остаточного аустенита имеется в сталях и после охлаждения ниже Мк).
Свойства мартенсита обусловлены особенностями его образования. Мартенсит характеризуется очень высокой твердостью (HRC55—65) и хрупкостью. Такая высокая твердость объясняется, во-первых, тем, что при образовании пересыщенного углеродом твердого раствора кристаллическая решетка Feα сильно искажается, в ней создаются большие внутренние напряжения. Во-вторых, вследствие увеличения объема при превращении аустенита в мартенсит возникает фазовый наклеп, что способствует измельчению блочной структуры и росту внутренних напряжений.
В сталях и сплавах на основе железа наблюдают два морфологических типа мартенсита — пластинчатый и реечный.
Пластинчатый мартенсит, который также называют игольчатым, низкотемпературным или двойникованным, образуется в высокоуглеродистых сталях и сплавах железа с большим содержанием никеля. Кристаллы пластинчатого мартенсита имеют форму тонких линзообразных пластин, которые в разрезе на шлифе выглядят иглами. Такая форма мартенсита соответствует минимуму энергии упругих искажений при его образовании в аустенитной матрице и аналогична форме механических двойников.
Реечный мартенсит, называемый также массивным, высокотемпературным, недвойникованным, образуется в закаленных малоуглеродистых и среднеуглеродистых сталях, а также в большинстве конструкционных легированных сталях. Кристаллы этого мартенсита имеют форму тонких реек, вытянутых в одном направлении (отсюда название этой формы мартенсита). Рейки параллельны и образуют плотный пакет, внутри которого они разделены мало- или высокоугловыми границами.
Огромная скорость образования пластин мартенсита объясняется когерентностью и упругим сопряжением двух решеток — образующегося мартенсита и исходной фазы, аустенита. Происходит «скользящее» движение, обусловленное бездиффузионным, кооперативным перемещением атомов на расстояния, меньшие межатомных. Так же характерной чертой кинетики мартенситного превращения является его автокаталитичность, напоминающая цепные реакции. На скорость роста кристаллов мартенсита оказывает большое влияние плотность дислокаций и механизм их движения — скольжение вместе с границей или переползание. Повышенная плотность дефектов (дислокаций, двойниковых прослоек) оказывает дополнительное влияние и на фазовый наклеп, наблюдающийся при превращении аустенита в мартенсит (объем мартенсита больше объема аустенита). Кроме того, повышенная плотность дислокаций, особенно их появление на границе фаз, может привести даже к частичному нарушению когерентности.
Мартенситное превращение происходит не только у сталей, оно обнаружено у многих металлов и сплавов, испытывающих аллотропические или полиморфные превращения при быстром значительном переохлаждении высокотемпературных модификаций. Особенностью мартенситного превращения в сталях является его необратимость.
Превращение аустенита в мартенсит — бездиффузионный процесс. Превращение мартенсита в аустенит при нагреве происходит диффузионно.
ПРЕВРАЩЕНИЯ В ЗАКАЛЕННОЙ СТАЛИ ПРИ НАГРЕВЕ
Мартенсит закалки — неравновесная (метастабильная) структура, сохраняющаяся ввиду малой подвижности атомов при низких температурах. При закалке в изделиях всегда возникают большие внутренние напряжения в результате объемных изменений. Для получения более равновесного состояния после закалки изделия подвергают отпуску, нагревая до температур ниже Ас1. Изучая процессы, происходящие в закаленной стали при нагреве, наиболее часто пользуются прибором — дилатометром. В прибор помещают два одинаковых по размерам образца из одной и той же стали. Один из образцов находится в отожженном, другой — в закаленном состояниях. При нагреве до температур ниже Ас1 в отожженном образце никаких превращений не происходит, его размеры изменяются только за счет теплового расширения, а в закаленном образце совершаются и структурные превращения, сопровождающиеся изменениями объема. Прибор дифференциальный, он показывает только те изменения размеров, которые происходят в закаленном образце при нагреве за счет структурных превращений. В результате получается кривая, подобная приведенной на рис. 18.
Различают четыре основных превращения, происходящих при нагреве закаленной стали. В результате изменения состава стали и времени выдержки при отпуске происходит смещение температурных интервалов этих превращений, однако сущность процессов остается неизменной.
Первое превращение происходит при температуре до 200 °С. При низких температурах — до 100 °С — скорость диффузии очень мала. Так, при 0 °С время, в течение которого половина объема мартенсита будет участвовать в начальной стадии распада, это сотни лет. При 20 °С на этот же процесс потребуется около шести лет, а при 100° С всего лишь 50 мин. Поэтому до 80 °С за время эксперимента практически никаких изменений в закаленном образце не наблюдается.
В интервале температур от 80 до 150—200 °С происходит так называемый «двухфазный» или «гетерогенный» распад мартенсита.

Рис. 18. Дилатометрическая кривая отпуска закаленной (а) и отожженной (б) углеродистой стали (1,2% С)
При этих температурах в отдельных участках исходного мартенсита выделяются тончайшие пластины карбида. Толщина таких пластинок составляет несколько атомных слоев, длина — несколько сот ангстрем. Решетка образовавшегося карбида когерентна решетке мартенсита, т. е. на их границе имеется общий слой атомов. Состав образовавшихся пластинок карбида окончательно не установлен. Известно, что он метастабилен, имеет гексагональную решетку. Его обозначают как ε-карбид или карбид FexC.
В непосредственной близости от образовавшихся пластинок карбида твердый раствор обедняется углеродом, уменьшается тетрагональность мартенсита. Но при этих температурах ввиду малой скорости диффузии концентрация не успевает выравниваться, поэтому в одном зерне могут сосуществовать два твердых раствора с одинаковым типом решетки, но с разной концентрацией углерода. Поэтому такой распад мартенсита и называется «двухфазным».
Кристаллы образовавшихся карбидов при этих температурах не растут. Процесс развивается за счет выделения новых частиц карбида в тех участках мартенсита, которые имеют исходную концентрацию углерода.
В результате первого превращения при отпуске получается так называемый отпущенный или кубический мартенсит.
Отпущенный мартенсит — это гетерогенная смесь пересыщенного углеродом α-раствора неоднородной концентрации (от исходной до незначительно большей, чем в феррите) и не обособленных частиц карбида. С уменьшением тетрагональности мартенсита уменьшается объем всего образца (см. рис. 18).
Второе превращение происходит в интервале температур 200—300 °С. В этом интервале остаточный аустенит превращается в отпущенный мартенсит. Такое превращение возможно вследствие того, что с уменьшением тетрагональности мартенсита уменьшаются сжимающие напряжения, действующие на остаточный аустенит.
Превращение остаточного аустенита сопровождается некоторым увеличением объема. Одновременно происходит уменьшение тетрагональности мартенсита и при температурах ближе к 300 °С начинаются обособление и рост частичек карбида. Внутренние напряжения уменьшаются.
Третье превращение происходит в интервале 300— 400 °С. Скорость диффузии при этих температурах заметно увеличивается, весь избыточный углерод постепенно выделяется из решетки Feα, карбидные частички полностью обособляются, приобретают строение Fe3C и начинают расти. Образующаяся высокодисперсная смесь феррита и цементита называется трооститом отпуска.
Четвертое превращение — при нагреве выше 400° С. При этой температуре происходят постепенный рост частичек карбида и их коагуляция. При 550—600 °С размер частичек равен 0,1—0,2 мкм. Такая структура называется сорбитом отпуска.
В отличие от сорбита, полученного при охлаждении аустенита, цементит в сорбите отпуска имеет округлую форму. При нагреве закаленной стали до 650—700 °С получают перлит отпуска или глобулярный перлит с размером частиц —0,3—0,4 мкм.
Малая диффузионная подвижность атомов легирующих элементов оказывает существенное влияние на процессы, протекающие в закаленных сталях при отпуске (только никель и марганец не оказывают заметного влияния на эти процессы).
На первую стадию распада мартенсита (до 150 °С), когда происходит «двухфазный» распад, влияние легирующих элементов незначительно. Выделяющийся карбид железа имеет такую же концентрацию легирующих элементов, как и исходный мартенсит, и также существует когерентная связь.
При дальнейшем нагреве процесс протекает медленнее, чем в углеродистых сталях, и поэтому легированные стали сохраняют структуру отпущенного мартенсита до более высоких температур (иногда до 400— 500 °С).
Легирование оказывает существенное влияние на второе превращение остаточного аустенита в отпущенный мартенсит. Температура этого превращения повышается. Так как в легированных сталях, как правило, сохраняется значительное количество остаточного аустенита, то превращение последнего в отпущенный мартенсит способствует сохранению твердости до более высоких температур.
Третье и четвертое превращения в легированных сталях также происходят при более высоких температурах. Поэтому после одинаковых по температуре нагревов закаленных сталей легированные стали имеют более высокую твердость и прочность.
Карбидная фаза при отпуске претерпевает специфические превращения. С повышением температуры увеличивается подвижность атомов легирующих элементов, благодаря чему становится возможным их перераспределение между цементитом и ферритом. Концентрация легирующих элементов в цементите увеличивается и при определенных значениях решетка цементита перестраивается в решетку того специального карбида, который может находиться в данной стали в равновесии с ферритом. (При сохранении легированного мартенсита до высоких температур возможно выделение специального карбида и непосредственно из мартенсита). Образовавшиеся дисперсные карбиды могут значительно увеличивать твердость.
Таким образом, выше были рассмотрены четыре основных превращения в стали, протекающие при нагреве и охлаждении: П→А, А→П, А→М и М→П. В основе всех превращений лежит стремление системы к минимуму свободной энергии. На рис. 19 приведена схема изменения свободной энергии основных структур с изменением температуры. Из этой схемы видно, что превращения М→А и П→М невозможны.
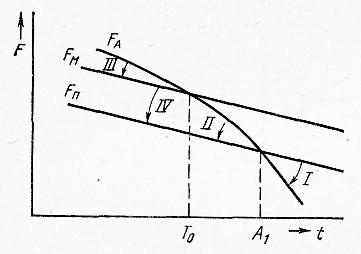
Рис. 19. Изменение свободной энергии аустенита (FА), мартенсита (FM) и перлита (FП) с изменением температуры; То — температура метастабильного равновесия А—М
Практика закалки и отпуска стали
Закалка углеродистых сплавов производится в целях повышения их механических свойств: твердости, предела прочности, упругости и износостойкости.
Процесс закалки состоит из следующих этапов:
а) нагревания изделия до температуры закалки;
б) выдержки изделия в течение определенного времени при за данной температуре;
в) охлаждения изделия с нужной скоростью.
Температура нагрева под закалку должна обеспечить в стали аустенитную структуру. На рис. 20 показан интервал температур для закалки сталей в зависимости от содержания углерода. Если доэвтектоидную сталь нагревать до аустенито-ферритной структуры, то закалка будет неполная, а твердость стали — невысокая (в структуре будет феррит). Заэвтектоидные стали рекомендуется нагревать до аустенито-цементитной структуры, т. е. производить неполную закалку, так как цементит в структуре увеличит твердость металла.
В случае нагрева выше рекомендованного интервала возможен перегрев стали и снижение ее свойств. Для контроля температуры в печи применяются пирометры. При отсутствии пирометров температуру ориентировочно можно определять по цветам каления. Цвет каления стали в зависимости от температуры, °С, изменяется следующим образом:
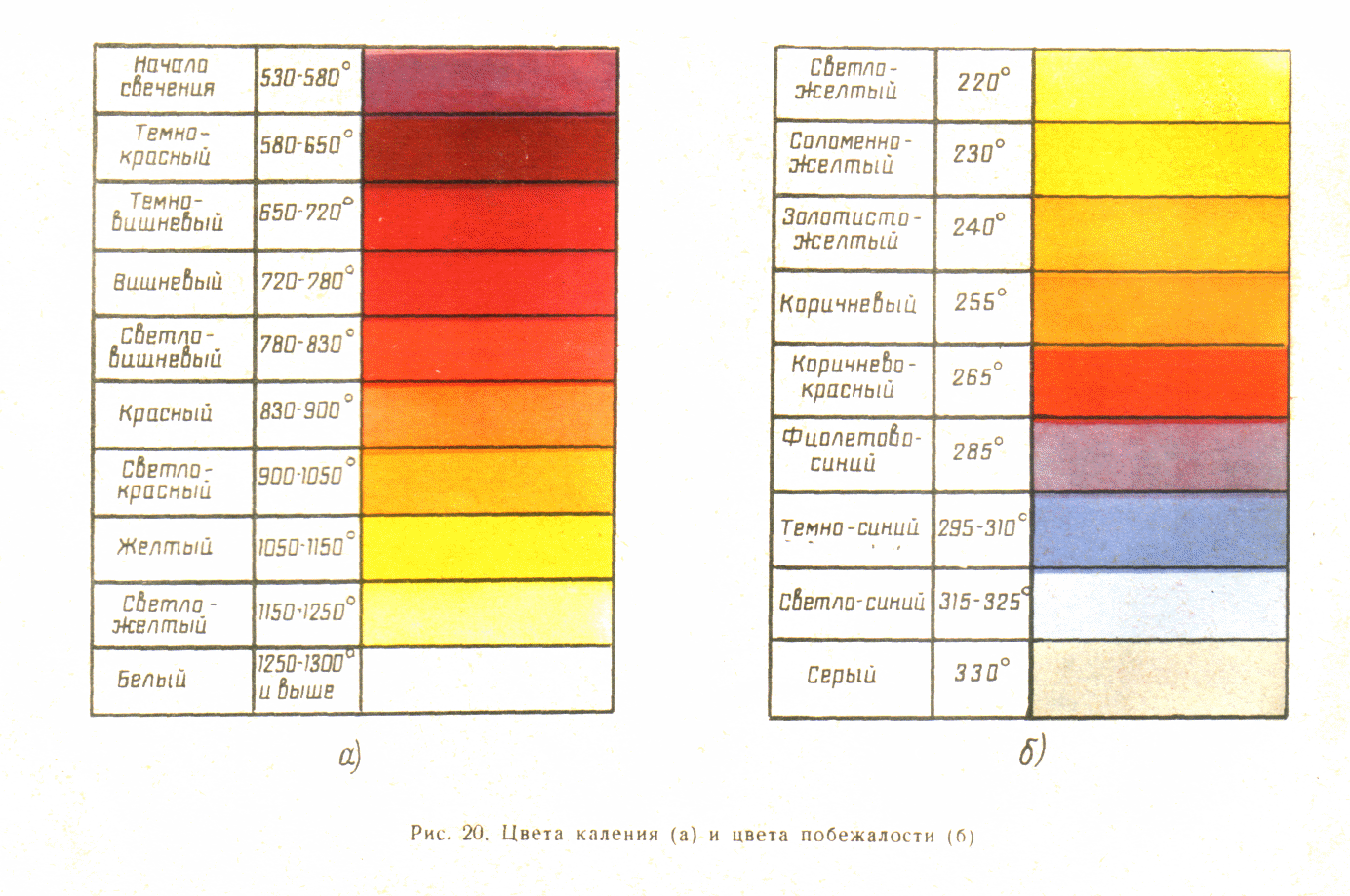
Рис. 20. Цвета каления (а) и побежалости (б)
Время выдержки стали при температуре закалки должно быть достаточным для того, чтобы обеспечить образование однородного аустенита по всему сечению.
Время нагрева и выдержки изделий из углеродистой стали зависит от температуры нагрева, нагревающей среды и формы изделий.
В табл. 2 Приведены условия нагрева стали при термической обработке в лабораторных электрических печах.
Таблица 2
Условия нагрева стали при термообработке
Температура нагрева, °С |
Время выдержки, мин, на 1 мм толщины (диаметра) образца в зависимости от его формы |
Температура нагрева, °С
|
Время выдержки, мин, на 1 мм толщины (диаметра) образца в зависимости от его формы |
||||
цилиндр |
квадрат |
пластина |
цилиндр |
квадрат |
пластина |
||
500 |
2,5 |
3,8 |
5,0 |
800 |
1,0 |
1,5 |
2,0 |
600 |
2,0 |
3,0 |
4,0 |
900 |
0,8 |
1,2 |
1,6 |
700 |
1.5 |
2,2 |
3,0 |
1000 |
0,4 |
0,6 |
0,8 |
Скорость охлаждения при закалке оказывает влияние на структуру и свойства стали. Для получения структуры мартенсита в углеродистых сталях необходимо охлаждение со скоростью 400—600 °С в секунду в интервале 600—400 °С. Снижение скорости приводит к появлению структуры троостита (200 °С в 1 сек) и сорбита (около 100 °С в 1 сек).
При закалке важным является медленное охлаждение стали в интервале температур, при которых происходит превращение аустенита в мартенсит (300 °С), так как непосредственный переход аустенита в мартенсит не требует больших скоростей охлаждения и, кроме того, если превращение аустенита в мартенсит будет происходить при медленном охлаждении, то изменение его объема по сечению протекает равномерно и тем самым снижаются внутренние напряжения и деформации.
В табл. 3 приведены скорости охлаждения, получаемые в некоторых наиболее распространенных охлаждающих средах.
Важное значение при закалке имеет способ погружения изделия в охлаждающую жидкость (рис. 21).
Неправильное погружение приводит к, неравномерному распределению в металле внутренних напряжений, что может вызвать коробление изделий, а также недостаточную твердость его отдельных частей. Изделия, имеющие несквозные отверстия, следует погружать в охлаждающую жидкость закрытой стороной, чтобы воздух и пар могли выйти в отверстия, а вода проникла в него. Детали, имеющие вогнутую поверхность, нельзя погружать вогнутой поверхностью вниз, так как образующаяся паровая рубашка не даст этому месту закалиться. При закалке изделий, имеющих неодинаковые сечения, сначала погружают в жидкость наиболее массивные их части. Изделия плоской формы следует погружать в охлаждающую среду узкой стороной.
Отпуск стали проводится после закалки, чтобы уменьшить хрупкость, ослабить напряжения и получить требуемые механические свойства.
Таблица 3 Скорость охлаждения стали в охлаждающих средах
Закалочная среда |
Скорость охлаждения в интервале температур, град/сек |
|
650-550 °С |
300—200 °С |
|
Вода при температуре, °С: |
|
|
18 |
600 |
270 |
28 |
500 |
270 |
50 |
100 |
270 |
74 |
30 |
200 |
10%-ный раствор в воде при 18° С: |
|
|
едкого натра |
1200 |
300 |
поваренной соли |
1100 |
300 |
соды |
800 |
270 |
Эмульсия масла в воде |
70 |
200 |
Масло: |
|
|
минеральное машинное |
150 |
30 |
трансформаторное |
120 |
25 |
Спокойный воздух |
18 |
|
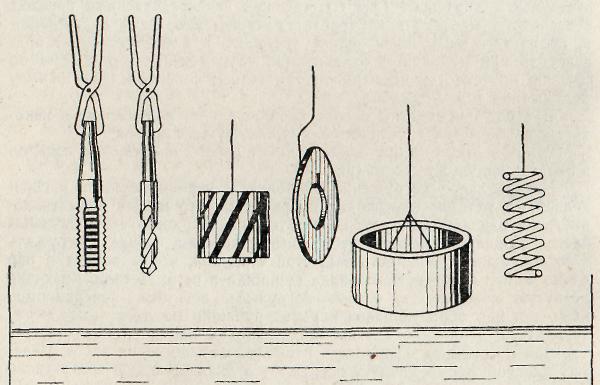
Рис. 21 Способ погружения изделия в охлаждающую жидкость
Температура нагрева стали зависит от вида отпуска.
Время выдержки зависит от размеров изделия и температуры нагрева (табл. 2).
Большое применение имеет отпуск по цветам побежалости, которые зависят от температуры нагрева, °С:
Метастабильные структуры
К метастабильным (неустойчивым) структурам относятся мартенсит, троостит, сорбит и аустенит.
Мартенсит имеет игольчатое строение. Размеры игл зависят от температуры, закалки и от размеров зерен аустенита, из которых они образовались, и их количества. Лучшими механическими свойствами обладает мелкоигольчатый мартенсит. В металломикроскопе мартенсит наблюдается в виде игл, расположенных под углом 60, 90 и 120° друг к другу.
Троостит является продуктом распада аустенита при закалке, а при среднем отпуске — продуктом распада мартенсита. Троостит травится реактивами интенсивнее мартенсита, поэтому под микроскопом он выглядит темным.
Сорбит образуется при высоком отпуске закаленной на мартенсит стали. Сорбит виден под микроскопом в виде светлых участков — зерен цементита в феррите.
Аустенит наблюдается в виде светлых полей или светлого фона. Остаточный аустенит бывает только в высокоуглеродистых и некоторых легированных сталях после закалки.
Вопросы для самопроверки:
От чего зависят свойства сплава?
Назовите основные виды термической обработки?
Как различают разновидности отжига I рода?
Что понимают под отжигом II рода?
Дайте определение закалки?
Дайте определение отпуска?
Что понимают под химико-термической обработкой?
Что понимают под термомеханической обработкой?
Что лежит в основе всех превращений, которые совершаются в стали при нагреве?
Поясните влияние скорости нагрева на продолжительность превращения?
Как различают величину зерна наследственного и действительного?
Какие происходят превращения в стали при охлаждении?
Как можно легко обнаружить превращение аустенита?
Какие превращения происходят в закаленной стали?
Какие применяются виды закалок?
Какой интервал температур применяется при закалке?
Какие применяются виды отпусков?
Какие интервалы температур применяются при отпуске?
Литература:
1. Иваней А.А. Электронный конспект лекций.
2.Технология металлов и материаловедение: Учебник для вузов и техникумов /Под ред. Л.Ф. Усовой – Производственное издание. М.: Металлургия, 1987. – с.106-123;
3. Гуляев А.П. Металловедение: Учеб. пособие для вузов. – 6-е изд., перераб. и доп. – М.: Металлургия, 1986. – 542 с.89-141
4. Материаловедение и технология металлов: Учеб. для студентов машиностроит. спец. вузов/ Г.П. Фетисов, М.Г. Карпман, В.М. Матюнин и др.; Под ред. Г.П. Фетисова – 4-е изд., испр. – М.: Высш. шк. 2006. – 862с.
Форма отчета
Практическая работа №2.
«Термическая обработка сталей»
По таблице заданий найти свой вариант.
Изучить теоретические сведения термической обработки сталей.
Определить режим закалки образца стали в соответствии с заданием.
Определить режим низкого, среднего и высокого отпуска образцов стали в соответствии с заданием.
Указать твердость образцов после закалки.
Указать твердость образцов после отпуска.
Охарактеризовать структуру стали после выполненных различных видов термической обработки.
Сделать анализ влияния термической обработки стали на ее механические свойства.
Протокол испытаний
№ образца |
Марка стали |
Закалка |
Твердость HRC |
Отпуск |
Твердость HRC |
||||
температура нагрева , °С |
выдержка, мин |
охлаждающая среда |
температура нагрева , °С |
выдержка, мин |
охлаждающая среда |
||||
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица заданий
№ задания |
Марка стали |
Требуемая структура |
1 |
У 12 |
мартенсит |
2 |
12Х18Н10Б |
троостит |
3 |
12Х18Н10Т |
сорбит |
4 |
30ХГС |
перлит |
5 |
14Г2АФ |
бейнит |
6 |
Р6М5 |
перлит+цементит |
7 |
03Н18К9М5Т |
феррит+перлит |
8 |
95Х18 |
мартенсит |
9 |
08Х13 |
троостит |
10 |
ШХ15 |
сорбит |
11 |
36Х2Н2МФА |
перлит |
12 |
25Н25М4Г1 |
бейнит |
13 |
Р18 |
мартенсит |
14 |
12Х1МФ |
троостит |
15 |
30Х9Н8М4Г2С2 |
сорбит |
16 |
40ХН2МА |
перлит |
17 |
04Х11Н9М2Д2ТЮ |
бейнит |
18 |
30ХГСН2А |
мартенсит |
19 |
ШХ15СГ |
троостит |
20 |
09Х14Н19В2БР |
сорбит |
21 |
65С2ВА |
перлит |
22 |
60С2Н2А |
бейнит |
23 |
30Х10Г10 |
мартенсит |
24 |
40Х13 |
троостит |
25 |
09Х15Н8Ю |
сорбит |
Практическая работа № 3
«Изучение технологии литейного производства»
Цель работы - ознакомиться с технологиями литейного производства, подобрать технологический процесс изготовления фасонных деталей.
Задачи:
Ознакомиться с модельной оснасткой и способами изготовления литейной формы по разъёмной и неразъёмной моделям.
Ознакомиться с технологиями литейного производства.
Подобрать и описать технологический процесс изготовления фасонных деталей в соответствии с заданием.
Краткие теоретические сведения
Чугун имеет высокие литейные, антикоррозионные и антифрикционные свойства, достаточно высокую прочность и невысокую стоимость. В машиностроении широко распространены чугуны всех четырех модификаций (серый, высокопрочный, ковкий и легированный).
Стальные отливки обладают более высокими прочностью и вязкостью, чем отливки из чугуна. Но по литейным свойствам сталь уступает чугуну (она имеет большую усадку, низкую жидкотекучесть и т.д.). Особое место по износостойкости занимает аустенитная высокомарганцовистая износостойкая сталь марки Г13Л. Она обладает настолько высокой износостойкостью, что почти не поддается обработке резанием, ее обычно применяют только в отливках.
Для изготовления фасонных отливок используют обе главные разновидности медных сплавов — латуни и бронзы. Для коррозионно-стойких деталей наиболее широко применяют латуни марок ЛА67-2Д ЛАЖ60-1-1- и ЛК80-3.
Литейными сплавами на основе алюминия являются сплавы его с кремнием и другими элементами, именуемые силуминами.
Широко применяют отливки из магниевых сплавов. Механические свойства магниевых сплавов значительно повышаются после термообработки.
Основными видами брака литья являются:
1) газовые, осадочные, шлаковые и песчаные раковины; 2) рыхлота и пористость; 3) недостаточное заполнение литейной формы металлом; 4) горячие и холодные трещины; 5) коробление; 6) несоответствие микроструктуры, химического состава, механических свойств металла отливок требованиям ГОСТов и технических условий.
Эти дефекты отливок выявляются различными методами контроля. Контроль размеров отливок позволяет своевременно предупредить массовый брак из-за износа или коробления модели и стержневых ящиков. Механические свойства и микроструктура контролируются испытаниями и исследованием отдельно изготовленных или отлитых совместно с заготовкой образцов.
Внутренние дефекты отливок выявляются методами радиографической или ультразвуковой дефектоскопии.
Отливки, которые по условию работы должны выдерживать повышенное давление жидкости или газа, подвергают гидравлическим или ревматическим испытаниям при давлениях, несколько превышающих рабочее давление.
Основными способами исправления дефектов отливок являются правка, заварка, пропитка.
Литейным производством называется технологический процесс изготовления фасонных деталей или заготовок путём заливки расплавленного металла в форму. После затвердевания металл (расплав) принимает очертания формы и называется отливкой. Отливки могут быть деталями или заготовками, которые в дальнейшем подвергаются обработке.
Технология производства отливок слагается из следующих основных процессов:
изготовление моделей и стержневых ящиков;
приготовление формовочной и стержневой смеси;
изготовление форм и стержней;
сушка форм и стержней
приготовление расплава и заливка формы;
выбивки отливок из форм и стержней из отливок.
Изготовление литейной формы – трудоёмкая и наиболее сложная операция, от которой в значительной мере зависит качество отливок. В единичном и мелкосерийном производстве формы изготавливаются вручную. Для каждого наименования отливки изготавливается своя литейная форма.
Различают следующие виды форм.
Разовые – служат для получения только одной отливки, после чего они разрушаются. Для их изготовления используют песчано-глинистые смеси, в состав которых входит кварцевый песок (85 – 90 %), огнеупорная глина (8 – 14 %), вода и связующие (жидкое стекло, искусственные смолы и др.).
Разовые формы могут быть сырыми, сухими, поверхностно – высушиваемыми и химически твердеющими.
Полупостоянные – изготавливаются из смеси с высоким содержанием глины и высокоогнеупорных материалов. Их применяют чаще всего при производстве крупных и тяжёлых отливок простой конфигурации.
При производстве отливок полость формы сохраняет свои очертания, получая лишь незначительные повреждения. Эти формы допускают многократную (до нескольких десятков раз) заливку металла с мелким ремонтом рабочей поверхности после получения каждой отливки.
Постоянные изготавливаются преимущественно из металла. Такие формы обеспечивают получение в одной форме нескольких тысяч, а иногда десятков тысяч отливок. Металлические формы – кокили – применяют в серийном производстве, а также при специальных способах литья.
Модели
У литейной формы имеется рабочая часть – полость, в которой застывающий расплавленный металл приобретает очертания и размеры литой заготовки. Для получения в форме такой полости необходимо иметь модель. Конструкция модели должна обеспечить лёгкость выемки её из формы, поверхность модели должна быть прочной, не изменяться в размерах, противостоять влиянию влаги формовочной смеси.
Для чугунных отливок модели окрашивают в красный цвет, для стальных – в серый или синий, для цветных сплавов – в жёлтый. Стержневые знаки на модели окрашивают в чёрный цвет.
Модели изготавливают из дерева, цемента, гипса, пластмасс, полистирола, сплавов.
Модели бывают неразъёмные, разъёмные и с отъёмными частями. Их размеры превышают размеры деталей на величину усадки, которая составляет: для стали – 2 %; для чугунов – 1 %; для цветных сплавов – 1,2 - 1,5 %.
Неразъёмные модели – служат для производства несложных отливок, формовка которых может осуществляться в одной из половин формы.
Разъёмные модели – применяются при производстве отливок более сложной конфигурации, состоящих из двух и более частей. Для точного соединения половин модели на одной из них выполнены шипы, а на другой – углубления. Отверстия в литых заготовках образуются с помощью стержней, которые вставляются в форму при её сборке. Конфигурация стержня соответствует конфигурации отверстия, полости.
Стержни изготавливаются в стержневых ящиках из стержневой смеси, которая от формовочной смеси отличается повышенной прочностью, газопроницаемостью, противопригарностью. Для удержания стержня в нужном положении, во время заливки формы металлом, его вставляют в специальные углубления в форме, которые образуются выступами на модели, так называемыми знаками.
Литниковая система
Литниковой системой называют каналы в форме, предназначенные для подачи в форму расплавленного металла. Шлакоуловитель литниковой системы исключает возможность попадать неметаллическим включениям в тело отливки и служит для задержания шлака.
Литниковая система состоит из литниковой чаши 1, стояка 2, шлакоуловителя 3 и питателей 4 (рисунок 1). Литниковая чаша является сосудом, в который расплавленный металл поступает из разливочного ковша. Она служит для предотвращения разбрызгивания и смягчения удара струи металла. Стояк – вертикальный канал в верхней полуформе, соединяющий литниковую чашу со шлакоуловителем. Шлакоуловитель – горизонтальный, трапецевидного сечения канал, обычно выполняемый в верхней полуформе. Питатель – канал, служащий для непосредственного подвода металла к полости формы. Наличие большого количества питателей облегчает заполнение сложной формы металлом.
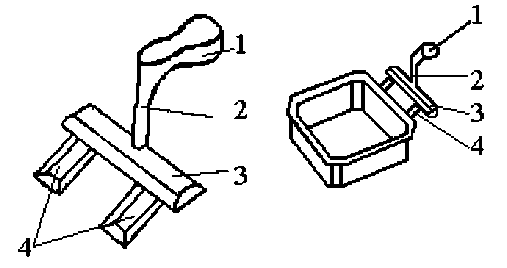
Литье в кокиль и литье под давлением относятся к специальным видам литья. Отливки, получаемые этими методами, характеризуются повышенной точностью размеров, пониженной шероховатостью поверхности, уменьшением припусков на механическую обработку, возможностью получения деталей, не нуждающихся в механической обработке. При этом специальные виды литья дают возможность обойтись без многих побочных операций (таких, как приготовление земляной и стержневой смесей), без пыльной выбивки и пескоструйной очистки.
Литье в кокиль. Кокиль — это металлическая форма многократного использования, заливаемая жидким металлом. Отливки, получаемые в кокиле, отличаются большой точностью размеров и высокой чистотой поверхности. Кокиль изготавливается из чугуна, стали или алюминиевых сплавов.
Достоинство литья в кокиль заключается в первую очередь в возможности обеспечить высокую производительность литейного процесса. Кокильное литье легко механизировать и автоматизировать.
Распространение этого способа литья несколько ограничивается высокой стоимостью изготовления кокилей и сложностью получения тонкостенных отливок вследствие значительной теплопроводности кокилей и быстрой кристаллизации металла.
Для получения отливок с очень тонкими стенками (до 0,8 мм), повышенной чистотой поверхности, точностью размеров и высокого качества применяется литье под давлением. При этом способе литья металлическая пресс-форма соединяется литниковой системой с камерой прессования, в которой ходит поршень (рисунок 2,а). Поршень энергично, с большой скоростью и силой давит на металл, который устремляется в пресс-форму и заполняет все его самые тонкие щели (рисунок 2,б). Давление может достигать сотен или нескольких тысяч атмосфер.
Литье под давлением применяют в массовом производстве для получения отливок из цветных металлов и сплавов, реже чугуна и стали(рисунок 2,в).
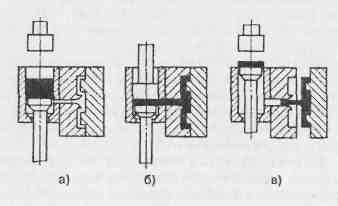
Рис.2 Литье под давлением.
Центробежное литье представляет собой заливку металла в литейную форму, которая вращается с определенной скоростью. При этом скорость вращения изменяется в течение всего времени кристаллизации. Под действием центробежной силы металл прижимается к стенкам формы, в результате получается деталь повышенной прочности, так как газы и шлак вытесняются во внутренние полости отливок и удаляются.
Оси вращения формы могут быть горизонтальными (рисунок 3,а) или вертикальными (рисунок 3,б). Центрифугированным называется такое центробежное литье, при котором ось вращения формы не совпадает с осью отливки.
Центробежное литье применяют при изготовлении труб, цилиндровых втулок, гильз и поршневых колец двигателей, колес, шкивов, орудийных стволов и др.
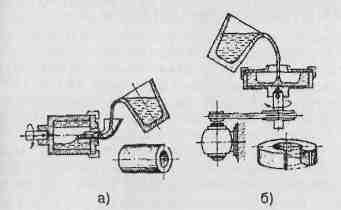
Рис.3 Центробежное литье.
При непрерывном и полунепрерывном литье в металлическую форму — кристаллизатор без дна — жидкий металл заливается с одной стороны, отдавая тепло холодным стенкам формы, а с другой стороны этой формы затвердевший металл извлекается и остывает на воздухе. Форма кристаллизатора может быть различной: круглой, прямоугольной, в форме кольца. Отливка представляет собой круглый пруток, прямоугольную штангу, трубу или длинный брус произвольного профиля.
Если изделие извлекается тянущими валками при условии непрерывной подачи жидкого металла, оно может оказаться бесконечно длинным. В этом случае процесс называется непрерывным.
Если после изготовления изделия заданной длины механизмы извлечения отливки возвращаются в исходное состояние и закрывают форму для дальнейшего заполнения жидким металлом, процесс называется полунепрерывным.
Стенки кристаллизатора при таких видах литья представляют собой тонкие металлические пластины или трубы, охлаждаемые при помощи воды.
При электрошлаковом литье приготовление расплава совмещается с заполнением литейной формы во времени и пространстве путем переплава электродов необходимого химического состава. При этом виде литья источником тепла является шлаковая ванна, которая нагревается при прохождении через нее электрического тока.
Процесс плавки можно разделить на следующие этапы:
в водоохлаждаемый медный кристаллизатор заливают расплавленный шлак особого состава;
электрический ток подводят к нижней части кристаллизатора и к переплавляемым электродам;
шлаковая ванна нагревается по действием тока до 1700 оС, и концы электродов плавятся;
капли расплавленного металла проходят через шлак, в котором очищаются от вредных примесей;
металл собирается в зоне кристаллизации, образуя под шлаком металлическую ванну;
6) ванна металла затвердевает в нижней части вследствие отвода тепла через стенки кристаллизатора;
7) отливку извлекают из кристаллизатора.
Электрошлаковое литье применяют для изготовления прокатных валков, кокилей, для производства коленчатых валов мощных дизелей, задвижек паропроводов, корпусов атомных реакторов и др.
При литье вакуумным всасыванием расплав под действием разряжения, создаваемого в полости, заполняет ее и затвердевает, образовав отливку. Скорость заполнения формы расплавом можно регулировать изменением разности атмосферного давления и давления внутри формы. Толщина стенок отливки при таком способе литья составляет 1—1,5 мм, также исключается попадание воздуха, повышаются точность, герметичность и механические свойства отливки.
Сущность литья выжиманием состоит в том, что для улучшения заполнения формы и качества отливки процесс происходит так, чтобы геометрические размеры полости формы изделия изменялись при заполнении расплавом и затвердевании. При этом:
уменьшаются потери расплавом тепла;
заполняются формы тонкостенных крупногабаритных отливок;
осуществляется компенсация усадки отливки путем уменьшения ее объема при кристаллизации.
Полученный металл имеет хорошую структуру, механические свойства.
Таблица 1 - Классы точности размеров и масс и ряды припусков на механическую обработку отливок для различных способов литья (по ГОСТ 26645-85)
Способ литья
|
Наибольший габаритный размер отливки, мм
|
Металлы и сплавы |
||
цветные с температурой плавления ниже 700 °С |
цветные с температурой плавления выше 700 °С |
ковкий, высокопрочный и легированный чугуны, стали |
||
1 |
2 |
3 |
4 |
5 |
Под давлением в металлические формы
|
До 100 |
3т-5 I |
3-6 I |
4-7 I |
Св. 100 |
3-6 I |
4-7т I |
5т-7 I |
|
В керамические формы и по выполняемым и выжигаемым моделям
|
До 100 |
3-6 I |
4-7т I-2 |
5т-7 I-2 |
Св. 100 |
4-7 I-2 |
5т-7 I-2 |
5-8 I-2 |
|
В кокиль и под низким давлением в металлические формы с песчаными стержнями и без них, литье в песчаные формы, отверждаемые в контакте с оснасткой
|
До 100 |
4-9 I-2 |
5т-10 I-3 |
5-11т I-3 |
Св. 100 до 630 |
5т-10 I-3 |
5-11т I-3 |
6-11 2-4 |
|
Cв. 630 |
5-11т I-3 |
6-11 2-4 |
7т-12 2-5 |
|
В песчаные формы, отверждаемые вне контакта с оснасткой, центробежное, сварные и сухие песчано-глинистые формы
|
До 630 |
6-11 2-4 |
7т-12 2-4 |
7-13т 2-5 |
Св. 630 до 4000 |
7-12 2 - 4 |
8-13т 3 - 5 |
9т-13 3 - 6 |
|
Св. 4000 |
8-13т 3 - 5 |
9т-13 3 - 6 |
9-14 4 - 6 |
|
Примечание - В числителе указаны классы точности размеров и масс, в знаменателе – ряды припусков. Меньшие их значения относятся к простым отливкам и условиям; большие значения – к сложным, мелкосерийного производства; Средние значения – к отливкам средней сложности и условиям серийного производства. Классы точности масс следует принимать соответствующими классам точности отливок. |
||||
Литейные уклоны на отливке облегчают извлечение моделей из формы без разрушения ее, и для свободного удаления стержня из стержневого ящика. Уклоны выполняют в направлении извлечения модели из формы. На чертеже формовочные уклоны указывают, как и припуски на механическую обработку, - красным карандашом или тонкими линиями. Величина формовочных уклонов регламентируется ГОСТ 3212-92 в зависимости от высоты боковых поверхностей (таблица 2).
Таблица 2 - Формовочные уклоны
Измеряемая высота вертикальной поверхности, мм |
Углы наклона моделей (не более) |
|
металлических |
деревянных |
|
До 20 |
1°30´ |
3º |
21-50 |
1º |
1º30´ |
51-100 |
0º45´ |
1º |
101-201 |
0º30´ |
0º45´ |
201-300 |
0º30´ |
0º30´ |
301-500 |
0º20´ |
0º30´ |
501-800 |
0º20´ |
0º20´ |
Напуск - служит для упрощения изготовления отливки. Так отверстия в отливке диаметром 20-30 мм в условиях массового и серийного производства и диаметром до 50 мм в условиях единичного производства можно не делать, так как их целесообразнее просверлить в процессе механической обработки. В этом случае на чертеже отливки отверстия зачеркивают тонкими линиями.
Галтели - закругления внутреннего угла отливки в модели (рисунок 18.1 в) для получения плавного перехода в сопрягаемых стенках. С помощью галтелей исключается осыпание формовочной смеси в углах модели при ее извлечении из формы. Нормативные материалы рекомендуют пользоваться нормальным рядов радиусов: 1, 2, 3, 5, 10, 15, 20, 25, 30, 40 мм. Радиусы галтелей составляют 1/5-1/3 средней арифметической толщины сопряженных стенок отливки.
Плоскость разъема формы и модели обозначают на чертежах буквами РМ и двумя стрелками с буквами В (верх) и Н (низ).
Литейный стержень - элемент литейной формы для образования отверстий, полости или иного сложного контура в отливке. Стержни бывают вертикальные и горизонтальные в зависимости от их положения при установке в форму. Конфигурацию и размеры стержней регламентирует ГОСТ 3606-80. Для правильной установки и крепления стержней в форме служат знаковые части стержня, которые у горизонтальных стержней делают прямыми, а у вертикальных с уклоном для удобства сборки формы. Длину знаков определяют в зависимости от длины стержня (таблицы 3 и 4).
Высоту верхнего знака принимают равной 60 % от высоты нижнего.
На чертеже стержни в разрезе штрихуют по контуру. Если стержней несколько, для каждого стержня применяют свою, отличающуюся от других штриховку.
Таблица 3 - Высота нижних вертикальных знаков стержня (мм)
Диаметр стержня |
Длина стержня, мм |
|||
до 150 |
151-500 |
501-1000 |
1001 и выше |
|
До 100 |
20-30 |
50-70 |
100-120 |
|
101-400 |
20-40 |
40-60 |
70-100 |
140-190 |
401-1000 |
40-50 |
40-50 |
60-100 |
110-180 |
1001 и выше |
60-100 |
60-110 |
60-110 |
80-150 |
Таблица 4 - Длина горизонтальных стержневых знаков (мм)
Длина стержня, мм |
Длина стержня, мм |
|||||
до 50 |
51-150 |
151-300 |
301-500 |
501-750 |
750-1000 |
|
До 25 |
15 |
25 |
40 |
- |
- |
- |
25-50 |
20 |
30 |
45 |
60 |
- |
- |
51-100 |
25 |
35 |
50 |
70 |
90 |
110 |
101-200 |
30 |
40 |
55 |
80 |
100 |
120 |
201-300 |
- |
50 |
80 |
90 |
110 |
130 |
Литейная модель – приспособление для получения в форме отпечатка, соответствующая конфигурации внешней поверхности отливки.
Чертеж модели составляют по наружным очертаниям детали с технологическими указаниями, причем все размеры увеличивают на коэффициент линейной усадки. В среднем коэффициент линейной усадки принимается: для серого чугуна – 1 %; для стали – 2 %; для цветных сплавов – 1 - 1,5 %.
Конструкция отливки должна иметь плавные переходы от больших сечений к меньшим (рёбра жесткости, окна) с целью равномерного охлаждения и предотвращения внутренних напряжений и трещин.
С целью повышения точности отливок и упрощения моделей и процесса формовки необходимо стремиться к неразъемным моделям.
Сборкой называется процесс соединения отдельных частей формы в одно целое и подготовка формы к заливке. Сборка формы состоит из следующих операций: установка и крепление стержней, установка верхней опоки, крепление опок, установка литниковой чаши, контроль правильности сборки. Форма в сборе должна быть показана на чертеже так, чтобы было видно положение стержней и литниковых каналов, выпоров, прибылей и способов крепления опок.
На рисунке 4 показана форма в сборе, а на рисунке 5 – готовая отливка.
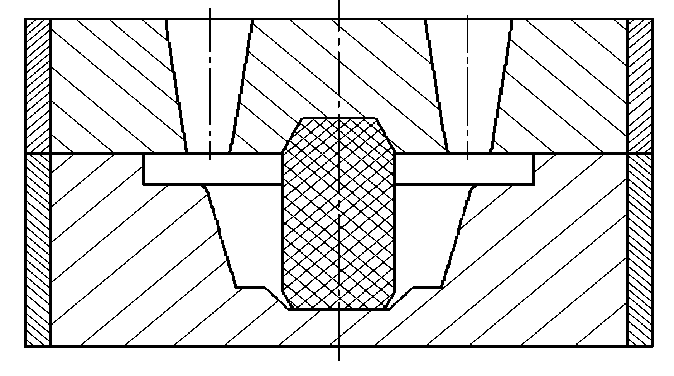
Рисунок 4 – Литейная форма в сборе
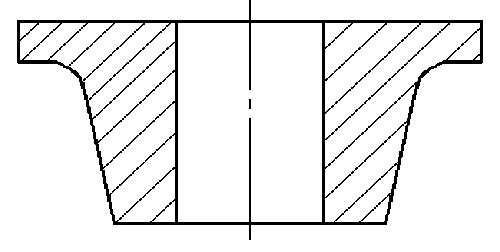
Рисунок 5 – Эскиз отливки
Вопросы для самопроверки:
Назначение модели, стержня, стержневого ящика.
Назначение и устройство литниковой системы.
Из каких материалов изготавливают разовые, полупостоянные и постоянные формы?
Какие виды ручной формовки существуют?
Какие бывают виды форм?
Что относится к модельному комплекту?
Назначение модели и требования, предъявляемые к ее изготовлению.
Назначение стержней и стержневых знаков.
В каких случаях назначаются припуски на механическую обработку и их определения?
Назначение формовочных уклонов и их определение.
Назначение галтелей и их определение.
Как учитывается усадка металла при изготовлении моделей?
Чем размеры модели отличаются от размеров отливки?
Чем размеры отливки отличаются от размеров конструкторского чертежа?
Литература:
1. Иваней А.А. Электронный конспект лекций.
2.Технология металлов и материаловедение: Учебник для вузов и техникумов /Под ред. Л.Ф. Усовой – Производственное издание. М.: Металлургия, 1987. – с.106-123;
3. Гуляев А.П. Металловедение: Учеб. пособие для вузов. – 6-е изд., перераб. и доп. – М.: Металлургия, 1986. – 542 с.89-141
4. Материаловедение и технология металлов: Учеб. для студентов машиностроит. спец. вузов/ Г.П. Фетисов, М.Г. Карпман, В.М. Матюнин и др.; Под ред. Г.П. Фетисова – 4-е изд., испр. – М.: Высш. шк. 2006. – 862с.
Форма отчета
Практическая работа №3.
«Изучение технологии литейного производства»
По таблице заданий найти свой вариант.
Ознакомиться с модельной оснасткой и способами изготовления литейной формы по разъёмной и неразъёмной моделям.
Ознакомиться с технологиями литейного производства.
Подобрать и описать технологический процесс изготовления фасонных деталей.
Таблица заданий.
№ варианта |
Вид материала |
Наибольший габаритный размер отливки, мм |
1 |
МЛ3 |
До 100 |
2 |
АЛ2 |
Св. 100 |
3 |
БрОЦСН3-7-5-1 |
До 100 |
4 |
ЛА67-2Д |
Св. 100 |
5 |
КЧ 330-8 |
До 100 |
6 |
ЛАЖ60-1-1Л |
Св. 100 до 630 |
7 |
ВЧ 1200-4 |
Cв. 630 |
8 |
КЧ 370-12 |
До 630 |
9 |
БрАМц10-2 |
Св. 630 до 4000 |
10 |
ВЧ 450-5 |
Св. 4000 |
11 |
КЧ 630-2 |
До 100 |
12 |
БрАЖ9-4Л |
Св. 100 |
13 |
БрОЦС3-12-5 |
До 100 |
14 |
БрАЖН10-4-4Л |
Св. 100 |
15 |
КЧ 370-12 |
До 100 |
16 |
МЛ2 |
Св. 100 до 630 |
17 |
ЛАЖ60-1-1 |
Cв. 630 |
18 |
ВЧ 450-5 |
До 630 |
19 |
БрОЦС3-12-5 |
Св. 630 до 4000 |
20 |
ВЧ 600-2 |
Св. 4000 |
21 |
АЛ4 |
До 100 |
22 |
ВЧ 600-2 |
Св. 100 |
23 |
ВЧ 1200-4 |
До 100 |
24 |
Г13Л |
Св. 100 |
25 |
БрОФ6,5-0,15 |
До 100 |
