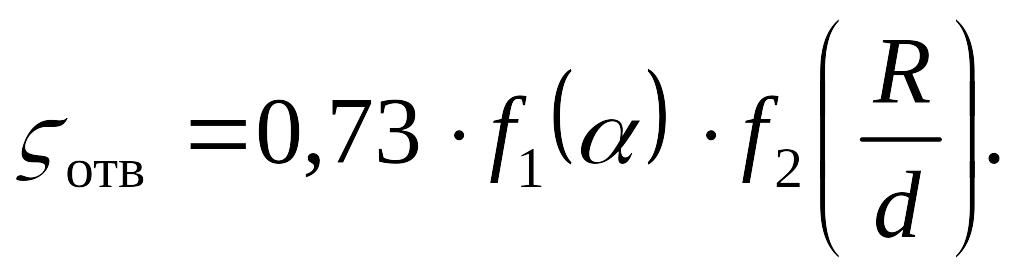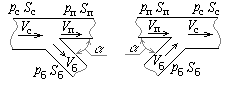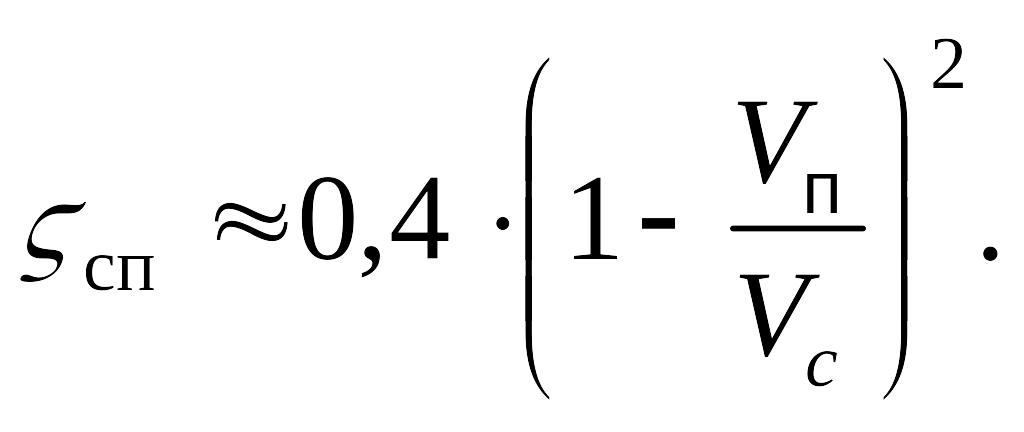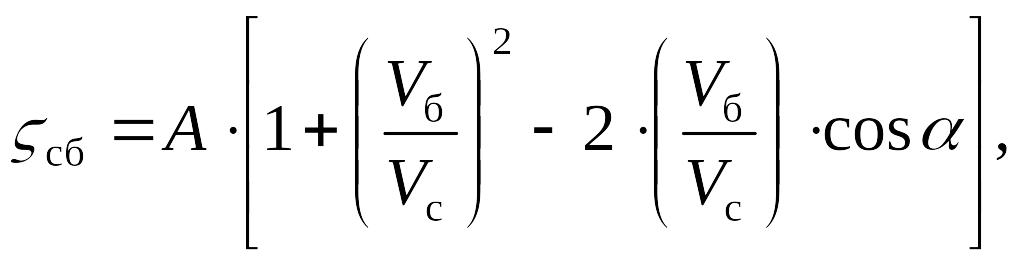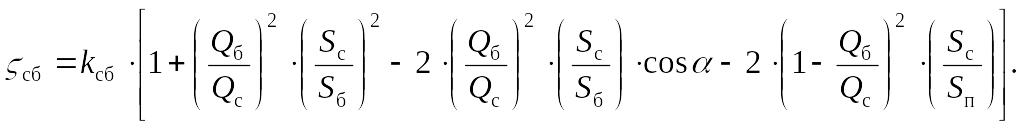- •Формула Шухова
- •Определение пластовых давлений
- •2.2.2 Определение забойного давления по давлению на устье при неподвижном столбе газа (барометрическая формула)
- •Определение забойного давления в работающей скважине
- •Определение забойного давления при движении газа по двухступенчатой колонне фонтанных труб
- •Определение забойного давления в газоводяных и газоконденсатных скважинах
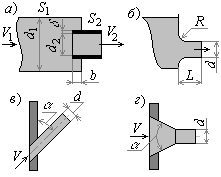
Вход потока в трубу |
||||||||||||||||||||||||||||||
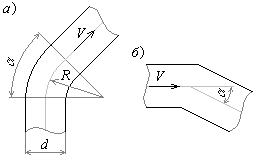
Рис. 1. Вход потока в трубу 1. Прямой вход при наличии сужения (рис. 1, а) без учета неравномерности профилей скорости:
Коэффициент определяют по приближенной формуле
2. Прямой вход при наличии коллектора радиусом R и торцевой стенки (рис.1, б) (Reавт = 104).
3. Косой вход в трубу без скругления (рис. 1, в) (Reавт = 104):
4. Прямой вход через конический коллектор (рис. 1, г). При = 180˚ независимо от отношения h/D, = 0,5.
При = 40–60˚ имеет наименьшее значение:
|
||||||||||||||||||||||||||||||
Изменение площади поперечного сечения потока без изменения направления течения |
||||||||||||||||||||||||||||||
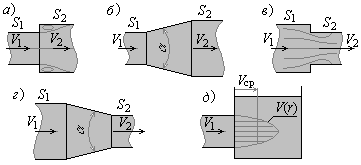
Рис. 2. Изменение площади сечения потока без изменения направления 1. Внезапное расширение (рис. 2, а). при Re > 104
а при Re < 104
2. Плавное расширение в диффузорах (рис. 2, б). Коэффициент потери давления в диффузоре
3. Внезапное сужение (рис. 2, в).
4. Плавное сужение (конфузор) (рис. 2, г).
Для углов сужения конических диффузоров (40–80)˚ с = 0,1–0,2. Минимальными значениями коэффициента потери давления обладают конические конфузоры с углом при вершине 15–55˚; для них к = 0,04–0,05.
5. Выход потока из трубопровода (рис. 2, д):
|
||||||||||||||||||||||||||||||
Изменение направления потока |
||||||||||||||||||||||||||||||
Изменение направления течения в трубопроводах осуществляется в отводах и коленах (рис. 3).
Рис. 3. Изменение направления течения: а – отвод; б – колено
Для стандартных отводов постоянного сечения с углом = 90˚ коэффициент потери давления можно принимать равным:
Коэффициент потери давления в простом колене при Re > 2*105 (рис. 3, б) можно принимать равным нижеприведенным значениям в зависимости от угла поворота.
|
Узлы деления и слияния потоков |
|||||||||||||
Рис. 4. Узлы деления и слияния потоков Коэффициент потери давления слияния сб оценивают по уравнению
Коэффициент потери давления на ответвление сб оценивают по уравнению
где А = 1,0 при Vб/Vс < 0,8 и А = 0,9 при Vб/Vс > 0,8.
Коэффициент потерь давления на проход в магистральном канале при слиянии потоков определяют из выражения
Коэффициент потерь давления потока, направленного из ответвления в магистральный канал, отнесенный к скорости в сечении после слияния, определяют по формуле
Значения kсб находятся в пределах 0,6–1,0. Для прямых тройников ( = 90˚) kсб находят в зависимости от отношения площадей Sб/Sс.
|
|||||||||||||
Коэффициенты истечения из насадков Значения коэффициентов местных потерь давления для наиболее характерных групп элементов
|
|
||||||||||||
Формула Шухова
Если на входе в газопровод температура газа Т1 отличается от
наружной температуры Тнар, то течение газа будет неизотермическим.
Полагая dx —> 0, получим
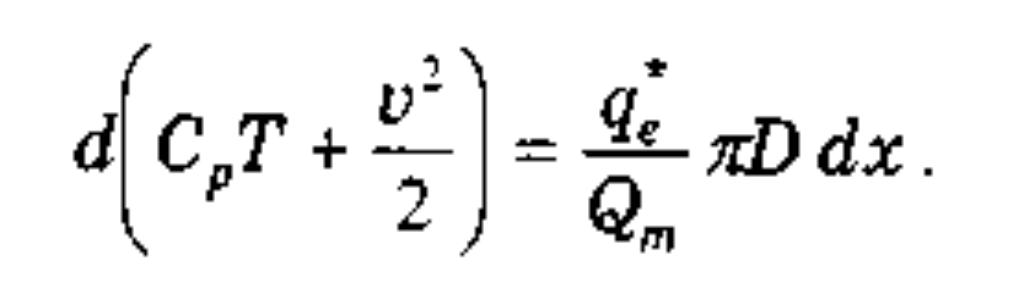
q*e - тепло, подведенное в единицу времени через единицу площади поверхности - периметр газопровода можно представить в виде
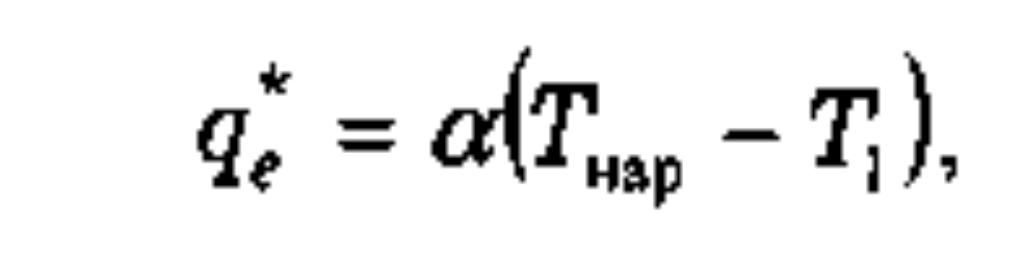
где
а
-
коэффициент теплопередачи![]() температура газа в газопроводе.
температура газа в газопроводе.
Пренебрегая изменением скоростного напора по длине газопровода имеем
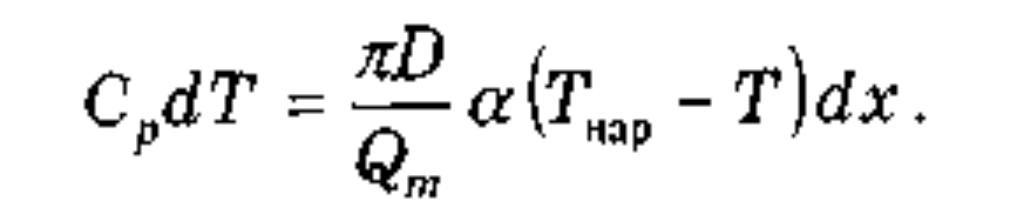
Интегрируя соотношение, при условии, что в начале трубопровода при
х = 0 Т = Т1 получим
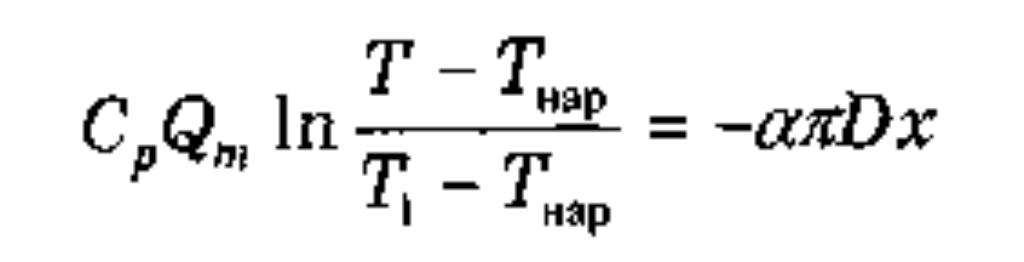
или
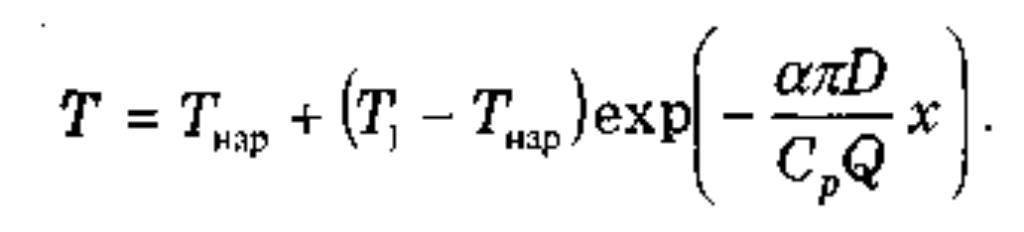
формула В.Г. Шухова оказывается вполне точной для идеального газа, движущегося в трубе с дозвуковой скоростью.
Отсюда следует, что Т --> Тнар при х --> ∞. Значение х = х1, при котором температура газа в трубопроводе отличается от Тнар меньше, чем на 1%, и определяется по формуле в виде
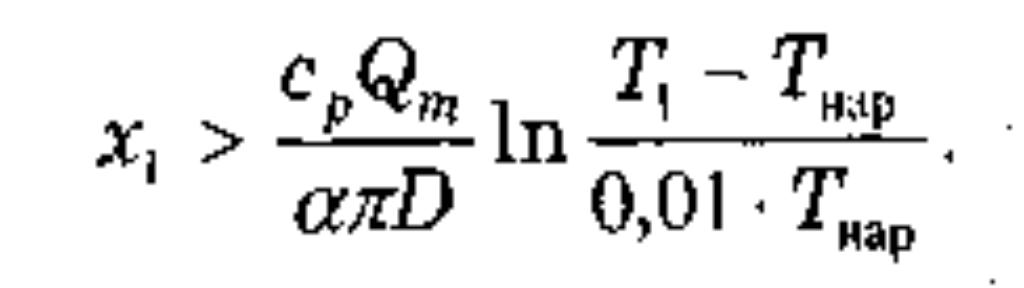
Оценки, выполненные по этой формуле, показывают, что величина x достаточно мала, то есть течение в магистральном газопроводе можно считать изотермическим.
Законы сохранения массы и энергии при движении газа. Расчет газопровода
Уравнение состояния газа (уравнение Клайперона)
![]()
![]()
Массовый расход
Qм = υ1 ρ1 s1 = υ2 ρ2 s2 = … …=υi ρi si = CONST
закон сохранения энергии (политропный процесс) для единицы веса газа:
Z1
![]()
![]()
![]() =Z2
=Z2![]()
![]()
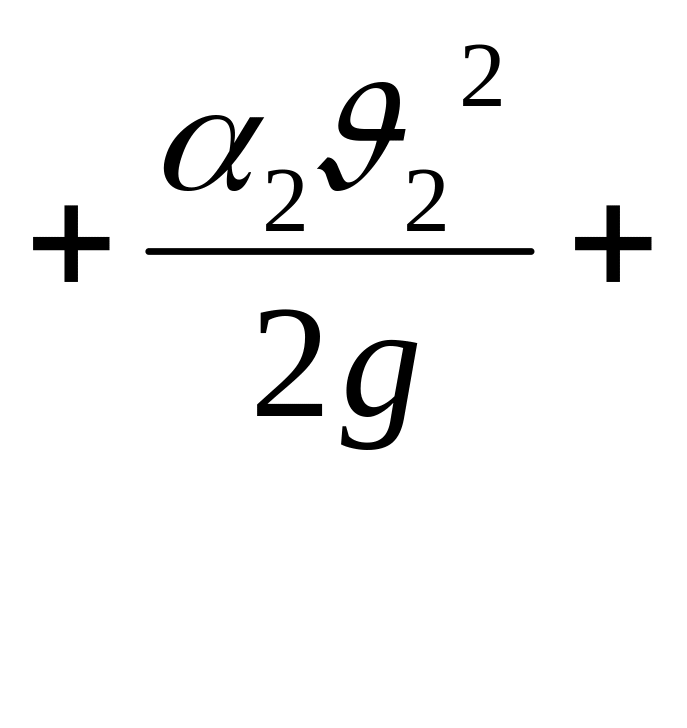 h1-2
h1-2
Z – удельная потенциальная энергия положения;
![]() -
удельная потенциальная энергия давления;
-
удельная потенциальная энергия давления;
P / (ρg (n-1)) = RT / (g (n-1)) – внутренняя энергия;
![]() -
удельная кинетическая энергия;
-
удельная кинетическая энергия;
ɑ - коэффициент Кориолиса (корректив кинетической энергии)
при ламинарном режиме ɑ = 2
при турбулентном режиме ɑ = 1,1 – 1,2, для практических расчетов при турбулентном режиме принимают ɑ = 1
h1-2 = hдл + hм – суммарные потери энергии (потери по длине и местные
потери);
n – показатель политропы.
Уравнение Бернулли при изотермическом течении газа:
Z1
=Z2
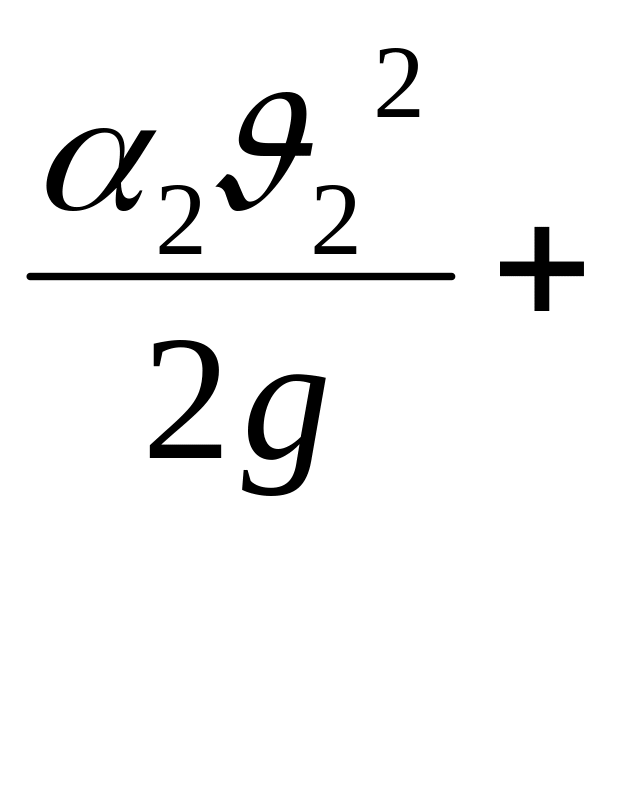 h1-2
h1-2
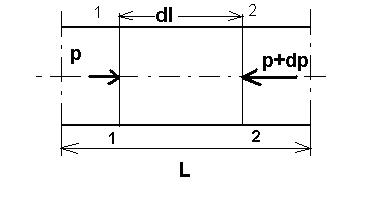
Схема к выводу расчетных зависимостей при движении газа
Уравнение Бернулли для выделенного элемента:
![]()
![]() dhдл
dhдл
-dР = ρ g dhдл = ρ λ (dl/d) υ2/2
Коэффициент трения
λ=ƒ(Re, ∆/d)
при
ламинарном режиме
![]()
![]()
при
турбулентном режиме
![]()
λ = 0,11 (68/Re+ ∆/d )0.25
![]() =
4 Qρ
/
=
4 Qρ
/
![]() d μ
=4
Qм/
π
d µ=
CONST
d μ
=4
Qм/
π
d µ=
CONST
ρυ2 =ρQ2 м /ρs2 = Q2 м /s2 = Q2 м Р1 /ρ1Р s2
Р /ρ = Р1 /ρ1 = RT = CONST
-dР = ρ λ (dl/d) υ2/2 = λ (dl/d) (Q2мР1 / 2 ρ1Р s2)
Определение давления при известном расходе
Р1 - Р2 = λ (l/d5) (16 Q2мР1 / ρ1π2)
Определение массового расхода при известных давлениях Р1 и Р2
Qм = ((Р21 – Р22) ρ1π2 d5 / 16 λ l Р1 )0,5
Физические и теплофизические свойства природных газов.
Вязкость
Для расчета динамической вязкости природных газов m следует использовать соотношения Тодоса, которые в зависимости от величины приведённой плотности rпр=r/rкр имеют вид:
При rпр> 2

При 0,3<rпр£ 2
![]() (в1)
(в1)
При rпр£ 0,3
![]()
![]()
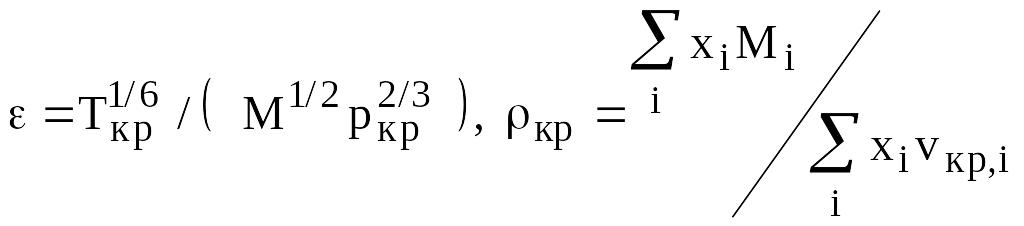
где
Коэффициент динамической вязкости m0 при атмосферном давлении в зависимости от температуры рассчитывается по зависимостям:
при Тпр³ 1,5
![]() (в2)
(в2)
при Тпр< 1,5
![]()
В формулах (2), (3): ркр - 0,1МПа, m - мкПа×с, Т - оК.
Для расчета вязкости в зависимости от температуры при атмосферном давлении можно использовать и следующие зависимости:
![]() (в.3)
(в.3)
или
![]() ,
(в3.1)
,
(в3.1)
где t- 0С, h-м Па .с.
Погрешность расчетов по формулам (3.3), (3.3..1) при 12 £ Мсм£100 и 283 £ Т£477 К не превышает 5%.
Порядок расчета m:
![]()
При содержании азота в природном газе более 5% следует учитывать его влияние на вязкость газа по правилу аддитивности:
![]() ,
(в.4)
,
(в.4)
где уа - молярная доля азота в составе смеси; mа, mу - коэффициенты динамической вязкости азота и углеводородной части, соответственно.
Коэффициент динамической вязкости углеводородного конденсата при различных давлениях и температурах приближенно можно рассчитать по эмпирической формуле Муталибова, Шубина и Абдурахманова:
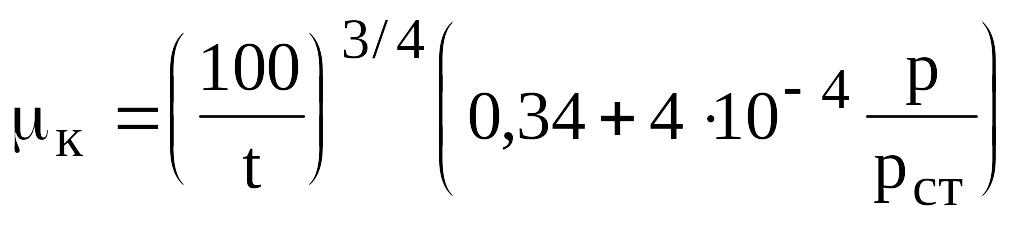 ,
(в.5)
,
(в.5)
при 0,1 £ р£50,0 МПа и 30 £ t£200 0C.
Теплоёмкость
При изобарическом процессе зависимость молярной теплоёмкости углеводородных компонентов природных газов при атмосферном давлении и различной температуре приближенно можно выразить следующим уравнением
![]() ,
(в.6)
,
(в.6)
где t - температура, 0С;
Mi - молекулярная масса углеводорода, являющегося компонентом природного газа (от метана до гексана включительно).
Погрешность в интервале температур от -40 до +1200С: для СН4 - С5Н12 – не более5%, для С6Н14-С7Н16 – не превышает 10%.
При изобарическом процессе молярная теплоёмкость неуглеводородных компонентов природных газов (азота, углекислого газа, сероводорода) равна примерно половине теплоёмкости углеводорода с одинаковой молекулярной массой при одной и той же температуре, которая рассчитывается по уравнению (7). Теплоёмкость смесей рассчитывается по правилу аддитивности
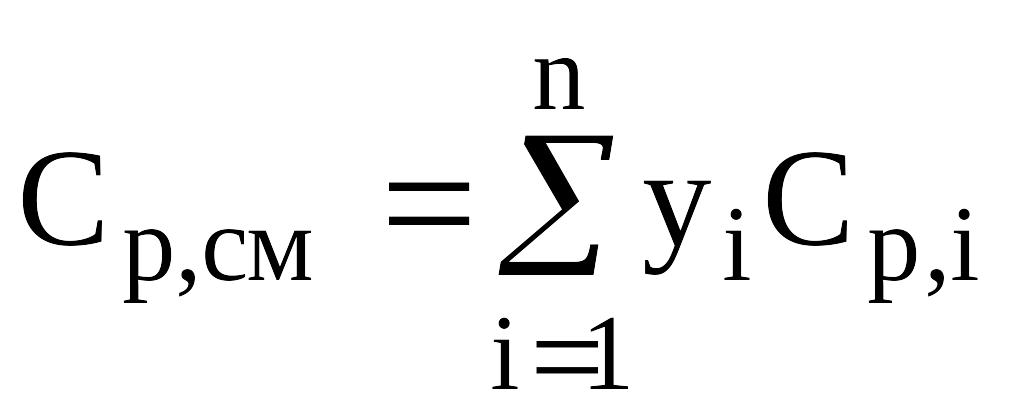 ,
(в7)
,
(в7)
где yi - молярная доля i-го компонента в смеси;
Ср,i - молярная теплоёмкость i-го компонента.
Молярная теплоёмкость природных газов зависит от давления и температуры
![]() ,
(в8)
,
(в8)
где DСр(р,t) - изотермическая поправка теплоёмкости на давление.
Поправка находится из графика по приведённым значениям давления и температуры или аналитически из уравнения состояния, например, Пенга-Робинсона
 (в9)
(в9)
Здесь:
 (в10)
(в10)
Для приближенных расчетов при 0,02 £ рпр £ 4 и 1,3 £ Тпр £ 2,5 поправку DСр(р,t) можно рассчитать с погрешностью, не превышающей 10% по формуле
 [кДж/(кмоль
К)].
(в11)
[кДж/(кмоль
К)].
(в11)
При изобарическом процессе молярную теплоёмкость природного газа можно рассчитать и по формуле, предложенной Гухманом и Нагаревой
 [кДж/(кмоль
К)]. (в12)
[кДж/(кмоль
К)]. (в12)
Для расчета температуры и мощности в процессах адиабатного расширения и сжатия природных газов необходимо строго математически определить значения температурного КТ и объёмного КV коэффициентов адиабаты. Последнее возможно при определении частных производных коэффициента сверхсжимаемости соотношениями (1.30) и подстановкой их в зависимости:
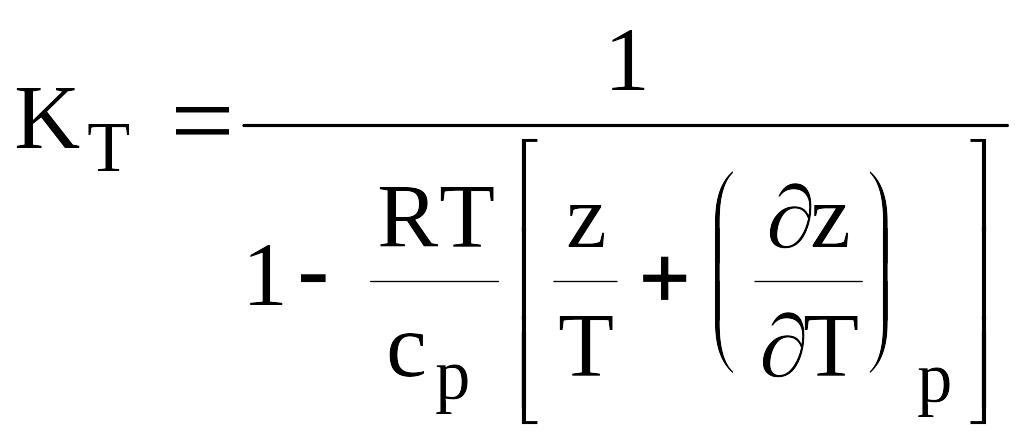 ,
(в13)
,
(в13)
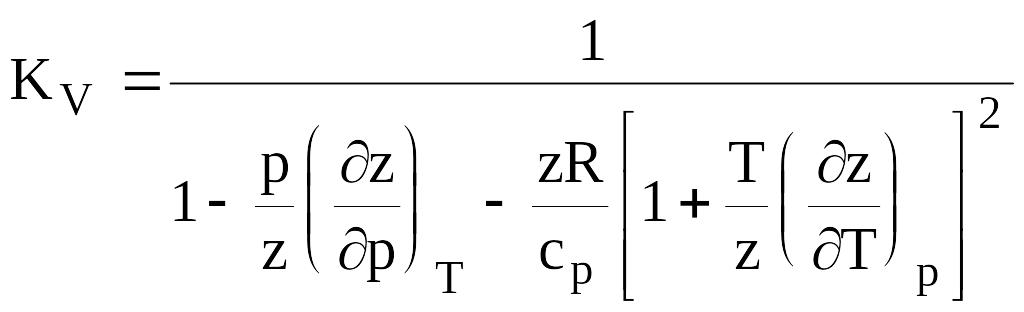 ,
(в14)
,
(в14)
Коэффициент адиабаты природного газа находится по формуле
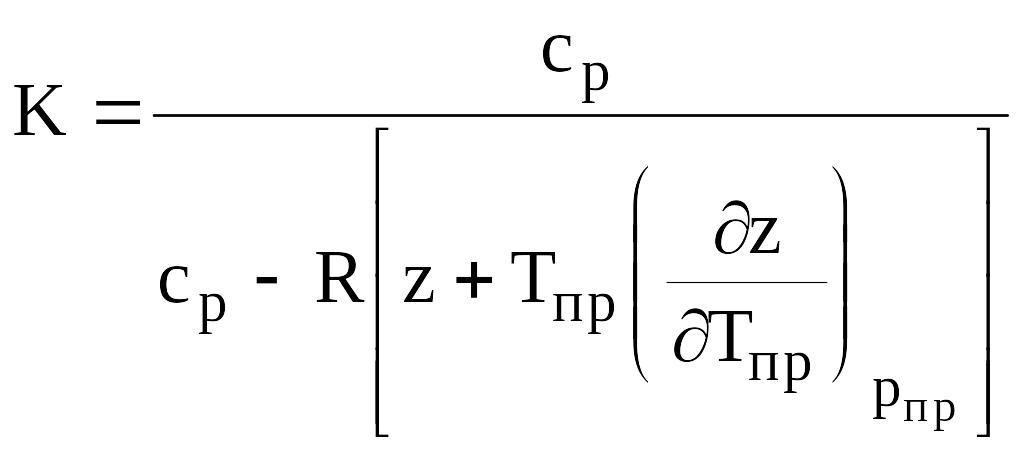 (в15)
(в15)
или используя аппроксимацию вычитаемого в знаменателе
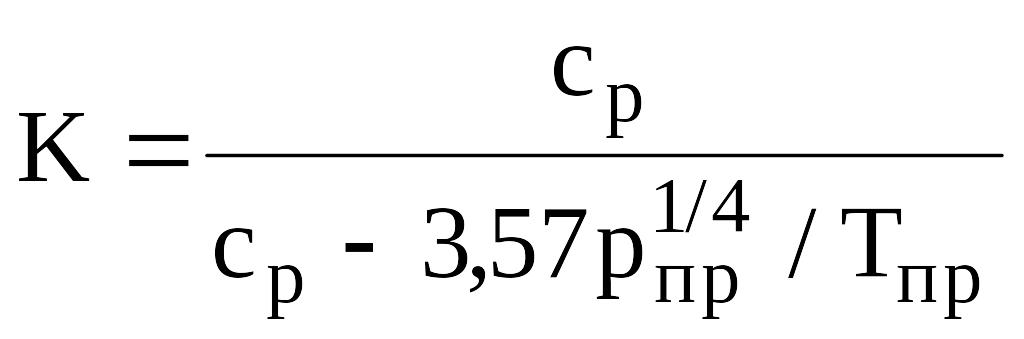 (в16)
(в16)
Если в расчетах необходимо иметь не молярную, а массовую теплоёмкость, то следует значение молярной теплоёмкости разделить на молекулярную массу газа Мi , т.е на массу киломоля i-го компонента, кг/моль.
Дросселирование газа. Коэффициент Джоуля-Томсона
Изменение температуры при снижении давления на 1 атм называется коэффициентом Джоуля - Томсона. Этот коэффициент изменяется в широких пределах и может быть положительным (охлаждение) или отрицательным (нагревание). Для природных газов коэффициент Джоуля - Томсона определяется из выражения
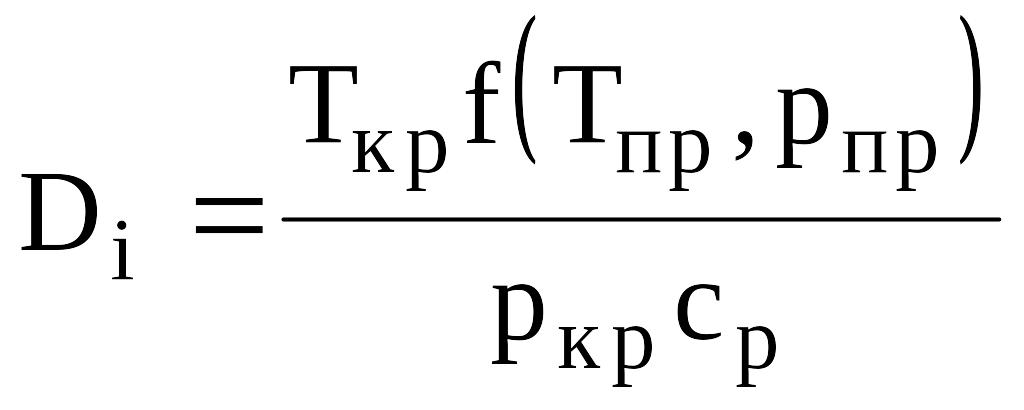 ,
(в17)
,
(в17)
где
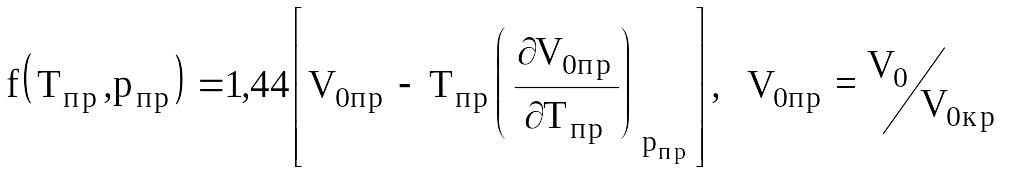 .
.
Значение функции f можно определить по графику или рассчитать с погрешностью менее 7% по корреляции Гухмана и Нагарёвой
![]() ,
(в18)
,
(в18)
при 0,82 £ рпр £ 3,5 и 1,6 £ Тпр £ 2,1.
Для реальных природных газов коэффициент Джоуля-Томсона, кроме (в17) можно выразить через коэффициент сверхсжимаемости z:
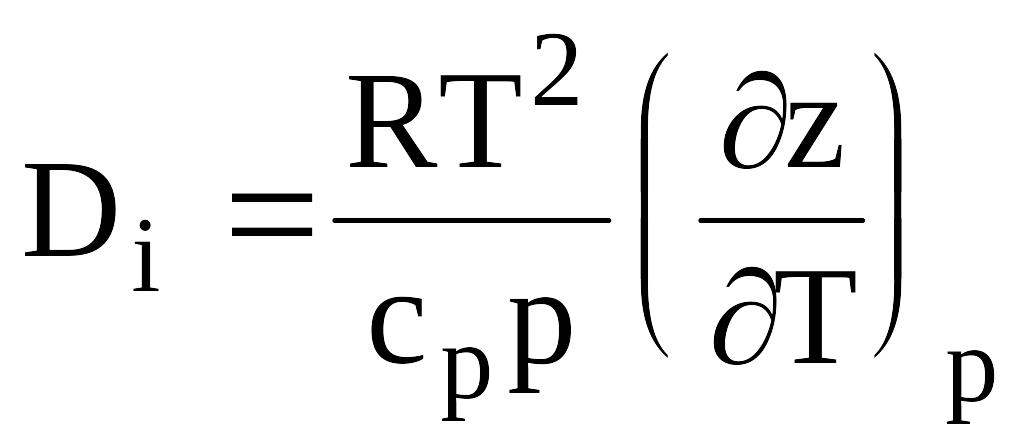 .
(в19)
.
(в19)
Изменение температуры газа в процессе изоэнтальпийного расширения при значительном перепаде давления на дросселе называется интегральным дроссель-эффектом. Это изменение можно определить по соотношению
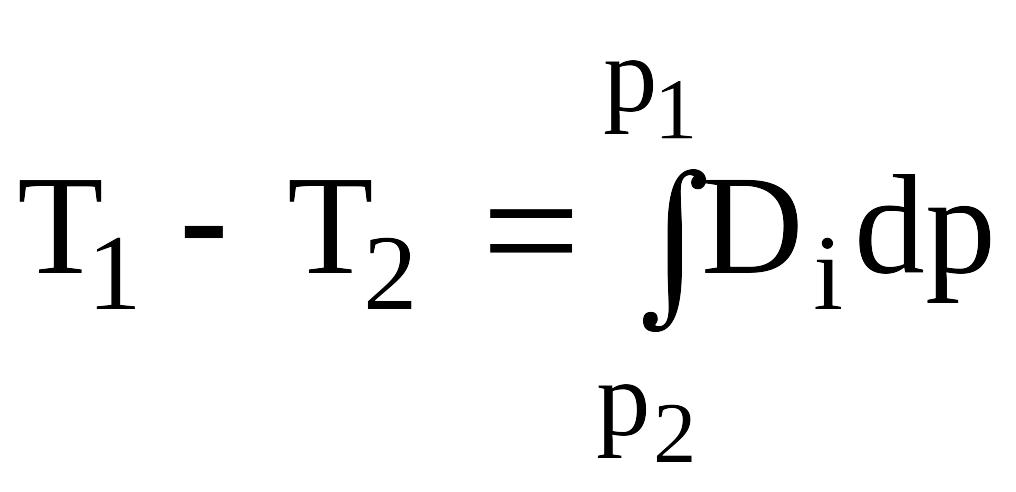 (3.20)
(3.20)
или по энтальпийным диаграммам
Приближенно конечную температуру газа в процессе дросселирования находят по формуле
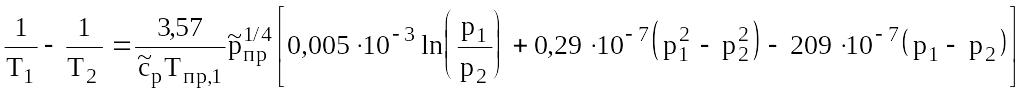 ,
(в21)
,
(в21)
где
![]() .
.
Интегральный коэффициент Джоуля-Томсона для природного газа изменяется от 2 до 4 К/МПа в зависимости от состава газа, падения давления и начальной температуры газа. Для приближенных расчетов среднее значение коэффициента Джоуля-Томсона можно принять равным 3 К/МПа.
Аналитические выражения частных производных от коэффициента сверхсжимаемости позволяют рассчитать изменение температур природных газов при изоэнтальпийном, изоэнтропийном и политропном процессах, т.е. изменение температур природных газов в процессе дросселирования, охлаждения и сжатия в идеальных детандере и компрессоре.
Дифференциальный коэффициент Джоуля-Томсона ( i =const)
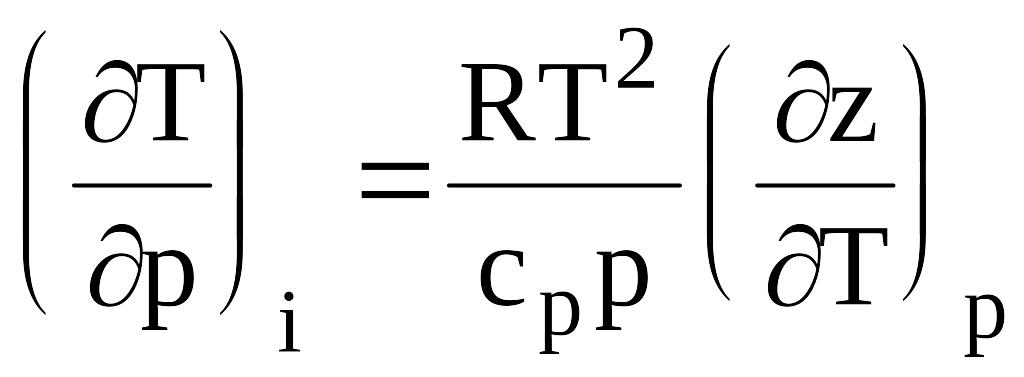 .
(в22)
.
(в22)
Изменение температуры природного газа в идеальном детандере или компрессоре (S=const)
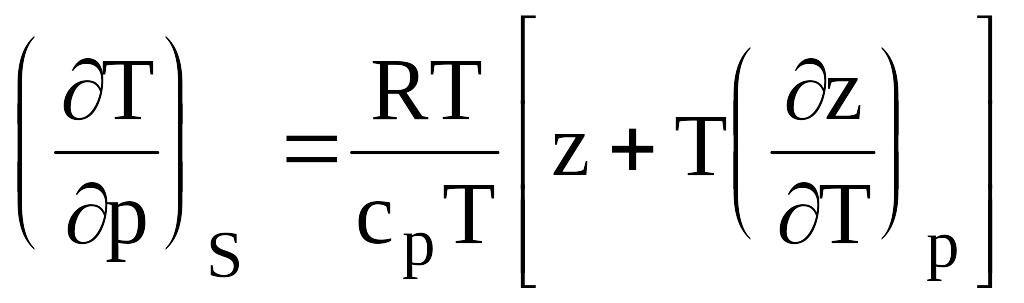 .
(в23)
.
(в23)
Изменение температуры в политропном процессе (h=const)
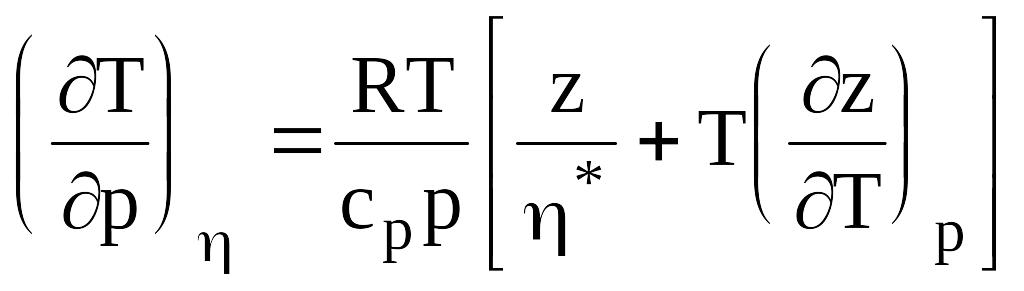 ,
(в24)
,
(в24)
где h* - условный к.п.д. процесса (h*<1 при сжатии газа в компрессоре и h*>1 при расширении газа в детандере).
Эффективность использования свободного перепада давления для охлаждения газа в детандере по сравнению с дросселированием его в штуцере можно рассчитать по уравнению
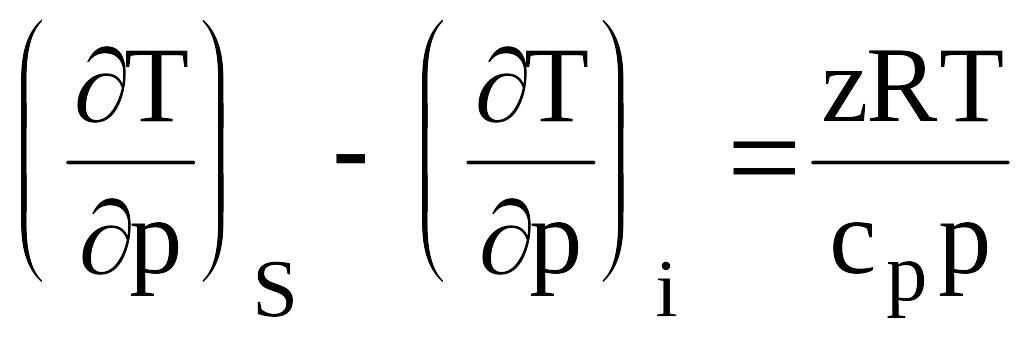 .
(в25)
.
(в25)
Теплопроводность газов
Теплопроводность - физическое свойство вещества, определяющее скорость переноса теплоты и выражаемое уравнением Фурье
![]() ,
(в26)
,
(в26)
где dQ/dt - перенос теплоты посредством проводимости, Дж/с;
l - коэффициент теплопроводности вещества (теплопроводность) Вт/(м К);
А - площадь, перпендикулярная направлению потока тепла, м2;
х - расстояние, м;
Т - температура, К.
Теплопроводность природной газовой смеси можно определить по приведённой плотности rпр=r/rкр из зависимостей Стила -Тодоса и Тиракьяна.
Зависимости Стила-Тодоса:
а) rпр> 2
![]()
b) 0,5<rпр£ 2
![]() (в.27)
(в.27)
rпр£ 0,5
![]()
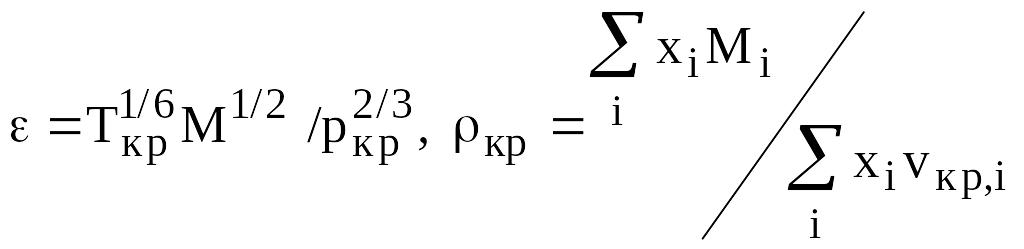
где l измеряется в 418.68 Вт/(м К).
Коэффициент теплопроводности l0 при атмосферном давлении имеет следующую зависимость от температуры
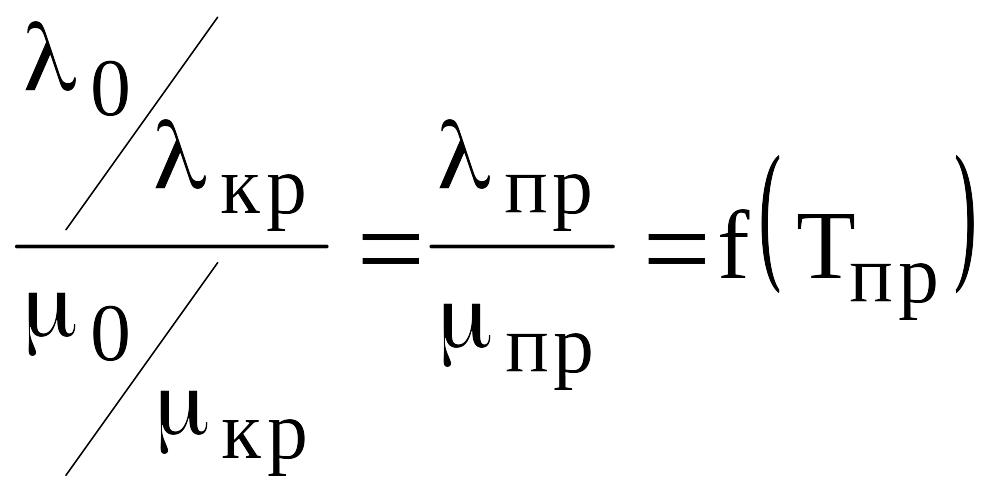 ,
(в28)
,
(в28)
где
Тпр |
0,5 |
1,0 |
2,0 |
3,0 |
5,0 |
10,0 |
40,0 |
f |
0,655 |
0,855 |
0,97 |
1,018 |
1,11 |
1,192 |
1,395 |
При Тпр=0,8 - 8,0
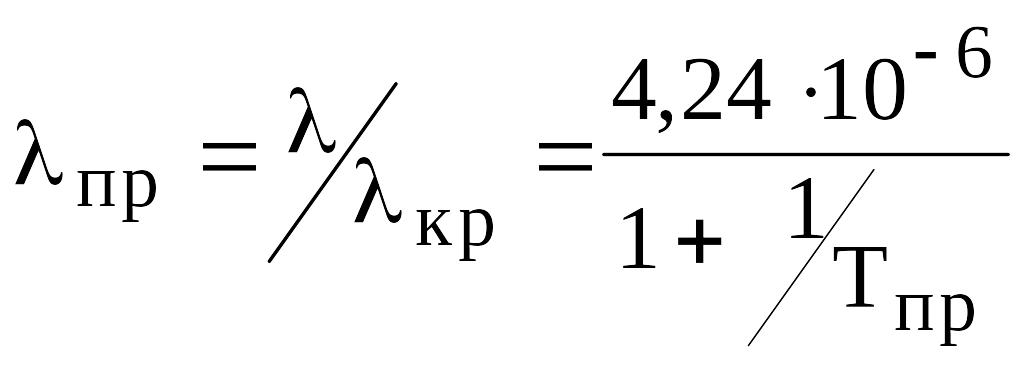 .
(в29)
.
(в29)
Зависимость Тиракьяна
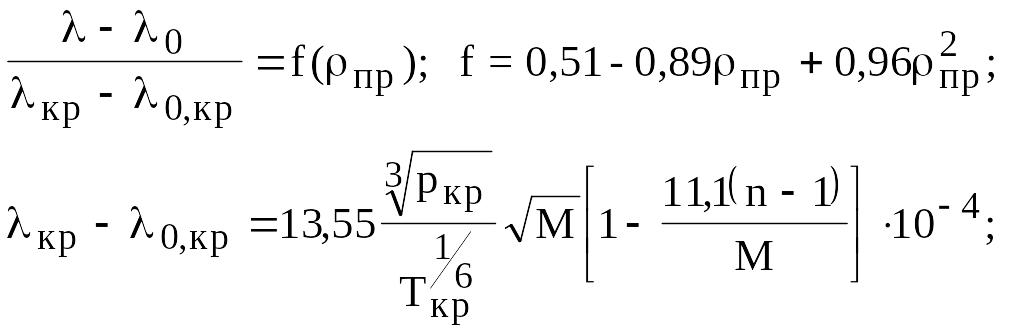 (в30)
(в30)
где n- число атомов углерода в молекулах; для смеси n=åxini .

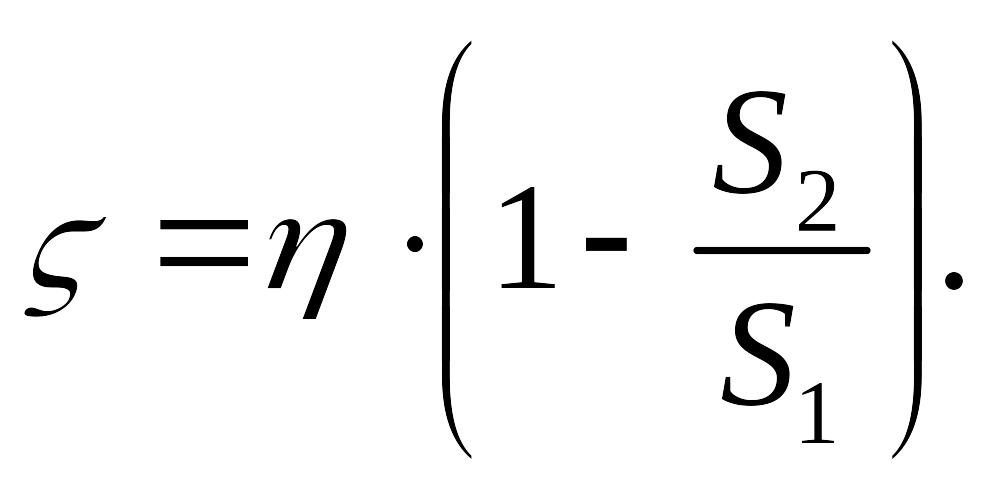
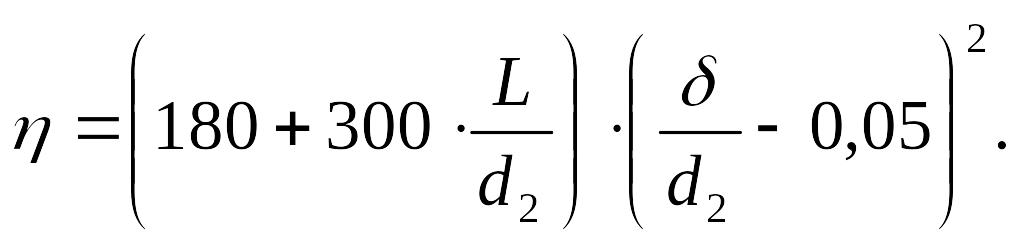
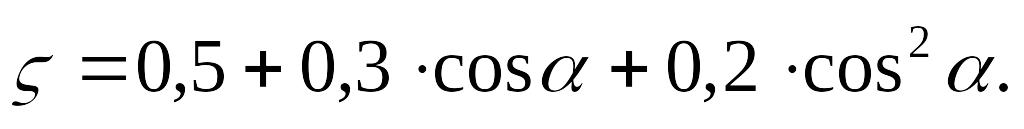
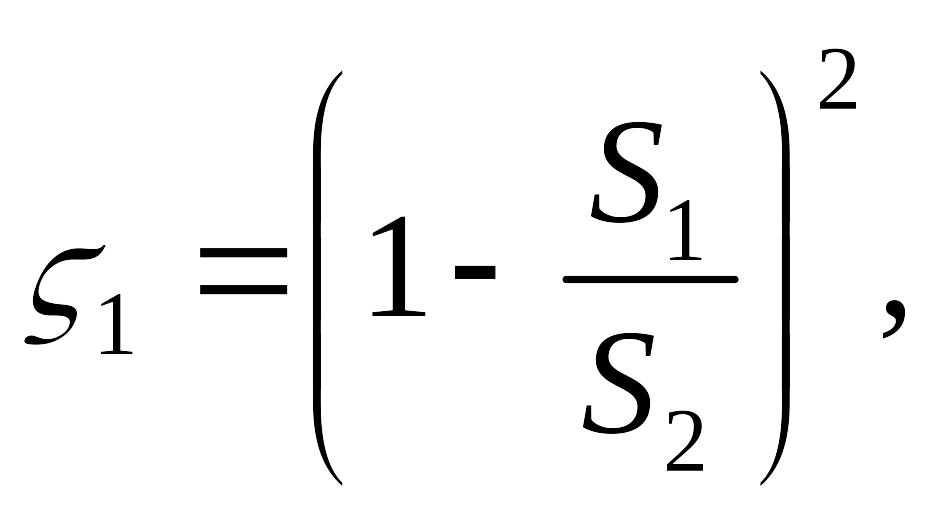
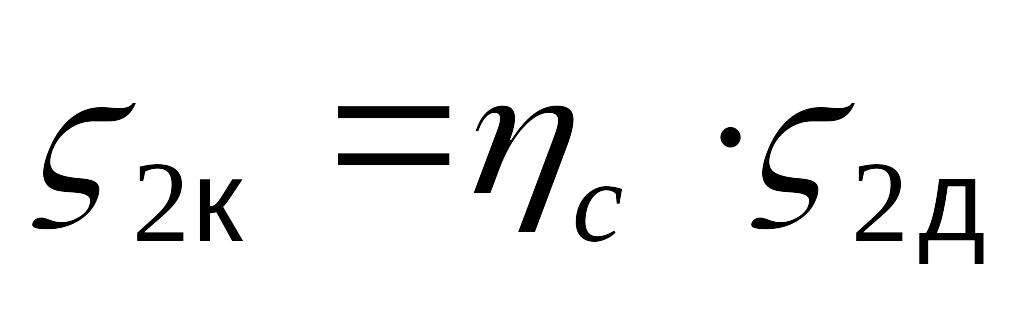 .
.