
- •Глава 1. (введение). “кризис” кинетической теории. Необходимое изменение традиционной молекулярной модели. История и состояние вопроса
- •Глава 2. Компьютерное моделирование затвердевания. Отсутствие затвердевания в традиционной модели. Характер эффектов, стабилизирующих структуру
- •Глава 3. Квазикристаллические свойства жидкостей.
- •1.1.1. В традиционной модели нет затвердевания
- •1.1.3. Затвердевание как следствие нарастания атомарных квантовых эффектов
- •1.1.5. История вопроса об отсутствии затвердевания
- •1.1.6. Соотношение теории и опыта. Психологические аспекты
- •1.1.7. Общая физическая причина обсуждаемых дискуссий
- •1.1.8. Квазикристаллические свойства жидкости
- •1.2. Феноменологическое описание свойств жидкости и твердого тела, представление о их противоположности.
- •1.2.1. Прочность и дальний порядок
- •1.2.2. Формирование традиционной молекулярной модели жидкости и затвердевания
- •1.2.3. Успехи кинетической теории на основе традиционной модели
- •1.2.4. Современный вид традиционной модели
- •1.2.5. Аналитические оценки кинетических свойств
- •1.2.6.Выявление неадекватности модели. Анализ прочности на атомарном уровне
- •1.2.7.Структурный подход к плавлению
- •1.2.8. Энергии активации
- •1.2.9. Нарастание трудностей в истолковании фазовых переходов
- •1.2.10. Признаки застоя в молекулярной теории кинетических свойств
- •1.3. Заключение
- •1.3.1. Мировоззренческий характер традиционных взглядов. Влияние философии
- •Традиционная модель и философия
- •Традиционная модель и философия
- •Кризисы в разных областях исследования
- •1.3.2. О химической форме движения материи
- •1.3.3. Ориентировочные оценки и строгие методы. Математизация исследований
- •1.3.4.Математизация исследований. Вытеснение
- •1.3.5. Приближённые оценки
- •1.4. Заключение к главе 1
- •Глава 2. Компьютерное моделирование затвердевания. Характер эффектов, стабилизирующих структуру
- •2.1 Прямое моделирование процессов переноса. Отсутствие затвердевания в традиционной модели
- •2.1.1.Затвердевание как скачок кинетических свойств
- •2.1.2. Прямое компьютерное моделирование вязкого или пластического течения и ионного электропереноса
- •2.1.3. Течение в модели при температурах около абсолютного нуля
- •2.1.4. Релаксация механических напряжений. Деформация постоянной силой
- •2.2. Обсуждение результатов моделирования
- •2.2.1.Температурная зависимость кинетических свойств
- •2.2.2. Влияние вида парного потенциала
- •2.2.3. Молекулярный механизм пластической деформации или вязкого течения
- •2.2.4. Молекулярный механизм течения около абсолютного нуля
- •2.3. Кристаллизация. Устойчивость
- •2.3.1. Моделирование кристаллизации
- •2.3.2. Устойчивость решеток и сеток
- •2.3.3. Определение мягких мод в компьютерном эксперименте
- •2.4. Состояние вопроса об отсутствии затвердевания
- •2.4.1. Литературные данные
- •2.4.2. Расхождение традиционной модели с действительностью по дальнему порядку и размытости фазовых переходов
- •2.5. Затвердевание как переход в квантовую область. Подбор потенциала для стабилизирующих структуру эффектов
- •2.5.1. Затвердевание приходится на температуры перехода из классической области в квантовую
- •2.5.2. Подобие затвердевания и перехода к сверхтекучести
- •2.5.3. Диаграммы состояния других веществ в области около абсолютного нуля
- •2.5.4. Подбор поправки к потенциалу для выражения эффектов, стабилизирующих структуру
- •2.5.5. Влияние направленности и ковалентности связи
- •2.5.6. Другие свойства твердых тел, не объясняющиеся в рамках традиционной модели
- •2.6. Заключение к гЛаве 2. Состояние вопроса
- •Глава 3. Квазикристалличекие свойства жидкостей
- •3.1. Традиционная модель и квазикристаллические свойства. Состояние вопроса
- •3.1.1. Введение
- •3.2. Модуль сдвига и предел прочности жидкости
- •3.2.1. Экспериментальная часть
- •3.2.2. Обсуждение результатов. Состояние вопроса
- •3.2.3. Последействие
- •3.3. Особенности на политермах и структурные перестройки в жидкости
- •3.3.1. Превращение в жидком железе около 1640 oС
- •3.3.2. Превращения в силикатных расплавах
- •3.3.3. Политермы вязкости воды
- •3.3.4. Дифференциальные координаты
- •3.4. О дальнем порядке в жидкости
- •3.4.1. Экспериментальные данные
- •3.4.2. Огранка
- •3.4.3. Сопоставление с традиционным подходом. Состояние вопроса
- •3.5. Осцилляции
- •3. 6. Квазикристаллические свойства жидкости и генерация турбулентных пульсаций в гидродинамическом потоке. Состояние вопроса
- •3.6.1. Введение
- •3.6.2. История вопроса (по работам [12, 53, 133, 134])
- •3.6.3. Механизм генерации пульсаций в потоке при твердоподобном сопротивлении течению
- •3.6.4. Сопоставление с известными примерами генерации колебаний.
- •3.6.5. Концентрация течения в отдельных плоскостях
- •3.6.6. Образование вихрей
- •3.6.7. Объемная и поверхностная турбулизация
- •3.6.8. Резюме к параграфу 3.6
- •Глава 4. Зернистая, или блоковая, структура реальной жидкости
- •4.1. Блоки и размытость фазовых переходов
- •4.1.1. Температурный интервал размытия т переходов
- •4.1.2. Экспериментальные данные [28, 30]
- •4.1.3. Оценка величины "кванта превращения" при других переходах
- •4.1.4. Размытость "концентрационных фазовых переходов"
- •4.1.5. "Надмолекулярный" характер соединений в твердом теле
- •4.1.6. Устойчивость соединений. Выделение химического и структурного слагаемых в энергии взаимодействия
- •4.2. Неоднородность течения реальной жидкости. Зернистая структура и соотношение коэффициентов вязкости и диффузии
- •4.2.1. Неоднородность течения
- •4.2.2. Оценка размеров "блоков течения" в жидкости
- •4.3. Наследование зернистой структуры при плавлении и кристаллизации
- •4.3.1."Наследственность"
- •4.3.2. Потоковая обработка
- •4.3.3. Термовременная обработка жидкого металла (тво) [24, 25]
- •4.3.4. Зародышеобразование и кинетика кристаллизации
- •4.3.5. Микронеоднородность эвтектических расплавов
- •4.3.6. Влияние слабых полей. Ультразвуковая обработка
- •4.3.7. Жидкий кристалл
- •4.3.8. Зависимость свойств поликристалла от размера зерна. Сверхпластичность. Дисперсионное упрочнение
- •4.4.9. Микрокристаллитная и коллоидная модель стекла
- •4.3.10. Состояние вопроса
- •4.4. Заключение к главе 4
- •Глава 5. Структурные дальнодействия и поверхностные явления
- •5.1. Дальнодействия в пленках и коллоидах
- •5.1.1. Дальнодействия в модели
- •5.1.2. Опытные данные по пленкам
- •5.1.3. Вязкие коллоиды и гели
- •5.1.4. Обсуждение опытных данных. Состояние вопроса
- •5.2. Дальнодействия в твердом состоянии
- •5.2.1. Масштабный фактор прочности
- •5.2.3. Дисперсионное упрочнение
- •5.2.4. О морфологии включений, фаз эвтектики, растущих кристаллов
- •5.2.5. Эффект ребиндера
- •5.2.6. Ориентирующие взаимодействия кристаллов
- •5.3. Выделение вклада дальнодействий в поверхностном натяжении
- •5.3.1. Дальнодействия, толстые пленки и их вклад в поверхностное натяжение
- •5.3.2. Термодинамические функции взаимодействия
- •5.3.3. Энтропия взаимодействия и оценки плотности упаковки, степени квантовости
- •5.3.4. Модель разорванных связей
- •5. 3. 5. Электронные теории поверхностного натяжения
- •5. 3. 6. Уточнение формулы для поверхностного натяжения чистых жидкостей
- •5.3.7.Поверхностное натяжение растворов
- •5.3.8.Аномально высокая поверхностная активность
- •5.3.9. Межфазное натяжение
- •5.3.10.Выделение вклада структурных дальнодействий и толстых пленок в поверхностное натяжение. Граница кристалл-жидкость в однокомпонентной системе
- •5.3.11. Граница кристалл-газ. Межзеренные границы
- •5.3.12. Зависимость температуры кристаллизации от размера капельки
- •5.3.13. Решетка и огранка малых частиц
- •5.4. Спекание и смачивание. Роль структурных дальнодействий и толстых пленок
- •5.4.1. Кинетический акт в традиционной модели
- •5.4.2. Кинетический акт спекания и смачивания в предлагаемой модели. Трение
- •5.4.3. Опытные данные по скорости самого акта спекания (кинетического звена)
- •5.4.4. Кинетическое сопротивление растеканию
- •5.4.5. Транспортное сопротивление спеканию и смачиванию.
- •5.5. Поверхностные свойства и дальнодействующие структурные
- •Глава 6. Корреляция параметров затвердевания и стабильности структуры с приведенной температурой и с мерой квантовости.
- •6.2.Превращения в начале и конце интервала затвердевания.
- •6.2.1. Начало интервала затвердевания или переход от состояния простой жидкости к состоянию реальной (затвердевающей) жидкости.
- •6.2.2. Конец интервала затвердевания.
- •6.2.3. "Точка стеклования" кристаллических веществ.
- •6.3.Общая сxема изменения кинетических свойств.
- •6.3.1. Общая схема изменения кинетических свойств при стекловании и кристаллизации.
- •6.3.2. Общий вид и истолкование политерм вязкости. Состояние вопроса.
- •6.3.3. Описание затвердевания в терминах вязкости и прочности. O качественном различии жидкости и твердого тела.
- •6.3.4. Тепловой эффект, сопровождающий повышение вязкости.
- •6.3.5. Химические классы жидкостей и стадии затвердевания.
- •6.4. Влияние атомарных квантовых эффектов.
- •6.4.1. Затвердевание и “степень квантовости”.
- •6. 4. 2. Влияние квантового параметра на tемпературу плавления.
- •6.5. Аналогичные закономерности для скорости химических реакций.
- •6.5.1. Подобие закономерностей для стабильности межмолекулярной и внутримолекулярной структуры. Постановка вопроса.
- •6.5.2. Зависимость стабильности внутримолекулярной структуры и “степени молекулярности” от квантового параметра.
- •6.5.3. Переходы от молекулярной формы к атомарной. Стёкла как промежуточные состояния.
- •6.5.4.Размягчение внутримолекулярной структуры при нагреве. Температурная зависимость энергий активации химических реакций.
- •6.5.5.Другие закономерности. Усреднение степени молекулярности компонентов раствора и катализ.
- •6.5.6. Перераспределение суммарной стабильности между внутри- и межмолекулярной структурой.
- •6.5.7. Перераспределение жесткости структуры и термодинамические характеристики плавления молекулярных веществ.
- •6.5.8.Простая атомарная многокомпонентная жидкость.
- •6.6. Заключение. Состояние вопроса.
- •6.6.1. Основные результаты.
- •7. Резюме.
- •Часть 2. - м.: Металлургиздат, 1966, 720 с.
6. 4. 2. Влияние квантового параметра на tемпературу плавления.
Согласно традиционным представлениям, температура плавления различных веществ должна приходиться на одинаковые значения приведённой энергии взаимодействия Uвз/RT или энтропии взаимодействия Sвз , относительной амплитуды колебаний атомов qс/q. Известное правило Линдемана утверждает, что все вещества плавятся при достижении одинаковой величины приведённой амплитуды колебаний, qс/q = const при Тпл. Правило Линдемана остаётся одной из наиболее применяемых закономерностей, связывающих температуру плавления с параметрами межатомных взаимодействий: Тпл = С(/AV2/3)1/2 ; С - постоянная Линдемана, - температура Дебая.
Кристаллизация в традиционной модели, то есть переход беспорядок-порядок, подробно изучен к настоящему времени, как аналитически, так и с помощью компьютерных экспериментов [2, 4, 55, 56]. При одинаковом потенциале состояния различных веществ с равными значениями Uвз/RT (или с одинаковыми Sвз, Vс/V, qс/q) являются соответственными и моделируются одним компьютерным экспериментом. Хорошо изучено упорядочение (кристаллизация) в системе жёстких сфер. Упорядоченная система с плотнейшей шаровой упаковкой ГЦК или ГПУ разупорядочивается, если амплитуда атомных колебаний возрастает до qс/q 0,13, плотность упаковки Y и энтропия взаимодействия Sвз понижаются до значений соответственно Y 0,54, Sвз 6R. Эти величины Y и Sвз связаны соотношением Sвз = R*[(4Y-3Y2)/(1-Y)2] [78]. Приблизительно при этих же значениях Sвз ,Y , qс/q, Vс/V наступает разупорядочение или плавление и в моделях с более реальными потенциальными ямами, при этом оно приходится на значение приведенной температуры около RT/Uвз 0,02.
Однако реальные кристалличесие решетки часто оказываются значительно более устойчивыми к разупорядочению (плавлению), чем соответствующие структуры в модели. Это считается “настоящим вызовом теоретикам” [55]; реальные вещества плавятся при больших значениях qс/q, Vс/V, RTвз/Uвз, меньших Sвз и Y. Параметры плавления в модели и в действительности особенно сильно разнятся при большой степени квантовости h/kT. Это привело к предположению, что здесь также более точными будут двупараметрические кореляции, при втором параметре h/kTпл.
Пользуясь энтропией межатомного взаимодействия Sвз 3Rln(qc/ q), модельное правило Линдемана qc/q = const можно записать в форме термодинамического условия Sвз = const; возможности расчетов при этом намного увеличиваются.
На рисунке 6.17 представлены результаты проверки правила в форме условия Sвз = const для элементов периодической системы. Видно, что энтропия взаимодействия действительно примерно одинакова у всех веществ в точке плавления. В среднем Sвз 5,19R и среднеквадратичная ошибка (дисперсия) Sвз составляет 0,94R; температуры плавления элементов можно рассчитать из такого правила Линдемана со средней ошибкой примерно в два раза.
Разброс значений на графике или дисперсия (ошибка правила) уменьшается, если выделить группу веществ с близкими свойствами и без лёгких элементов. Например, щелочные металлы K, Rb, Cs попадают в узкий интервал 4,2 < Sвз/R < 4,35. Дисперсия несколько уменьшается также, если выделить группы элементов с одинаковой кристаллической решёткой предплавления. На рисунке 6.17 корреляции для ОЦК, ГЦК, ГПУ - элементов представлены отдельно.
Температура плавления также значительно точнее описывается двупараметрической зависимостью, как и рассмотренные выше политермы вязкости. Вторым параметром здесь также оказывается квантовый параметр h/kT или степень квантовости атомарной системы. Постоянная Линдемана С или величина энтропии взаимодействия в точке плавления сильно зависит от параметра h/kTпл (от Sпл) в этом состоянии.
Согласно правилу Линдемана, “различные вещества плавятся при достижении определённой относительной амплитуды колебаний. " Было проверено другое правило: “различные вещества плавятся при достижении определённой степени квантовости”, тоесть в точке плавления h/kT = const, S = const. Точность последнего условия получается примерно такой же, как и у самого правила Линдемана. Другие возможные условия или “правила” помимо этих, дают большую ошибку [203].
Статистическая обработка данных по корреляциям для ОЦК, ГЦК и ГПУ структурам рис.6.17 дала следующие уравнения:
ОЦК: Sвз - 0,24S = 2,23
ГЦК: Sвз - 0,21S = 2,81 ( 6.4 )
ГПУ: Sвз - 0,34S = 2,39
Эти уравнения можно рассматривать как новые “правила”, определяющие температуру плавления различных веществ с учётом уже двух факторов - плотности упаковки структуры и “степени квантовости”, то есть Sвз и S. Дисперсия или средняя ошибка этих “правил” составляет около 0,25R; с помощью такого условия Sвз - aS = const можно рассчитать температуру плавления в 3-4 раза точнее, чем по исходному правилу Линдемана или по условию постоянства “степени квантовости” - (h/kT) в точке плавления.
Полученные корреляции показали, что повышение величины квантовых эффектов приводит к более раннему затвердеванию при охлаждении. Квантовые эффекты способствуют затвердеванию, повышают стабильность упорядоченной структуры. Параметры реального плав-ления приближаются к теоретическим для традиционной модели лишь в области малых квантовых эффектов, то есть для тяжёлых и тугоплавких элементов и их соединений, для которых параметр h/kTпл составляет 0,1-0,2. Компьютерные эксперименты и аналитические решения дают плавление ( разупорядочение ) при :
Sвз = 6R; qс/q = 0,13; Vс/V = 0,002; Y = 0,54; RTпл/Uвз = 0,02
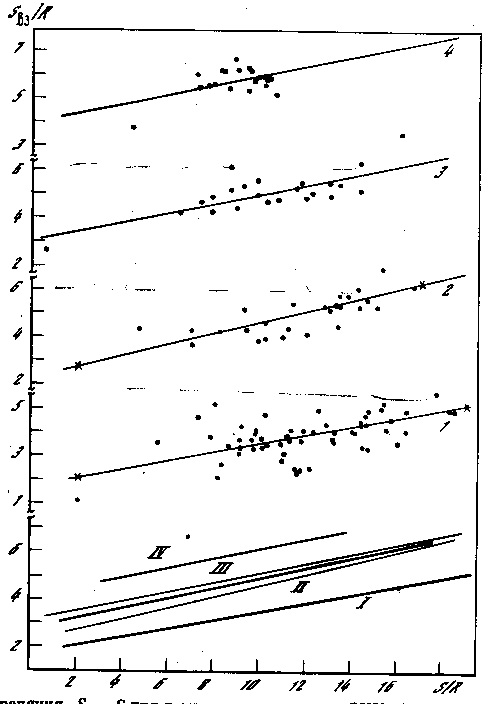
Рис.6.17 Корреляция плотности упаковки и степени квантовости в форме Sвз-S для температур плавления ОЦК, ГЦКи ГПУ - элементов (прямые 1,2,3). 4 - Та же корреляция для полиморфного превращения ОЦК - ГПУ. Вещества с большими значениями квантового параметра ( с меньшей S) плавятся при меньшей плотности упаковки атомов (меньшей Sвз).
Из рисунка 6.17 видно, что, по мере увеличения квантового параметра, величина Sвз всё больше удаляется вниз от теоретического значения 6R. В среднем для всех элементов Sвз 5,19R. Лёгкие и легкоплавкие вещества, которые имеют наибольшее значение параметра h/kTпл = (1-10) и являются “наиболее квантовыми”, плавятся при Sвз (2,5-3,5)R, рис.6.17. Расчёт по приведённым выше формулам показывает, что “наиболее квантовые” вещества плавятся при повышенной почти на порядок величины приведённой температуре (RTпл/Uвз (0.10-0,15) вместо 0,02), увеличенной относительной амплитуде колебаний (qс/q (0,3-0,5) вместо 0,13), весьма низкой плотности упаковки “жёстких сердцевин” атомов Y порядка 0,2 (вместо 0,54).
Интересно, что атомарные вещества He, Ne, Ar здесь попадают в ту же корреляцию, как и молекулярные; важна суммарная степень квантовости и неважно, обусловлена ли она единственной связью данного атома в молекуле (H2, N2, CO), или же создаётся одинаковыми связями атома со всеми соседями, как в He, Ne, Ar. Гелий здесь не образует исключение, как во многих корреляциях; здесь он выступает не как отличная от других особая квантовая жидкость, или квантовый кристалл, а укладывается в общую закономерность. При увеличении давления и, соответственно, температуры плавления, степень квантовости гелия уменьшается, и приведённая температура плавления приближается к нормальной величине; при увеличении Рпл до 13900 атм и Тпл = 77,3 К приведённая температура плавления понижается уже с 10.7*10-2 до 3,5*10-2. В целом повышение приведенной температуры плавления у веществ из легких элементов видно из табл. 3.
“Степень квантовости” веществ здесь выражена величиной квантового понижения теплоемкости С и принята равной (3R/C-1); эта величина в данном случае удобнее, так как для ряда веществ есть данные по теплоемкости, но нет по энтропии.
Обычно считается, что у таких жидкостей, как вода и углеводороды, величина квантовых эффектов незначительна. Однако даже в точке плавления льда его теплоёмкость составляет лишь половину классического значения 3R; примерно половина степеней свободы “выморожена”, параметр (h/ kT)ср 4 значителен и, соответственно, приведённая температура плавления льда (а также CH4, NH3 и др.) заметно повышена ( 0,054; 0,085; 0,062 вместо 0,02, см. таблицу). Повышение температуры плавления у рассмотренных жидкостей с высокими значениями h/kT приводит к тому, что температура плавления приближается у них к температуре кипения. Отношение Тпл/Ткип повышается до 0,7 - 0,95, тогда как у “нормальных” (тяжелых) веществ и в модели - Тпл/Ткип - (0,25 - 0,4). Ряд таких закономерностей приведены в монографии Уббелоде [29]. Например, у воды температура плавления (0 oС) выше, чем у тяжелой и “малоквантовой” ртути, (-40 oС) хотя температура кипения (100 oС) намного ниже (357 oС).
Вещество |
Тпл, К |
”степень квантовости” 3R/C-1 |
Приведённая Тпл (RTпл/Uвз)*102 |
Тпл/Ткип |
Вещества из легких элементов: |
||||
He |
1,8 |
20 |
10 |
- |
He |
2,0 |
15 |
10,4 |
- |
He |
4,0 |
10 |
10,7 |
- |
He |
14 |
2,3 |
8,8 |
- |
He |
77,3 |
0 |
4,8 |
- |
Ne |
24, 3 |
0,5 |
10 |
0,9 |
H2 |
14 |
10 |
14 |
0,7 |
D2 |
19 |
6 |
11 |
0,8 |
N2 |
63 |
0,3 |
15 |
0,8 |
CO |
68 |
0,15 |
10 |
0,85 |
NH3 |
195 |
1 |
6,2 |
0,8 |
H2O |
273 |
1 |
5,4 |
0,73 |
CH4 |
90 |
5 |
8,5 |
0,9 |
C2H6 |
90 |
3 |
5,2 |
0,46 |
C6H14 |
178 |
2 |
3,4 |
0,52 |
C20H42 |
310 |
2 |
2,0 |
0,50 |
Вещества из тяжелых элементов: |
||||
Hg |
233 |
0 |
3,5 |
0,33 |
K |
336 |
0 |
4,5 |
0,32 |
Pb |
600 |
0 |
2,6 |
0,29 |
Fe |
1808 |
0 |
3,7 |
0,25 |
В модели |
-- |
2,0 |
0,2 |
30,3 |
