
- •Глава 1. (введение). “кризис” кинетической теории. Необходимое изменение традиционной молекулярной модели. История и состояние вопроса
- •Глава 2. Компьютерное моделирование затвердевания. Отсутствие затвердевания в традиционной модели. Характер эффектов, стабилизирующих структуру
- •Глава 3. Квазикристаллические свойства жидкостей.
- •1.1.1. В традиционной модели нет затвердевания
- •1.1.3. Затвердевание как следствие нарастания атомарных квантовых эффектов
- •1.1.5. История вопроса об отсутствии затвердевания
- •1.1.6. Соотношение теории и опыта. Психологические аспекты
- •1.1.7. Общая физическая причина обсуждаемых дискуссий
- •1.1.8. Квазикристаллические свойства жидкости
- •1.2. Феноменологическое описание свойств жидкости и твердого тела, представление о их противоположности.
- •1.2.1. Прочность и дальний порядок
- •1.2.2. Формирование традиционной молекулярной модели жидкости и затвердевания
- •1.2.3. Успехи кинетической теории на основе традиционной модели
- •1.2.4. Современный вид традиционной модели
- •1.2.5. Аналитические оценки кинетических свойств
- •1.2.6.Выявление неадекватности модели. Анализ прочности на атомарном уровне
- •1.2.7.Структурный подход к плавлению
- •1.2.8. Энергии активации
- •1.2.9. Нарастание трудностей в истолковании фазовых переходов
- •1.2.10. Признаки застоя в молекулярной теории кинетических свойств
- •1.3. Заключение
- •1.3.1. Мировоззренческий характер традиционных взглядов. Влияние философии
- •Традиционная модель и философия
- •Традиционная модель и философия
- •Кризисы в разных областях исследования
- •1.3.2. О химической форме движения материи
- •1.3.3. Ориентировочные оценки и строгие методы. Математизация исследований
- •1.3.4.Математизация исследований. Вытеснение
- •1.3.5. Приближённые оценки
- •1.4. Заключение к главе 1
- •Глава 2. Компьютерное моделирование затвердевания. Характер эффектов, стабилизирующих структуру
- •2.1 Прямое моделирование процессов переноса. Отсутствие затвердевания в традиционной модели
- •2.1.1.Затвердевание как скачок кинетических свойств
- •2.1.2. Прямое компьютерное моделирование вязкого или пластического течения и ионного электропереноса
- •2.1.3. Течение в модели при температурах около абсолютного нуля
- •2.1.4. Релаксация механических напряжений. Деформация постоянной силой
- •2.2. Обсуждение результатов моделирования
- •2.2.1.Температурная зависимость кинетических свойств
- •2.2.2. Влияние вида парного потенциала
- •2.2.3. Молекулярный механизм пластической деформации или вязкого течения
- •2.2.4. Молекулярный механизм течения около абсолютного нуля
- •2.3. Кристаллизация. Устойчивость
- •2.3.1. Моделирование кристаллизации
- •2.3.2. Устойчивость решеток и сеток
- •2.3.3. Определение мягких мод в компьютерном эксперименте
- •2.4. Состояние вопроса об отсутствии затвердевания
- •2.4.1. Литературные данные
- •2.4.2. Расхождение традиционной модели с действительностью по дальнему порядку и размытости фазовых переходов
- •2.5. Затвердевание как переход в квантовую область. Подбор потенциала для стабилизирующих структуру эффектов
- •2.5.1. Затвердевание приходится на температуры перехода из классической области в квантовую
- •2.5.2. Подобие затвердевания и перехода к сверхтекучести
- •2.5.3. Диаграммы состояния других веществ в области около абсолютного нуля
- •2.5.4. Подбор поправки к потенциалу для выражения эффектов, стабилизирующих структуру
- •2.5.5. Влияние направленности и ковалентности связи
- •2.5.6. Другие свойства твердых тел, не объясняющиеся в рамках традиционной модели
- •2.6. Заключение к гЛаве 2. Состояние вопроса
- •Глава 3. Квазикристалличекие свойства жидкостей
- •3.1. Традиционная модель и квазикристаллические свойства. Состояние вопроса
- •3.1.1. Введение
- •3.2. Модуль сдвига и предел прочности жидкости
- •3.2.1. Экспериментальная часть
- •3.2.2. Обсуждение результатов. Состояние вопроса
- •3.2.3. Последействие
- •3.3. Особенности на политермах и структурные перестройки в жидкости
- •3.3.1. Превращение в жидком железе около 1640 oС
- •3.3.2. Превращения в силикатных расплавах
- •3.3.3. Политермы вязкости воды
- •3.3.4. Дифференциальные координаты
- •3.4. О дальнем порядке в жидкости
- •3.4.1. Экспериментальные данные
- •3.4.2. Огранка
- •3.4.3. Сопоставление с традиционным подходом. Состояние вопроса
- •3.5. Осцилляции
- •3. 6. Квазикристаллические свойства жидкости и генерация турбулентных пульсаций в гидродинамическом потоке. Состояние вопроса
- •3.6.1. Введение
- •3.6.2. История вопроса (по работам [12, 53, 133, 134])
- •3.6.3. Механизм генерации пульсаций в потоке при твердоподобном сопротивлении течению
- •3.6.4. Сопоставление с известными примерами генерации колебаний.
- •3.6.5. Концентрация течения в отдельных плоскостях
- •3.6.6. Образование вихрей
- •3.6.7. Объемная и поверхностная турбулизация
- •3.6.8. Резюме к параграфу 3.6
- •Глава 4. Зернистая, или блоковая, структура реальной жидкости
- •4.1. Блоки и размытость фазовых переходов
- •4.1.1. Температурный интервал размытия т переходов
- •4.1.2. Экспериментальные данные [28, 30]
- •4.1.3. Оценка величины "кванта превращения" при других переходах
- •4.1.4. Размытость "концентрационных фазовых переходов"
- •4.1.5. "Надмолекулярный" характер соединений в твердом теле
- •4.1.6. Устойчивость соединений. Выделение химического и структурного слагаемых в энергии взаимодействия
- •4.2. Неоднородность течения реальной жидкости. Зернистая структура и соотношение коэффициентов вязкости и диффузии
- •4.2.1. Неоднородность течения
- •4.2.2. Оценка размеров "блоков течения" в жидкости
- •4.3. Наследование зернистой структуры при плавлении и кристаллизации
- •4.3.1."Наследственность"
- •4.3.2. Потоковая обработка
- •4.3.3. Термовременная обработка жидкого металла (тво) [24, 25]
- •4.3.4. Зародышеобразование и кинетика кристаллизации
- •4.3.5. Микронеоднородность эвтектических расплавов
- •4.3.6. Влияние слабых полей. Ультразвуковая обработка
- •4.3.7. Жидкий кристалл
- •4.3.8. Зависимость свойств поликристалла от размера зерна. Сверхпластичность. Дисперсионное упрочнение
- •4.4.9. Микрокристаллитная и коллоидная модель стекла
- •4.3.10. Состояние вопроса
- •4.4. Заключение к главе 4
- •Глава 5. Структурные дальнодействия и поверхностные явления
- •5.1. Дальнодействия в пленках и коллоидах
- •5.1.1. Дальнодействия в модели
- •5.1.2. Опытные данные по пленкам
- •5.1.3. Вязкие коллоиды и гели
- •5.1.4. Обсуждение опытных данных. Состояние вопроса
- •5.2. Дальнодействия в твердом состоянии
- •5.2.1. Масштабный фактор прочности
- •5.2.3. Дисперсионное упрочнение
- •5.2.4. О морфологии включений, фаз эвтектики, растущих кристаллов
- •5.2.5. Эффект ребиндера
- •5.2.6. Ориентирующие взаимодействия кристаллов
- •5.3. Выделение вклада дальнодействий в поверхностном натяжении
- •5.3.1. Дальнодействия, толстые пленки и их вклад в поверхностное натяжение
- •5.3.2. Термодинамические функции взаимодействия
- •5.3.3. Энтропия взаимодействия и оценки плотности упаковки, степени квантовости
- •5.3.4. Модель разорванных связей
- •5. 3. 5. Электронные теории поверхностного натяжения
- •5. 3. 6. Уточнение формулы для поверхностного натяжения чистых жидкостей
- •5.3.7.Поверхностное натяжение растворов
- •5.3.8.Аномально высокая поверхностная активность
- •5.3.9. Межфазное натяжение
- •5.3.10.Выделение вклада структурных дальнодействий и толстых пленок в поверхностное натяжение. Граница кристалл-жидкость в однокомпонентной системе
- •5.3.11. Граница кристалл-газ. Межзеренные границы
- •5.3.12. Зависимость температуры кристаллизации от размера капельки
- •5.3.13. Решетка и огранка малых частиц
- •5.4. Спекание и смачивание. Роль структурных дальнодействий и толстых пленок
- •5.4.1. Кинетический акт в традиционной модели
- •5.4.2. Кинетический акт спекания и смачивания в предлагаемой модели. Трение
- •5.4.3. Опытные данные по скорости самого акта спекания (кинетического звена)
- •5.4.4. Кинетическое сопротивление растеканию
- •5.4.5. Транспортное сопротивление спеканию и смачиванию.
- •5.5. Поверхностные свойства и дальнодействующие структурные
- •Глава 6. Корреляция параметров затвердевания и стабильности структуры с приведенной температурой и с мерой квантовости.
- •6.2.Превращения в начале и конце интервала затвердевания.
- •6.2.1. Начало интервала затвердевания или переход от состояния простой жидкости к состоянию реальной (затвердевающей) жидкости.
- •6.2.2. Конец интервала затвердевания.
- •6.2.3. "Точка стеклования" кристаллических веществ.
- •6.3.Общая сxема изменения кинетических свойств.
- •6.3.1. Общая схема изменения кинетических свойств при стекловании и кристаллизации.
- •6.3.2. Общий вид и истолкование политерм вязкости. Состояние вопроса.
- •6.3.3. Описание затвердевания в терминах вязкости и прочности. O качественном различии жидкости и твердого тела.
- •6.3.4. Тепловой эффект, сопровождающий повышение вязкости.
- •6.3.5. Химические классы жидкостей и стадии затвердевания.
- •6.4. Влияние атомарных квантовых эффектов.
- •6.4.1. Затвердевание и “степень квантовости”.
- •6. 4. 2. Влияние квантового параметра на tемпературу плавления.
- •6.5. Аналогичные закономерности для скорости химических реакций.
- •6.5.1. Подобие закономерностей для стабильности межмолекулярной и внутримолекулярной структуры. Постановка вопроса.
- •6.5.2. Зависимость стабильности внутримолекулярной структуры и “степени молекулярности” от квантового параметра.
- •6.5.3. Переходы от молекулярной формы к атомарной. Стёкла как промежуточные состояния.
- •6.5.4.Размягчение внутримолекулярной структуры при нагреве. Температурная зависимость энергий активации химических реакций.
- •6.5.5.Другие закономерности. Усреднение степени молекулярности компонентов раствора и катализ.
- •6.5.6. Перераспределение суммарной стабильности между внутри- и межмолекулярной структурой.
- •6.5.7. Перераспределение жесткости структуры и термодинамические характеристики плавления молекулярных веществ.
- •6.5.8.Простая атомарная многокомпонентная жидкость.
- •6.6. Заключение. Состояние вопроса.
- •6.6.1. Основные результаты.
- •7. Резюме.
- •Часть 2. - м.: Металлургиздат, 1966, 720 с.
6.4. Влияние атомарных квантовых эффектов.
6.4.1. Затвердевание и “степень квантовости”.
Если ряд жидкостей имеют один потенциал межчастичного взаимодействия (r) (например, потенциал Леннард-Джонса, Морзе, Борна-Майера ), и различаются лишь глубиной потенциальной ямы, размером и массой частиц, то состояния таких жидкостей при одинаковых значениях RT/Uвз в традиционной теории называют соответственными; группа соответсвенных состояний моделируется одним компьютерным экспериментом. Точки плавления (разупорядочения) таких жидкостей также соответствуют одинаковой приведенной температуре RT/Uвз. Одинакова в соответственных состояниях и приведенная вязкость. В координатах dln/dlnT - ln, принятых для рисунков 6.2-6.6, политермы всех жидкостей с одинаковым потенциалом уложились бы на одну кривую.
В действительности на рис.6.6 получается не одна прямая, а довольно широкий веер или семейство прямых. В теории соответственных состояний такие зависимости называют двупараметрическими; вязкость зависит от двух параметров. Первым параметром можно считать температуру или приведённую температуру RT/Uвз. Изменению этого параметра соответствует перемещение по одной из политерм семейства, рис.6.6. Изменению второго параметра соответствует переход с одних линий семейства на другие, сдвиг на рис 6.6.. по горизонтали слева направо. Покажем, что вторым параметром можно взять “степень квантовости” системы, то есть величину квантового параметра h/kT при определённом фиксированном значении первого параметра Uвз/RT, или же при определённой вязкости, или при заданной величине m = dln/dlnT, или в точке плавления, и др.
На корреляциях рис.6.2 - 6.5 была отмечена горизонталь m=dln/dlnT=6 , пересекающая много политерм, и абсцисса точек пересечения были выбраны в качестве меры сдвига данной политермы вправо на рис.6.6. На рис. 6.15 представлена корреляция этого сдвига вправо в семействе кривых рис.6.6 с энтропией S и параметром h/kT в данном состоянии при m = 6. Получается чёткая корреляция. Вещества с большим значением h/kT, то есть с большей степенью квантовости располагаются на рисунке правее. Если не рассматривать молекулярные жидкости и благородные газы, то энергия взаимодействия всех остальных обсуждаемых веществ выражается величинами одного порядка, Uвз 100 ккал/г-атом. В этом случае большую интенсивность квантовых эффектов будут иметь просто атомы с наименьшим атомным весом. На рис. 6.15. крайними справа действительно являются линии, принадлежащие наиболее лёгким веществам - полимеризованным углеводородам со средним атомным весом Аср около 4,6.Аср. Далее располагаются линии стеклообразующих оксидов, таких как B2O3 (Аср - 14), SiO2 ( Аср - 20 ). С добавлением кристаллизующихся окислов, таких как CaO, K2O, FeO, PbO средний атомный вес увеличивается и соответствующая политерма располагается ещё левее. Далее лежат прямые тяжёлых металлов с атомным весом порядка 50 и более. С увеличением среднего атомного веса политерма почти монотонно смещается влево.
Все политермы рис. 6.2 - 6.6 начинаются в области простой жидкости около начала координат, поэтому сдвиг вправо означает переход к более медленному затвердеванию, к меньшим значениям угловых коэффициентов tg = n+1 политерм на рис. 6.15 ,то есть вторых производных или показателей n зависимости Е ~ Т-n. Для веществ, политермы которых располагаются справа, характерно медленное нарастание вязкости при охлаждении и большая длина интервала затвердевания по температуре, а также высокие значения вязкости жидкости в точке плавления ( см. корреляцию 3 рис.6.15 ), и, соответственно, медленная кристаллизация и лёгкое стеклование. Изменение энтропии S и скачок вязкости при кристаллизации по мере сдвига вправо становятся меньше; у некоторых веществ типа смол S, ,видимо, становятся нулевыми, исчезает и сама кристаллизация [31]. Наглядным признаком перехода в квантовую область является понижение теплоёмкости по сравнению с классической величиной С = 3R, то есть начинающееся при охлаждении квантовое “вымораживание” некоторых степеней свободы. По теории Дебая, это понижение теплоёмкости составляет 1% и, следовательно, может быть замечено при h/kT = 0,4; у “наиболее квантовых” веществ, политермы вязкости которых расположены на рис.6.6 справа, теплоёмкость действительно понижена по сравнению с классической величиной 3R.
В точке плавления у полиэтилена С 1,2R, у B2O3 2,4R , у P2O5 2,5R , у SiO2 2,6R. На рисунке 6.16. показано, какой стадии понижения теплоёмкости или вымораживания степеней свободы соответствуют температуры плавления различных веществ. Эти данные наглядно опровергают существующее мнение о том, что точки плавления лежат глубоко в классической области.
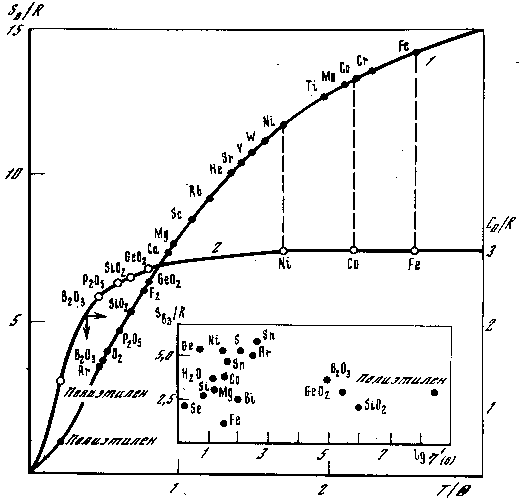
Рис.6.16 Энтропия и теплоёмкость жидкостей в точке плавления. Вещества с малым средним атомным весом плавятся при высокой степени квантовости и пониженной теплоёмкости.
Представляют интерес также данные о парциальной теплоёмкости С кал/г-ат град, элементов в твёрдых и жидких сплавах, шлаках, стёклах [9]:
Элементы |
C |
H |
N |
B |
Be |
O |
F |
S |
P |
Si |
Остальные |
Твёрдые |
1,8 |
2,3 |
2,7 |
2,8 |
3,8 |
4,0 |
5,0 |
5,4 |
5,5 |
4,8 |
6,3 |
Жидкости |
2,8 |
4,3 |
- |
4,7 |
- |
6,0 |
7,0 |
7,4 |
7,0 |
5,8 |
8,0 |
Теплоёмкость значительно понижена у перечисленных десяти лёгких элементов, которые относятся в основном к первой строке периодической системы ( S, Si - ко второй ). У C, H, N, B в твёрдых системах теплоёмкость меньше половины классического значения, то есть более половины степеней свободы “выморожены”. Невелика степень квантовости всех остальных элементов, кроме перечисленных десяти, поэтому из них нельзя получить медленно увеличивающие вязкость вещества с малым показателем n , большой вязкостью в точке плавления и легко стеклующиеся.
С традиционной точки зрения такими же свойствами должны обладать и другие вещества, химически подобные рассмотренным. Однако это не так; химически подобные вещества, но составленные из более тяжёлых элементов, увеличивают вязкость быстрее и не стеклуются; здесь важны не особенности химической связи, а “степень квантовости”, сильно зависящая от атомного веса. Так, соединение In2Te3 является химическим аналогом B2O3 но отнюдь не является сильным стеклообразователем, как B2O3. Si, Ge, Sn, Pb являются химическими аналогами углерода, однако из их соединений с водородом невозможно получить вязкие легко стеклующиеся вещества типа смол или полимеров.
В настоящее время достигнуты высокие скорости охлаждения (до 105 К/с) и за счет этого получено множество новых стекол. Для стеклования многих металлических сплавов необходимы скорости порядка 103 К/с. Для получения стеклообразного селена достаточны скорости охлаждения порядка десятков градусов в минуту. Давно известные силикатные, боратные и другие стёкла на основе перечисленных десяти лёгких элементов отличаются тем, что стеклование идет уже при обычной в лаборатории скорости охлаждения порядка (100-101) К/мин. Для стеклования кремнезема достаточна скорость охлаждения 10-2 К/мин.
Перечисленные десять лёгких элементов являются и лучшими “аморфизаторами” металлов - добавками, способствующими их стеклованию. Распространёнными аморфизаторами сплавов на основе железа являются кремний, фосфор, углерод; ещё более сильное аморфизирующее действие оказывает более лёгкий бор. Наиболее сильным аморфизатором является, видимо, водород, однако его общее действие не столь велико из-за малых концентраций вследствие очень низкой растворимости (10-2% ).
Таким образом, вид политерм вязкости в интервале затвердевания зависит от квантового параметра h/kT . При высоких значениях h/kT жидкость (не молекулярная) медленно увеличивает вязкость в интервале затвердевания, имеет малый показатель n в зависимости Е ~ Т-n, высокую вязкость в точке плавления и легко стеклуется. Такое вещество нельзя получить без десяти перечисленных лёгких элементов с высокой “степенью квантовости”.
Отметим ещё, что при переходе к веществам с ещё большими значениями квантового параметра, мы попадаем из области стёкол в область молекулярных жидкостей ( область 1 на рис. 6.6 ) для которых справедливы уже другие зависимости. Связь стеклообразования с молекулярностью и степенью квантовости обсуждается ниже.
