
- •Глава 1. (введение). “кризис” кинетической теории. Необходимое изменение традиционной молекулярной модели. История и состояние вопроса
- •Глава 2. Компьютерное моделирование затвердевания. Отсутствие затвердевания в традиционной модели. Характер эффектов, стабилизирующих структуру
- •Глава 3. Квазикристаллические свойства жидкостей.
- •1.1.1. В традиционной модели нет затвердевания
- •1.1.3. Затвердевание как следствие нарастания атомарных квантовых эффектов
- •1.1.5. История вопроса об отсутствии затвердевания
- •1.1.6. Соотношение теории и опыта. Психологические аспекты
- •1.1.7. Общая физическая причина обсуждаемых дискуссий
- •1.1.8. Квазикристаллические свойства жидкости
- •1.2. Феноменологическое описание свойств жидкости и твердого тела, представление о их противоположности.
- •1.2.1. Прочность и дальний порядок
- •1.2.2. Формирование традиционной молекулярной модели жидкости и затвердевания
- •1.2.3. Успехи кинетической теории на основе традиционной модели
- •1.2.4. Современный вид традиционной модели
- •1.2.5. Аналитические оценки кинетических свойств
- •1.2.6.Выявление неадекватности модели. Анализ прочности на атомарном уровне
- •1.2.7.Структурный подход к плавлению
- •1.2.8. Энергии активации
- •1.2.9. Нарастание трудностей в истолковании фазовых переходов
- •1.2.10. Признаки застоя в молекулярной теории кинетических свойств
- •1.3. Заключение
- •1.3.1. Мировоззренческий характер традиционных взглядов. Влияние философии
- •Традиционная модель и философия
- •Традиционная модель и философия
- •Кризисы в разных областях исследования
- •1.3.2. О химической форме движения материи
- •1.3.3. Ориентировочные оценки и строгие методы. Математизация исследований
- •1.3.4.Математизация исследований. Вытеснение
- •1.3.5. Приближённые оценки
- •1.4. Заключение к главе 1
- •Глава 2. Компьютерное моделирование затвердевания. Характер эффектов, стабилизирующих структуру
- •2.1 Прямое моделирование процессов переноса. Отсутствие затвердевания в традиционной модели
- •2.1.1.Затвердевание как скачок кинетических свойств
- •2.1.2. Прямое компьютерное моделирование вязкого или пластического течения и ионного электропереноса
- •2.1.3. Течение в модели при температурах около абсолютного нуля
- •2.1.4. Релаксация механических напряжений. Деформация постоянной силой
- •2.2. Обсуждение результатов моделирования
- •2.2.1.Температурная зависимость кинетических свойств
- •2.2.2. Влияние вида парного потенциала
- •2.2.3. Молекулярный механизм пластической деформации или вязкого течения
- •2.2.4. Молекулярный механизм течения около абсолютного нуля
- •2.3. Кристаллизация. Устойчивость
- •2.3.1. Моделирование кристаллизации
- •2.3.2. Устойчивость решеток и сеток
- •2.3.3. Определение мягких мод в компьютерном эксперименте
- •2.4. Состояние вопроса об отсутствии затвердевания
- •2.4.1. Литературные данные
- •2.4.2. Расхождение традиционной модели с действительностью по дальнему порядку и размытости фазовых переходов
- •2.5. Затвердевание как переход в квантовую область. Подбор потенциала для стабилизирующих структуру эффектов
- •2.5.1. Затвердевание приходится на температуры перехода из классической области в квантовую
- •2.5.2. Подобие затвердевания и перехода к сверхтекучести
- •2.5.3. Диаграммы состояния других веществ в области около абсолютного нуля
- •2.5.4. Подбор поправки к потенциалу для выражения эффектов, стабилизирующих структуру
- •2.5.5. Влияние направленности и ковалентности связи
- •2.5.6. Другие свойства твердых тел, не объясняющиеся в рамках традиционной модели
- •2.6. Заключение к гЛаве 2. Состояние вопроса
- •Глава 3. Квазикристалличекие свойства жидкостей
- •3.1. Традиционная модель и квазикристаллические свойства. Состояние вопроса
- •3.1.1. Введение
- •3.2. Модуль сдвига и предел прочности жидкости
- •3.2.1. Экспериментальная часть
- •3.2.2. Обсуждение результатов. Состояние вопроса
- •3.2.3. Последействие
- •3.3. Особенности на политермах и структурные перестройки в жидкости
- •3.3.1. Превращение в жидком железе около 1640 oС
- •3.3.2. Превращения в силикатных расплавах
- •3.3.3. Политермы вязкости воды
- •3.3.4. Дифференциальные координаты
- •3.4. О дальнем порядке в жидкости
- •3.4.1. Экспериментальные данные
- •3.4.2. Огранка
- •3.4.3. Сопоставление с традиционным подходом. Состояние вопроса
- •3.5. Осцилляции
- •3. 6. Квазикристаллические свойства жидкости и генерация турбулентных пульсаций в гидродинамическом потоке. Состояние вопроса
- •3.6.1. Введение
- •3.6.2. История вопроса (по работам [12, 53, 133, 134])
- •3.6.3. Механизм генерации пульсаций в потоке при твердоподобном сопротивлении течению
- •3.6.4. Сопоставление с известными примерами генерации колебаний.
- •3.6.5. Концентрация течения в отдельных плоскостях
- •3.6.6. Образование вихрей
- •3.6.7. Объемная и поверхностная турбулизация
- •3.6.8. Резюме к параграфу 3.6
- •Глава 4. Зернистая, или блоковая, структура реальной жидкости
- •4.1. Блоки и размытость фазовых переходов
- •4.1.1. Температурный интервал размытия т переходов
- •4.1.2. Экспериментальные данные [28, 30]
- •4.1.3. Оценка величины "кванта превращения" при других переходах
- •4.1.4. Размытость "концентрационных фазовых переходов"
- •4.1.5. "Надмолекулярный" характер соединений в твердом теле
- •4.1.6. Устойчивость соединений. Выделение химического и структурного слагаемых в энергии взаимодействия
- •4.2. Неоднородность течения реальной жидкости. Зернистая структура и соотношение коэффициентов вязкости и диффузии
- •4.2.1. Неоднородность течения
- •4.2.2. Оценка размеров "блоков течения" в жидкости
- •4.3. Наследование зернистой структуры при плавлении и кристаллизации
- •4.3.1."Наследственность"
- •4.3.2. Потоковая обработка
- •4.3.3. Термовременная обработка жидкого металла (тво) [24, 25]
- •4.3.4. Зародышеобразование и кинетика кристаллизации
- •4.3.5. Микронеоднородность эвтектических расплавов
- •4.3.6. Влияние слабых полей. Ультразвуковая обработка
- •4.3.7. Жидкий кристалл
- •4.3.8. Зависимость свойств поликристалла от размера зерна. Сверхпластичность. Дисперсионное упрочнение
- •4.4.9. Микрокристаллитная и коллоидная модель стекла
- •4.3.10. Состояние вопроса
- •4.4. Заключение к главе 4
- •Глава 5. Структурные дальнодействия и поверхностные явления
- •5.1. Дальнодействия в пленках и коллоидах
- •5.1.1. Дальнодействия в модели
- •5.1.2. Опытные данные по пленкам
- •5.1.3. Вязкие коллоиды и гели
- •5.1.4. Обсуждение опытных данных. Состояние вопроса
- •5.2. Дальнодействия в твердом состоянии
- •5.2.1. Масштабный фактор прочности
- •5.2.3. Дисперсионное упрочнение
- •5.2.4. О морфологии включений, фаз эвтектики, растущих кристаллов
- •5.2.5. Эффект ребиндера
- •5.2.6. Ориентирующие взаимодействия кристаллов
- •5.3. Выделение вклада дальнодействий в поверхностном натяжении
- •5.3.1. Дальнодействия, толстые пленки и их вклад в поверхностное натяжение
- •5.3.2. Термодинамические функции взаимодействия
- •5.3.3. Энтропия взаимодействия и оценки плотности упаковки, степени квантовости
- •5.3.4. Модель разорванных связей
- •5. 3. 5. Электронные теории поверхностного натяжения
- •5. 3. 6. Уточнение формулы для поверхностного натяжения чистых жидкостей
- •5.3.7.Поверхностное натяжение растворов
- •5.3.8.Аномально высокая поверхностная активность
- •5.3.9. Межфазное натяжение
- •5.3.10.Выделение вклада структурных дальнодействий и толстых пленок в поверхностное натяжение. Граница кристалл-жидкость в однокомпонентной системе
- •5.3.11. Граница кристалл-газ. Межзеренные границы
- •5.3.12. Зависимость температуры кристаллизации от размера капельки
- •5.3.13. Решетка и огранка малых частиц
- •5.4. Спекание и смачивание. Роль структурных дальнодействий и толстых пленок
- •5.4.1. Кинетический акт в традиционной модели
- •5.4.2. Кинетический акт спекания и смачивания в предлагаемой модели. Трение
- •5.4.3. Опытные данные по скорости самого акта спекания (кинетического звена)
- •5.4.4. Кинетическое сопротивление растеканию
- •5.4.5. Транспортное сопротивление спеканию и смачиванию.
- •5.5. Поверхностные свойства и дальнодействующие структурные
- •Глава 6. Корреляция параметров затвердевания и стабильности структуры с приведенной температурой и с мерой квантовости.
- •6.2.Превращения в начале и конце интервала затвердевания.
- •6.2.1. Начало интервала затвердевания или переход от состояния простой жидкости к состоянию реальной (затвердевающей) жидкости.
- •6.2.2. Конец интервала затвердевания.
- •6.2.3. "Точка стеклования" кристаллических веществ.
- •6.3.Общая сxема изменения кинетических свойств.
- •6.3.1. Общая схема изменения кинетических свойств при стекловании и кристаллизации.
- •6.3.2. Общий вид и истолкование политерм вязкости. Состояние вопроса.
- •6.3.3. Описание затвердевания в терминах вязкости и прочности. O качественном различии жидкости и твердого тела.
- •6.3.4. Тепловой эффект, сопровождающий повышение вязкости.
- •6.3.5. Химические классы жидкостей и стадии затвердевания.
- •6.4. Влияние атомарных квантовых эффектов.
- •6.4.1. Затвердевание и “степень квантовости”.
- •6. 4. 2. Влияние квантового параметра на tемпературу плавления.
- •6.5. Аналогичные закономерности для скорости химических реакций.
- •6.5.1. Подобие закономерностей для стабильности межмолекулярной и внутримолекулярной структуры. Постановка вопроса.
- •6.5.2. Зависимость стабильности внутримолекулярной структуры и “степени молекулярности” от квантового параметра.
- •6.5.3. Переходы от молекулярной формы к атомарной. Стёкла как промежуточные состояния.
- •6.5.4.Размягчение внутримолекулярной структуры при нагреве. Температурная зависимость энергий активации химических реакций.
- •6.5.5.Другие закономерности. Усреднение степени молекулярности компонентов раствора и катализ.
- •6.5.6. Перераспределение суммарной стабильности между внутри- и межмолекулярной структурой.
- •6.5.7. Перераспределение жесткости структуры и термодинамические характеристики плавления молекулярных веществ.
- •6.5.8.Простая атомарная многокомпонентная жидкость.
- •6.6. Заключение. Состояние вопроса.
- •6.6.1. Основные результаты.
- •7. Резюме.
- •Часть 2. - м.: Металлургиздат, 1966, 720 с.
6.3.3. Описание затвердевания в терминах вязкости и прочности. O качественном различии жидкости и твердого тела.
Реологическое поведение твердого тела обычно характеризуют величиной прочности, а в качестве реологической характеристики жидкости используют вязкость. Тем самым и здесь подчеркивается, как отмечено выше, противоположность свойств жидкости и твердого тела: жидкость не сохраняет формы, не имеет прочности, "уступает всякой силе", причем скорость течения V пропорциональна напряжению : V=/h, рис. 6.13., прямая I. Твердое тело, наоборот, даже при больших нагрузках сохраняет неизменную форму; если же нагрузка превышает предел прочности пч, то наступает разрушение, рис. 6.13, кривая II. Жидкость не имеет прочности, к твердому неприменимо описание через вязкость, в этом смысле их реологические свойства противоположны, качественно различны, и не могут быть выражены в одних единицах.
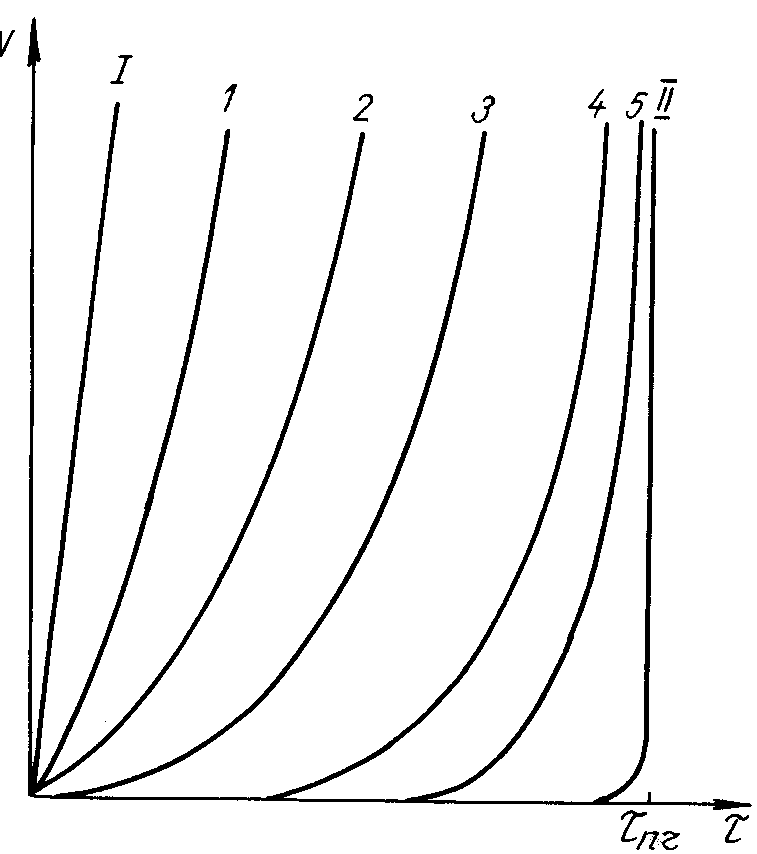
Рис. 6.13. Зависимость скорости течения V от нагрузки t. I-жидкостное поведение, II-твердотельное, 1-5 - последовательные промежуточные стадии, которые проходит реальная жидкость при охлаждении в интервале затвердевания.
На рис. 6.13 это качественное различие выражается различным характером зависимостей I и II в координатах V- .
Однако в настоящее время становится ясно, что в интервале затвердевания вещество и по этим характеристикам непрерывно переходит от типично жидкостной зависимости I к типично твердотельной II через все промежуточные стадии 1,2....5, рис. 6.13. У жидкости по мере повышения вязкости и соответствующего увеличения действующих нагрузок все более заметной становится зависимость вязкости или скорости течения от усилия. По мере охлаждения жидкость становится все более неньютоновской, ее вязкость - непостоянной, а зависимость V( - все более искривленной, рис. 6.13. Имеющиеся опытные данные по силикатным расплавам удовлетворительно описываются из условия: напряжение влияет на вязкость так же, как давление Р, и пропорционально влиянию на Sвз [7]: d/d: d/dT = dSвз/dP : dSвз/dT
Если же двигаться от противоположного предельного случая, от "абсолютно твердого тела", то при нагреве становится все более заметным течение и "временной аспект разрушения" - большая нагрузка приводит к более быстрому разрушению. В кинетической теории прочности [76] такая зависимость V (или ) от нагрузки описывается экспоненциальной формулой Журкова: V = Vо*exp(E-qv)/RT
В переходной области оба описания согласуются, "смыкаются", [76]. Таким образом, описание реологических свойств в интервале затвердевания через вязкость или через прочность становятся практически эквивалентными, если учесть зависимость вязкости от нагрузки и "временной аспект" разрушения или течения твердого тела. По этим характеристикам также выявляется непрерывный переход от жидкостного поведения к твердотельному через все промежуточные стадии.
Можно, вероятно, подобным же образом "сомкнуть" описание разрушения твердого тела и хрупкого разрушения жидкости при ударе [80].
6.3.4. Тепловой эффект, сопровождающий повышение вязкости.
Согласно традиционным представлениям, затвердевание обусловлено обычными межмолекулярными или межатомными химическими связями. Тепловой эффект затвердевания - это теплота кристаллизации, то есть перехода беспорядок - порядок; она обусловлена увеличением числа связей, или увеличением координационного числа, например, от (10 -11) до 12 и, соответственно, ростом энергии межатомного взаимодействия примерно на 1/10, Hпл 10-1Uвз. Теплота кристаллизации стекла с этой точки зрения примерно равна теплоте кристаллизации равновесной жидкости при Т = Тпл. При затвердевании в форме стеклования координационное число обычно почти не изменяется, и, следовательно, теплота процесса незначительна. Затвердевание в форме стеклования происходит без появления каких-либо новых взаимодействий, объясняется, например, уменьшением свободного объёма без изменения энергии взаимодействия, как в модели жёстких сфер. Следовательно, нарастание вязкости не сопровождается тепловым эффектом, если оно не совпадает с упорядочением; затвердевание в форме стеклования не является размытым фазовым переходом.
Исходя из предлагаемой модели, мы приходим по всем этим вопросам к противоположным выводам. В этой модели теплота затвердевания связана не с упорядочением, а с ростом интенсивности стабилизирующих структуру эффектов Fст и должна выделяться в тех температурных интервалах, где наиболее интенсивно возрастают ЕV, ln, Fcт, необязательно при упорядочении. Затвердевание в форме стеклования обусловлено появлением новых эффектов "взаимодействия" - стабилизирующих структуру сил Fст, и должно сопровождаться примерно таким же тепловым эффектом, как и кристаллизация жидкости; наоборот, теплота H кристаллизации стекла должна быть незначительной, H<<Hпл. Теплоёмкость при стекловании должна давать максимум, площадь которого примерно равна теплоте кристаллизации. Опытные данные в основном подтверждают эти следствия предлагаемой модели.
Действительно, у стёкол, особенно у стабилизированных и отожжёных, термодинамические свойства почти равны соответствующим свойствам кристалла [10], теплота их кристаллизации мала, H<<RTпл. Если разделить повышение вязкости и упорядочение, провести затвердевание как стеклование с последующей кристаллизацией стекла, то основная часть тепла действительно выделяется при повышении вязкости, а не при упорядочении; тепловой эффект приходится на область твердения структуры, роста Е, ln, но не на область увеличения координационного числа.
Отметим что оценка теплового эффекта кристаллизации по изменению координационного числа Z нередко кажется убедительной, а её ошибочность - странной. Однако подобные оценки и в других случаях дают неудовлетворительные результаты. Так, для перехода -Fe в -Fe при 1400 oС координационное число Z изменяется от 8 до 12, расчётная теплота получается 50 ккал/моль; в действительности H - 0,15 ккал/моль. Уменьшение числа связей практически полностью компенсируется увеличением энергии каждой остающейся связи.
Максимум теплоёмкости, соответствующий стеклованию, нетрудно проследить в случае легко переохлаждаемых жидкостей, таких как силикатные расплавы, глицерин, полимеры и др., см. рис.6.14. Площадь под таким максимумом ( заштрихована на рис. 6.14. ) даёт величину теплоты стеклования, которая примерно равна теплоте плавления. Удовлетворительные результаты даёт оценка высоты максимума стеклования по его известной площади, то есть по формуле С Hпл/(Tпл - Tст) .
Для кремнезёма эта оценка даёт несколько заниженное значение высоты максимума теплоёмкости С , для глицерина - завышенное. У рассматриваемых легко переохлаждающихся жидкостей теплоты плавления обычно невелики, и максимумы теплоёмкости при стекловании получаются невысокими. Вид максимумов часто искажается тем, что они совпадают с областью квантового понижения теплоёмкости при охлаждении. С другой стороны, такое наложение ещё раз наглядно подтверждает тот факт, что затвердевание происходит в области значительной величины квантовых эффектов (рис. 6.14.).
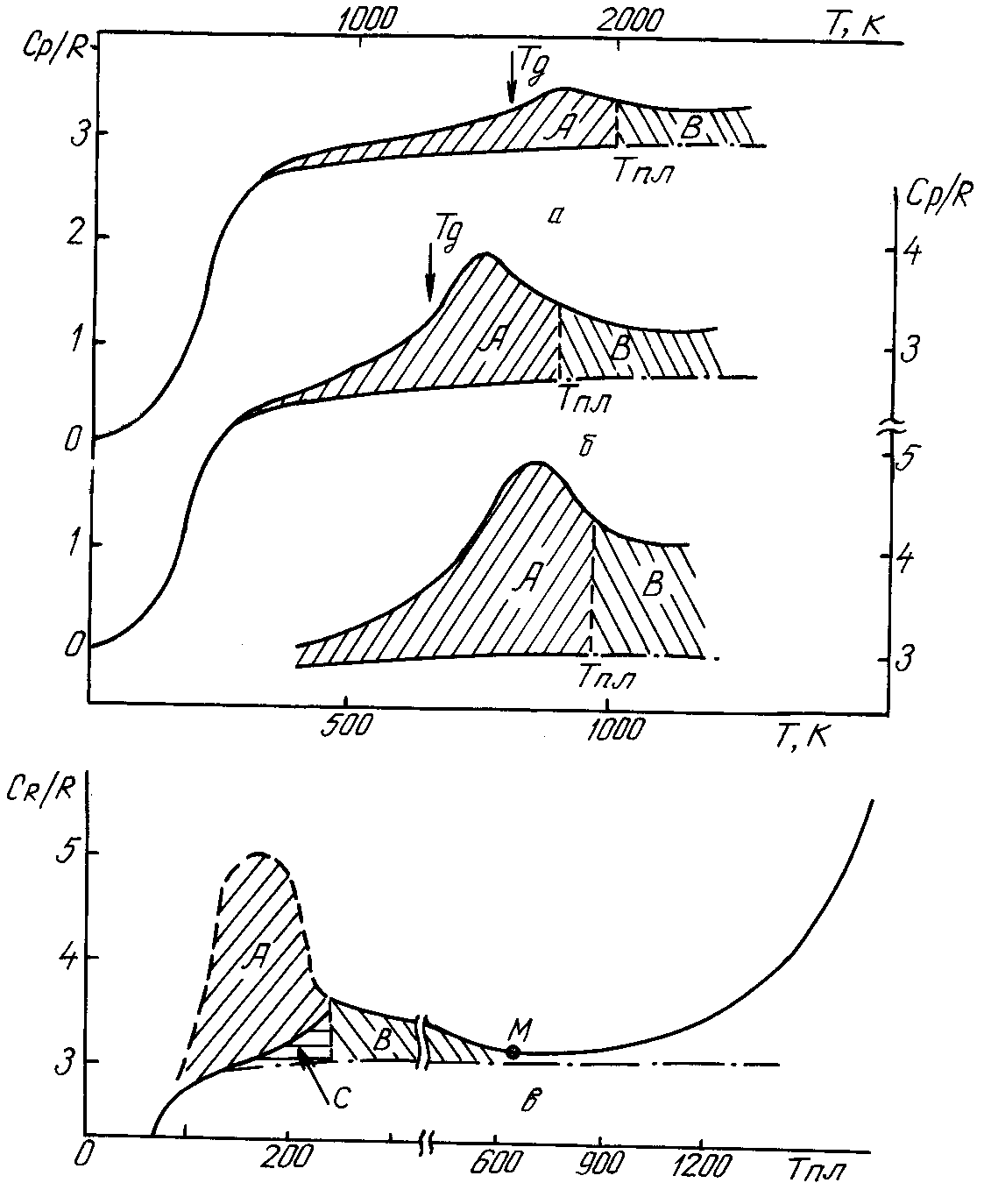
Рис. 6.14-1. Максимумы теплоемкости, соответствующие стеклованию. Вверху-кварц, кремнезем(а), стекло (б); внизу - ртуть (в).
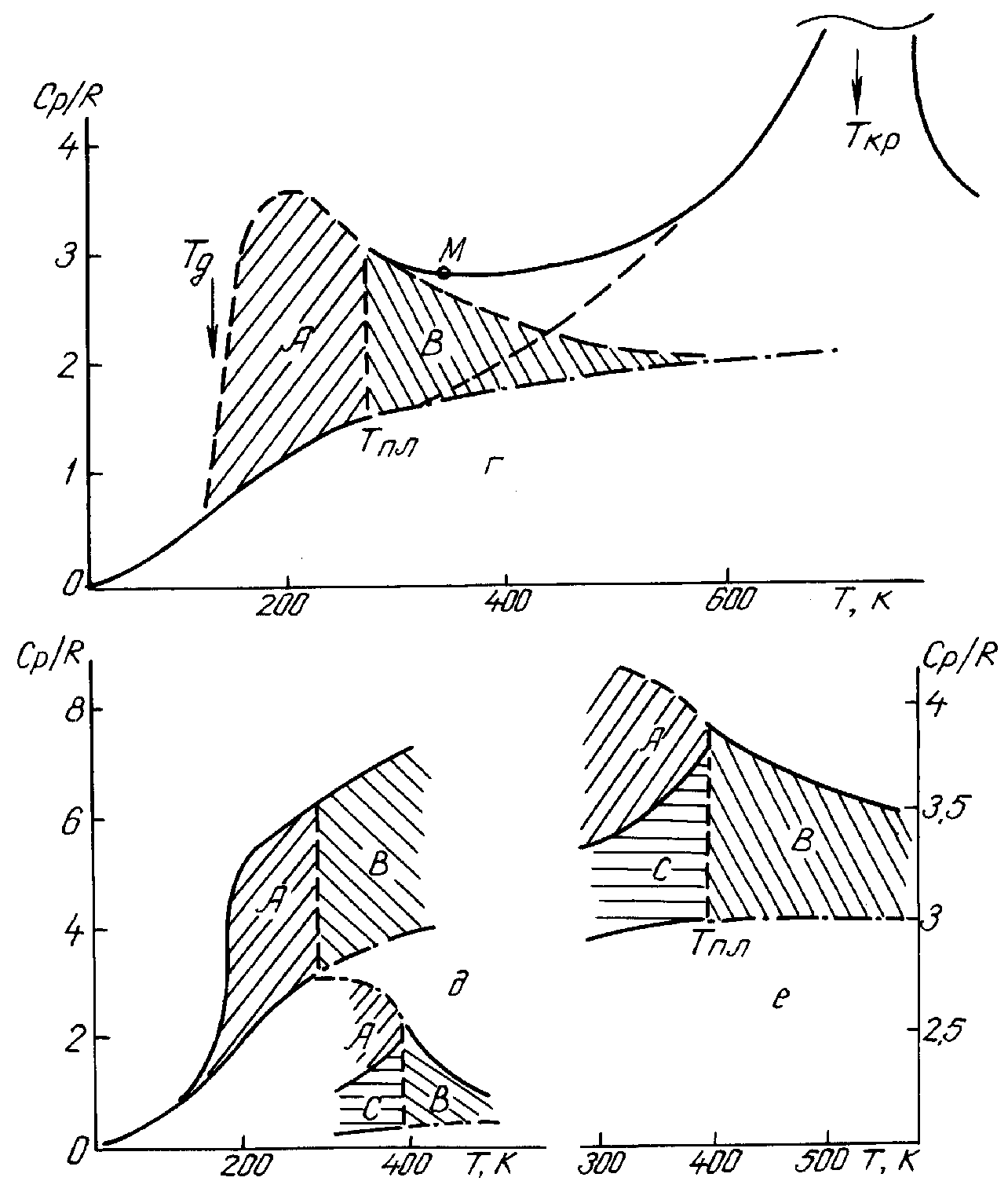
Рис.6.14-2. Максимумы теплоёмкости при стекловании. г)- вода, д)-натрий, е)- глицерин и полиэтилен. Данные справочников [9,10] . Сплошные линии - эксперимент , штриховые - расчёт, штрих пунктир - теплоёмкость в отсутствие явлений затвердевания. Площадь А выражает теплоту стеклования; В- теплоту нарастания вязкости непростой жидкости выше Тпл; С- теплоту "твердения" или "стеклования" закристаллизованного вещества. Второй максимум у ртути и воды относится к критическим явлениям - соответствует критической точке, причём у воды два максимума не разделены полностью и в значительной мере накладываются.
У жидких металлов и других легко кристаллизующихся жидкостей теплоёмкость их в переохлаждённом состоянии неизвестна, но максимум теплоёмкости при стекловании можно достаточно уверенно построить, зная его площадь (Hпл) и оценку высоты (C Hпл/(Tпл-Tст)); кроме того, часть восходящей и ниспадающей ветвей такого максимума обычно удаётся проследить по имеющимся опытным данным, см. рис. 6.14.
На подобных графиках часто можно выделить и теплоту равновесного затвердевания жидкости выше точки плавления ( заштрихованная площадь "А", рис. 6.14 ) примерно равную энергии стабилизирующих "взаимодействий" в точке плавления. У кремнезёма, как отмечено выше, эта часть является основным слагаемым всей теплоты затвердевания; большая часть тепла затвердевания поглощается ещё до точки плавления; большая часть нарастания Е, ln также происходит здесь. Площадь "Б" рис. 6.14 выражает часть теплоты затвердевания, приходящуюся на кристаллическое состояние, то есть на рост Е, Fст и жесткости структуры при охлаждении кристалла от точки плавления до конца интервала затвердевания, от Т = Тпл до Т 0.8Тпл, на обсуждавшемся интервале "затвердевания" кристалла длиною, например, 100-300К.
"Нормальная" теплоёмкость жидкости С, не искажённая стабилизирующими эффектами, определяется плавной экстраполяцией графика теплоёмкости кристаллического вещества; теплоёмкость С можно оценить также как С = Сп + R/2; здесь Сп - теплоёмкость паров. Такая нормальная теплоёмкость при небольшой величине квантовых эффектов близка к 3R , (правило Дюлонга-Пти), и несколько возрастает при нагревании. Там, где при охлаждении начинается интервал затвердевания, теплоёмкость проходит через минимум, аномально возрастает при охлаждении и становится значительно больше нормальной величины. У воды такой минимум теплоёмкости наблюдается около 37oС, у ртути около 300oС см. рис.6.14. Теплоёмкость воды сильно завышается также из-за того, что максимум стеклования у неё в значительной степени накладывается на максимум кипения-критического перехода, рис. 6.14в). У металлов, в частности, у ртути, эти максимумы обычно разделены, и теплоемкость между ними опускается до нормальных значений С 3R Cп+R/2, рис. 6.14б).
Таким образом, теплоёмкость повышена во всех интервалах, где при охлаждении нарастает энергия активации, вязкость и др., где происходит затвердевание - в равновесной непростой жидкости выше точки плавления, в переохлаждённой жидкости, особенно около точки стеклования, в кристаллическом состоянии несколько ниже точки плавления, где ещё продолжается рост Е, Fст. Существование максимумов теплоёмкости при стекловании ещё недостаточно осознано, особенно у легко кристаллизующихся жидкостей.
Если жидкость сначала стеклуется, и лишь затем стекло кристаллизуется, то почти всё затвердевание ( рост Е ) происходит в интервале существования одной - неупорядоченной фазы. Затвердевание и упорядочение разделяются, и основная часть теплового эффекта и в этом случае приходится на стадию затвердевания - роста Е, ln , Fст.
Затвердевание и упорядочение разделены также в системах с образованием жидких кристаллов, причём здесь наоборот, при охлаждении сначала происходит упорядочение - переход неупорядоченной жидкости в жидкий кристалл с незначительным тепловым эффектом. Затвердевание - превращение жидкого кристалла в твёрдый - происходит в интервале существования одной упорядоченной фазы и может не изменять характер дальнего порядка; тепловой эффект почти весь приходится на эту стадию и имеет величину, обычную для кристаллизации. Тепловой эффект и в этих системах в основном приходится на стадию затвердевания, а не упорядочения. Представления традиционной модели не подтверждаются. Приведённые факты согласуются с предлагаемой моделью в том, что теплота затвердевания связана не с изменением координационного числа и других параметров обычных взаимодействий; тепловой эффект затвердевания выражает появление дополнительных стабилизирующих структуру "взаимодействий" в тех интервалах температуры, где возрастают Е, ln и жёсткость структуры. При этом опытные данные позволяют выделить максимум теплоёмкости стеклования и теплоту этого процесса, а также отдельно теплоты нарастания вязкости (затвердевания) выше и ниже точки кристаллизации, в области соответственно жидкого и кристаллического состояния.
Отмеченные здесь противоречия традиционной теории с опытными данными в основном не замечаются, или они не осознаны еще в такой степени, на которой начинаются ожесточенне столкновения теоретиков и экспериментаторов, как аналогичные противоречия по квазикристаллическим свойствам (глава 3). Известна, однако, длительная дискуссия по вопросу: не следует ли рассматривать стеклование как фазовый переход второго рода [54]? В рамках традиционной модели на этот вопрос получается отрицательный ответ. Но появление или "включение" качественно иных стабилизирующих структуру взаимодействий, а также образование характерных -максимумов теплоёмкости является аргументом в пользу того, что стеклование является фазовым переходом, хотя и очень размытым по температуре.
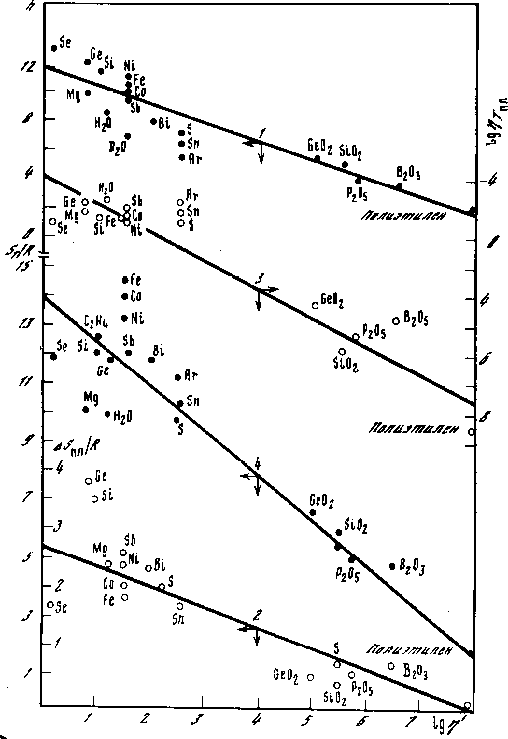
Рис.6.15 Кореляции энтропии взаимодействия (1), полной энтропии Sп/R (4), вязкости жидкости в точке плавления lghТпл (3) и величины DSпл (2) со сдвигом вправо lgh1 в веере линий кореляции рис. 6.6.
