
- •4.Выделение н-парафиновых углеводородов из нефтяных фракций с помощью цеолитов. Целевые направленности процесса. Характеристика стадий гидроочистки сырья, адсорбции и десорбции н-парафинов
- •1). Адсорбционное разделение при изомеризации
- •3). Депарафинизация бензина и кгф с целью получения н-парафинов (для нхс) и кондиционного топлива
- •6. Методы очистки выделенных из нефтяных фракций н-парафинов от примесей ароматических углеводородов Методы очистки выделенных из нефтяных фракций н-парафинов от примесей ароматических углеводородов.
- •7.Производство изопарафиновых углеводородов каталитической изомеризацией н-парафинов. Химизм и механизм изомеризации. Промышленные процессы и их основные показатели.
- •8. Технологическая схема процесса изомеризации н-бутана «Бутамер». Технологическая схема процесса изомеризации пентан-гексановой фракции фирмы British Petroleum.
- •11.Получение циклогексана каталитическим гидрированием бензола. Химизм и термодинамика процесса. Типы используемых катализаторов, требования к сырью.
- •12.Условия, показатели и технология процессов гидрирования бензола в циклогексан. Типы реакторов, методы теплоотвода. Схема гидрирования бензола в циклогексан в трубчатом реакторе.
- •Металлические катализаторы.
- •Сульфидные катализаторы
- •Технология
- •13. Схема процесса производства цг фирмы Atlantic Richfield. Схема гидрирования бензола в цг с рециркуляцией цг.
- •14. Схема гидрирования бензола в циклогексан с отводом тепла реакции поддувом циркулирующего газа.
- •15.Приципиальная технологическая схема установки по производству циклогексана по методу фин. Схема процесса пр-ва цг, разработанного фирмой Haines Associates.
- •20. Производство высших линейных олефинов каталитическим дегидрированием н-парафинов (химизм, термодинамика, условия и особенности технологии процесса). Процесс «Пакол-Олекс» фирмы uop.
- •21. Технологическая схема процесса «Пакол-Олекс».
- •22. Получение высших линейных а-олефинов каталитической олигомеризацией этилена в присутствии катализаторов Циглера. Химизм, технология, условия и показатели процессов.
- •23. Схема «Альфрен» с рециркуляцией AlR3. Схема производства линейных а-олефинов с чётным числом углеродных атомов методом фирмы Gulf Research.
- •24.Получение высших линейных а-олефинов олигомеризацией этилена в присутствии комплексных металлоорганических катализаторов. Условия и технология процесса.
- •25. Схема получения высших линейных а-олефинов низкотемпературной олигомеризацией этилена методом фирмы Mitsui Petrochemical.
- •26.Получение высших линейных а-олефинов и олефинов нормального строения с внутренним положением двойных связей методом фирмы Shell (схема с блоками изомеризации и диспропорционирования олефинов).
- •30.Технологическая схема дегидрирования этилбензола(1). Технологическая схема дегидрирования изопропилбензола(2).
- •1) Рис. 120. Техн схема производства стирола. Аппараты :
- •2) Рис. 86. Техн схема производства альфа-метилстирола. Аппараты :
- •31. Принципиальные схемы разделения катализатов дегидрирования эб и ипб.
- •31. Применение стирола и альфа-метилстирола
- •35. Разделение ароматических углеводородов с6-с8. Проблемы разделения фракции с8. Выделение п-ксилола методами фракционной кристаллизации и адсорбции цеолитами..
- •37Схема фракционной кристаллизации. Рис. 5.25.
- •36. Поточная схема производства и разделения ароматики.
- •1)Процесс фирмы ici
- •39.Процесс «xis» (включая его технологическую схему).
- •40.Изомеризация алкилароматических углеводородов. Процесс «Octafming» (условия,, показатели, технологическая схема). Процесс «Isomar».
- •42.Катализаторы, условия и показатели процесса каталитического гидродеалкилирования толуола (и ксилолов). Технология гидродеалкилирования. Типы реакторов, способы теплоотвода.
- •43 Схема уст термического гда толуола по методу фирмы Мицубиси Схема процесса кат гидродеалкилирования толуола
- •44.Гидродеалкилирование бензина пиролиза. Схема переработки пиролизного бензина с получением ароматических углеводородов.
- •46 Схема установки гда бензина пиролиза (had)
- •48.Показатели процессов термического и каталитического гидродеалкилирования алкилнафталинов. Схема процесса «Юнидак». Схема полочного реактора и температурная кривая гидродеалкилирования.
- •49.Производство бензола и нафталина конверсией водяным паром соответствующих алкилароматических углеводородов (химизм, катализаторы, условия и показатели процессов).
- •49.Производство бензола и нафталина конверсией водяным паром соответствующих алкилароматических углеводородов (химизм, катализаторы, условия и показатели процессов).
- •50.Каталитическое диспропорционирование алкилароматических углеводородов. Химизм, катализаторы, условия, технология и показатели процессов диспропорционирования толуола.
- •53.Условия, технология и показатели процесса алкилирования бензола пропиленом в присутствии а1с1з.
- •54. Принципиальная схема алкилирования бензола пропиленом. Общий вид алкилатора. Схема разделения алкилата.
- •55.Получение изопропилбензола алкилированием бензола пропиленом на твердом фосфорнокислотном катализаторе. Условия, технология, показатели, преимущества и недостатки процесса.
- •57.Производство высших алкилбензолов алкилированием бензола высшими олефинами (или высшими хлорпарафинами). Условия, технология и показатели процесса. Схема разделения алкилата.
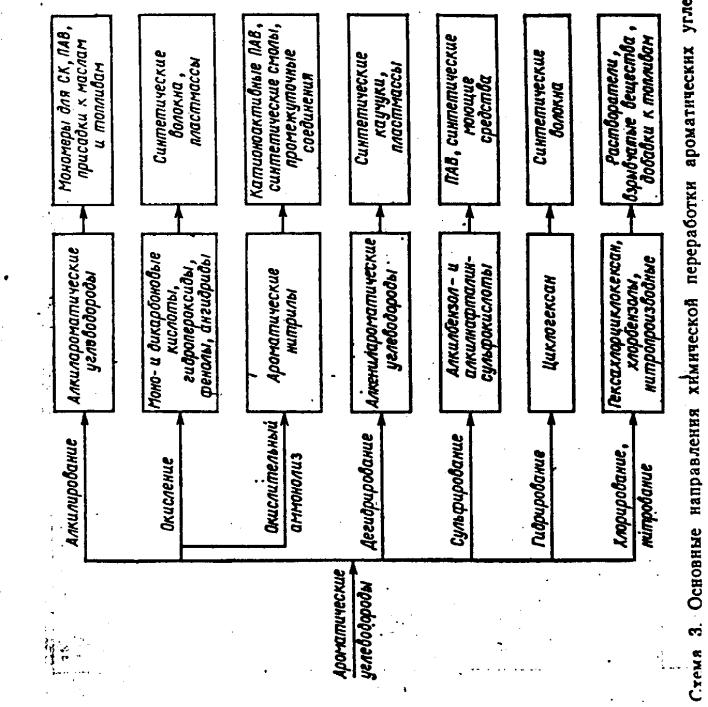
- •58. Основные направления химической переработки ароматики
- •Инициирование
- •Продолжение цепи
- •Вырожденное разветвление
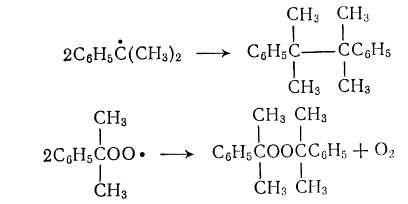
- •Обрыв цепи
- •68. Технология (типы реакторов, способы отвода тепла), условия, показатели стадии окисления ипб в гп ипб. Способы разделения оксидата.
- •70. Технологическая схема стадии окисления ипб и кислотного разложения гп ипб.Применение гп ипб, фенола и ацетона.
- •71. Получение бензойной кислоты жидкофазным окислением толуола. Химизм, механизм, условия и показатели процесса. Технологическая схема производства бензойной кислоты окислением толуола.
- •72. Жидкофазное окисление п-ксилола в терефталевую кислоту. Химизм, катализаторы, условия, технология и показатели двухстадийного совмещённого процесса.
- •73. Окисление циклогексана в смесь циклогексанона и циклогексанола в присутствии солей кобальта. Химизм, условия, технология и показатели процесса. Применение циклогексанона.
- •73.(Продолжение) Окисление циклогексана в смесь циклогексанола и циклогексанона в присутствии борной кислоты. Химизм, условия, технология и показатели процесса.
- •74. Окисление циклогексана в адипиновую кислоту. Химизм, катализаторы, условия, технология и показатели второй стадии двухстадийного процесса.
- •75. Газофазное окисление нафталина и о-ксилола во фталевый ангидрид. Химизм, катализаторы, условия, показатели, технология.
- •76. Газофазное окисление бензола в малеиновый ангидрида. Химизм, катализаторы, условия, показатели, тезнология.
- •77. Производство вжс каталитическим гидрированием сжк и их эфиров.
- •78. Технология гидрирования эфиров сжк. Стадии промышленного процесса. Принципиальная технологическая схема гидрирования метиловых эфиров сжк в реакторах со стационарным слоем катализатора.
- •79. Технологическая схема прямого гидрирования сжк в высшие спирты в суспендированном слое.
- •81. Выделение вжс из вторых неомыляемых производства сжк. Сырьевая база. Методы выделения и их сущность. Условия и показатели процесса.
- •83. Производство вжс алюминийорганическим синтезом. Стадии промышленного процесса. Их химизм, условия, технология, показатели.
- •1. Синтез триалкилалюминия осуществляется 3 способами:
- •84. Поточная схема получения вжс алюминийорганическим синтезом. Применение вжс.
- •85. Структура молекул пав
- •86. Физико-химич основы и мех-м действия пав и Моющ вешеств
- •88. Схема пр-ва Сульфонола нп-3
- •90. Схема получения альфа-олефинсульфонатов.
- •97. Технологическая схема получения алкилсульфонатов натрия сульфоокислением н-парафинов.
- •98. Схема производства вторичных алкилсульфатов натрия
- •99. Схема сульфатирования спиртов или сульфирования алкилбензолов фирмы Balestra.
57.Производство высших алкилбензолов алкилированием бензола высшими олефинами (или высшими хлорпарафинами). Условия, технология и показатели процесса. Схема разделения алкилата.
Алкилбензолы, получаемые алкилированием бензола высшими а-олефинами, применяются для производства поверхностно-активных веществ.
Катализатор хлористый алюминий.
Алкилирование может проводится в присутствии алюмосиликатов, серной и фосфорной кислот, фтористого бора и хлорида алюминия.
Технология.
Хлорид алюминия вводится в количестве 8-10% от алкилата. Потери его не превышают 1,5-2%. Промотор соляная кислота.
Алкилирование бензола производится в алкилаторе, представляющий собой пустотелый аппарат колонного типа. Поскольку среда коррозионная, реактор футерован графитовыми плитками, перемешивание которых осуществляется самим газом. Отвод тепла экзотермической реакции осуществляется за счет испарения части бензола, выходящего из алкилатора вместе с отходящими газами. При последовательном охлаждении газа бензол конденсируется и вновь возвращается на алкилирование. Температуру в алкилаторе регулируют степенью насыщения отходящего газа бензолом, а количество испаряющегося бензола зависит от давления в алкилаторе. R
С6Н6+RCH=CH2
С 6Н6-CH
CH3
Условия процесса:
мольное соотношение бензол : олефин = 7,5:1;
температура 45—50°С;
Р=0,2 МПа;
время контакта 45—50 мин.
Выход целевой фракции алкилата (280—340°С) составляет 87—90% на исходные олефины.
 Схема
разделения алкилата
Схема
разделения алкилата
аппаратура:
1,2,3,4, – ректификационные колоны под атмосферным давлением, 5-вакуумная колонна
Потоки:
I – алкилат; II – бензол на алкилирование (рецикл)
Из 2й колонны сверху выходит:ИПБ, ЭБ. ББ
III – полиалкилбензол, ДИПБ-на возврат
IV – тяжелые примеси, смолы; V – ЭБфракция.
VI – товарный алкилбензол
VII – ББ фракция
58. Основные направления химической переработки ароматики
61. Окисление высших н-парафинов С20-С40 в синтетические жирные кислоты (СЖК). Характиристика сырья. Ингибиторы окисления. Способы очистки сырья. Схема химических превращений, протекающих в процессе окисления н-парафинов в СЖК.
Окисление проводят с целью получения монокарбоновых кислот C10-C20 нормального строения.
Сырье:
Для производства СЖК применяются глубокообезмасленные (масла менее 0,5-1 %) и технические (масла 1—5 %) парафины (t пл. от 28 до 60—70°С), которые, в свою очередь, подразделяются на низкоплавкие (Тпл 28—45 °С), среднеплавкие (Тпл45—60°С) и высокоплавкие (Тпл 60°С и выше).
Применяются в основном среднеплавкие и твердые парафины, но в последнее время применяются и низкоплавкие (жидкие) парафины (примерно 5—10 % к общему потреблению парафинов).
Для производства СЖК вырабатываются три марки парафинов Т, С и Ж, отличающиеся физико-химическими свойствами в зависимости от происхождения и способа получения;
Выход сырых кислот при окислении парафинов различного происхождения растет с повышением темп кипения и средней мол массы исх парафина, растет среднее число атомов углерода в молекулах ЖК (обычно 60% от среднего числа атомов С в молекулах исх УВ). Из твердых парафинов в основном применяется парафин марки С (высокий выход целевых кислот).
Качество парафина в основном определяют примеси (нафтеновые, ароматические, ненасыщенные, насыщенные углеводороды изостроения, а также серосодержащие и высокомолекулярные соединения).
Наличие примесей существенно меняет скорость окисления, состав и выход образующихся кислот.
Ингибиторы окисления: серосодержащие и смолистые (полициклические ароматические углеводороды) соединения. Увеличение содержание н-алканов способствует улучшению показателей получаемых СЖК.
Способы очистки: сернокислотная или адсорбционная - для удаления аромат., гидроочистка - удаление олефинов.
Фракционный состав парафина, используемого в качестве сырья для производства СЖК, колеблется в довольно широких пределах. Вместе с тем, от него зависят скорость процессов окисления, отделения неомыляемых веществ и выход отдельных фракций жирных кислот.
Состав оксидата:
катализаторный шлам, нейтральные продукты, н-парафины С20 – С40, спирты С1 – С25, кислые продукты С1 – С25, монокарбоновые к-ты, сложные эфиры, кетоны, кетокислоты, оксикислоты, лактоны, дикарбоновые к-ты.
Расходные показатели (на 1 т к-т С10 – С20 )
Н-парафины – 1,2 ÷ 1,3 т, Сода - 0,42 т, Щелочь – 0,315 т, Серная к-та – 0,87 т, Отходы(сульфат натрия) – 1,2 т

62-64. Катализаторы, условия, технология и показатели процесса производства СЖК. Поточная схема производства СЖК окислением высших н-парафинов. Химические реакции, лежащие в основе разделения оксидата и облагороживания окисленной части парафина при производстве СЖК.
Условия:
Т=1100С, время конаткта 18-24часа, Р=0,2МПа, скорость w(воздуха)=40м3/т.ч., 170кг кислорода на окисление 1 тонны смеси парафина и неомыляемых возвратных соединений.
Показатели:
Суммарный выход кислот=80%
Катализатор:
марганцево-натриевые компоненты. В качестве Мn компонента катализатора используют оксиды марганца, гидроксид марганца и марганцевые мыла жирных кислот различных фракций. Na компонент катализатора—натриевые мыла кислот C1 — С4, C5 — С9 масляного конденсата, окисленного парафина, а также Na и K, содержащиеся в технических оксидах марганца. Гидроксид марганца и марганцевые мыла получают на основе сернокислого марганца или марганцевого шлама.
Механизм действия марганцевого катализатора обусловлен изменением его валентности под влиянием восстановительного характера углеводородной среды.
Марганцевый катализатор играет при окислении парафина двойную роль. В начальной стадии окисления он ускоряет процесс, инициируя цепную реакцию. В последующий период Mn-Na комплексы, растворенные в окисляемом парафине, ускоряют и регулируют процесс дальнейшего распада гидропероксидов и обеспечивают наиболее быстрое образование жирных кислот и минимальное накопление побочных продуктов.
Селективность процесса получения жирных кислот окислением парафинов повышается при использовании многокомпонентных Сг — Мn — К (1:1:1) катализаторов.
Технология процесса.
Процесс включает следующие стадии:
-приготовление катализатора;
-приготовление у/в-ной шихты для окисления;
-окисление у/в-ной шихты;
-шламоотделение и промывка оксидата от водорастворимых низкомолекулярных кислот;
-омыление оксидата и отделение 0-и1-ых неомыляемых;
-термическая обработка омыленного оксидата и отделение 2-ых неомыляемых;
-разложение мыльного клея (Na-солей жирных кислот);
-промывка сырых жирных кислот;
-дистилляция сырых жирных кислот.


Химические реакции, лежащие в основе разделения оксидата и облагороживания окисленной части парафина при производстве СЖК.
Состав оксидата:
Отработанный катализатор
Нейтрализованные продукты (н-парафины, спирты С1-С25)
Кислые продукты С1-С25 (монокарбоновые кислоты, сложные эфиры, кетоны, кетокислоты, оксикислоты, лактоны, дикарбоновые кислоты)
Омыление:
R COOН+Na2СО3 RCOONa+ NaНСО3
RCOOR’+ Na2СО3 RCOONa+R’OH + NaНСО3
RCOOН + NaНСО3 RCOONa + СО2 + Н2О
25 % раствор Na2СО3 Т=90-110 0С
Омыление оксидата осуществляется с целью превращения свободных и связанных ЖК в труднолетучие натриевые соли, что позволяет в дальнейшем отделить их от остальной части неомыляемых методом отстаивания и испарения.
RCOOН + NaОН RCOONa + Н2О
RCOOR’ + NaОН RCOONa+R’OH
25 % раствор щелочи, Т=90-110С, время контакта 1,5-2 часа
После разделения за счет разности плотностей омыленных и неомыленных продуктов отбирают одним из трех зондов возвращаемые на окисление 1-е неомыляемые. Продукты реакции образующие нижний слой в автоклаве подаются в ребристую трубчатку конвекционного типа, обогреваемой горячими газами (400-500ºС). Здесь – доомыление кетонов и лактанов (320-340ºС и 20-22 кгс/см2 )
R
O
 RCH2CHCH2CO
NaOH
RCH2CHCH2COONa
RCH2CHCH2CO
NaOH
RCH2CHCH2COONa
O
OH
А также дегидратация солей оксикислот в соли непредельных кислот:
r
 CH2CHCH2COONa
rCH=CHCH2COONa+
H2O
CH2CHCH2COONa
rCH=CHCH2COONa+
H2O
OH
Сода более дешевый агент, чем щелочь.
В последнее время предложена рационализация технологического процесса получения синтетических жирных кислот: применение для разложения натриевых солей жирных кислот (мыла) двуокиси углерода вместо серной, кислоты; извлечение спиртов в виде борнокислых эфиров из 2-х неомыляемых; выделение низкомолекулярных кислот Ci—С4 из кислых вод и, наконец, утилизация сульфата натрия.
При разложении мыла двуокисью углерода образуется «кислое мыло» и выделяется бикарбонат натрия:
2RCOONa + C02 —> [RCOOH + RCOONa] + NaHC03
„кислое мыло"
Необходимая для разложения двуокись углерода получается на стадии омыления окисленного парафина кальцинированной содой (карбонатом натрия). Образующийся при разложении мыла бикарбонат 'натрия превращается при нагревании до 95—105°С в карбонат натрия (возвращаемый на омыление окисленного парафина) с выделением дополнительного количества двуокиси углерода. В результате расход кальцинированной соды резко сокращается, а серная кислота требуется только для разложения солей, входящих в состав «кислого мыла». При разложении мыла двуокисью углерода даже па 60% расход серной кислоты снижается на 50%, а кальцинированной соды на 75%;. примерно вдвое уменьшается также количество образующегося сульфата натрия.
Высшие синтетические жирные кислоты нормального строения применяются в промышленпогти сиптстического каучука при проведении эмульсионной сополимеризации бутадиена и стироля (кислоты CI2 - CI6 И CI2 - CI4), а также при получении стереорегуляр. ных каучуков (кислоты Ср - С2о) и товарных латексов (кислоты C11 - CI4). Примеси непредельных кислот, вызывающих старение резиновых изделий, вежелагельны. Синтетические жирные кислоты используются также в шинной промышленности в производстве резинотехнических изделий. Они повышают пластичностъ резиновых смесей, способствуют лучшему диспергированию в них наполнителя (например, сажи) и облегчают процесс, бработки резиновых смесей.
Фракции кислот C17-C20 находят применение практически всюду, где использовался стеарин, получаемый из природных жиров, например для обработки лубяных изделий, Хлопчатобумажных тканей, в производстве бумаги. Перспективно использование синтетических жирных кислот в литейном деле и т. п.
ТЕХ Схема
В емкость 1 подаются кислая вода (из сборника 11) и 23-28%-ный раствор кальцинированной соды (или поташа). В результате образуются натриевые соли водорастворимых низкомолек.
улярных кислот RCOOH +Na2CO3→ RCOONа + Н2О + С02: После перемешивания в течение 0,5 ч в эту же емкость подаются 45-%ный раствор каустической соды и 25 %-ный раствор сернокислого марганца. Реакционная масса продувается в течение двух часов воздухом через барботер, образуется гидроксид марганца МnS04 + 2NaOH→Мn(ОН)2 + Na2S04.
После этого производят корректировку избытка щелочи, который должен составлять 0,2-0,5 % (масс.).
На установке предусмотрена регенерация марганцевых солей из производственных шламовых вод. С этой целью шламовые воды шламоотстойника 6 перекачиваются в аппарат 1', где происходит их обработка раствором кальцинированной соды
(RCOO)2Mn + Nа2СОЗ → МnСОз + RCOONa
Образовавшийся карбонат марганца осаждается, а осветленный раствор по переливной трубе сливается в канализацию кисых стоков (на схеме не показано) .
. 3.3. Схема производства синтетических жирных кислот Cs-C20:
- емкость для приготовления раствора катализатора; l' - емвэсть для выделения солей эгвнцв из шламовых вод; 2 - смеситель; 3 - окислительная колонна; 4 - конденсатор' - - ХО.10ДИЛЬИИК; 6 - шл амоотстойн ик: 7 - абсорбер; 8. 22 - промывныв колонны; 9 - га: пара-гор; 10 - отстойник; 11 - сборник кислой воды; 12 - барабаиные омылители; 13- яылитель: 14, 18, 21 - отстойникн-раэделители ; 15 - теплообменник; 16 - автоклав; 17- . бчатая печь; 17' - змеевик; 17" - отделитель с отпарной колонной; /9 - емкость для лвбавления мыльного клея (расклеиватель}; 20 - нейтралиаатор: 23 - колонна для обеэввания: 24, 25, 26, 27 - ректификационные колонны,
В этом же аппарате 1' карбонат марганца в смеси с маточным раствором обрабатывается раствором серной кислоты
МпСОз + H2S04 --+ MnS04 + Н2О + СО2
Раствор регенирированного сернокислого марганца в смеси с натриевыми солями жирных кислот самотеком поступает в емкость 1.
Приготовленный в емкости 1 10%-ный раствор катализатора поступает в смеситель 2, куда подается углеводородная шихта (свежий и возвратный парафин вместе с неомыляемыми в отношении 1:2).
Температура в смесителе поддерживается около 120С; вода испаряется, а катализатор диспергируется в парафине, после чего смесь поступает в окислительную колонну 3.
Промышленные окислительные колонны имеют высоту 8-12 м, диаметр 1-2 м, емкость от 30 до 60 м3, изготавливаются из кислотоупорной стали или алюминия.
В нижней части колонны 3 установлены распылители для воздуха и барботеры для пропарки колонны. По высоте колонны расположены обогревающий и три охлаждающих змеевика. В начал~ процесса температура в колонне 3 поддерживается около 120 С за счет подачи пара (ок 5 МПа) в обогревающий змеевик. После начала окисления обогрев прекращается, температура снижается до 110С и дальнейшее окисление проводится при постоянной температуре, которая поддерживается за счет подачи конденсата в охлаждающие змеевики. При достижении оксидатом кислотнотго числа, 65-75 мг КОН/г уменьшают подачу воздуха температуру оксидата снижают до 80-95С с прмощью охлаждающих змеевиков и увлажненного воздуха, для чего в трубопровод впрыскивается конденсат.
Охлажденный до 80-95С оксидат из окислительной колонны 3 через холодильник 5 поступает в шламоотстойник 6, а отходящий из колонны воздух, содержащии реакционную воду и ниэкомол-. кулярные органичесние Продукты, направляется сначала в конденсатор 4, а затем в адсорбер 7. В результате снижения температуры до 40С основная часть легкокипящих продуктов конденсируется. Оставшиеся в отработанном воздухе органические примеси сжигаются в контактной печи.
В шламоотстойник 6 подается кислая вода (из сборника 11) для отделения катализаторного шлама и водорастворимых кислот. Шламовая вода после отстоя подается на регенерацию солей марганца.
лители 12.
Из шламоотстойника 6 оксидат после разбавлення кислой водой подается в промывную колонну 8, где водной промывкой при 70-90С (50 частей воды на 100 частей оксидата) отделяют низкомолекулярные водорастворимые кислоты состава С1 - С4. Промытый оксидат с верха колонны 8 поступает в отстойник 10, где отделяется кислая вода, направляемая на получение катализатора. Промытый оксидат через теплообменник и эжектор смешения (на схеме не показаны) направляется на омыление в омылители 12. '
Процесс омыления оксидата осуществляется с целью превращения свободных и связанных жирных кислот в труднолетучие натриевые соли (мыла), что позволяет в дальнейшем отделить их от остальной части неомыляемых методом отстаивания и испарения.
Процесс омыления оксидата осуществляется в две стадии: 25%-ным раствором кальцинированной соды и 40 %-ным раствором едкого натра.
Основная цель первой стадии - замена едкого натра кальцинированной содой и достижение максимально возможной глубины омыления при минимальном содержании диоксида углерода, би-карбоната и карбоната натрия.
В омылителях 12, имеющих перемешивающее устроиство, неитрализуется основная часть жирных кислот и истинных сложных эфиров 25 % -ным раствором кальцинированной соды при 90- 110С. Химизм процесса содового омыления оксидата представляется следующими реакциями:
Образующийся диоксид углерода отдувается барботируемым паром. Реакционная масса из омылителей 12 по переливной трубе поступает в доомылитель 13, в который подается 25 % -ный раствор едкого натра. Перемешивание массы и поддерживание температуры 90-110°C осуществляется паром, подаваемым через барботер. В доомылителе происходит дальнеишее доомыление трудноомыляемых жирных кислот и их эфиров.
Парогазовая смесь (диоксид углерода, пары воды и ме~анически увлеченное мыло) из доомылителя 13 поступает в сеп~атор 9, из которого газы идут на сжигание, а конденсат возвращается в доомылитель 13. Реакционная масса из доомылителя 13 через переливную трубу поступает в отстойник 14 для частичного отделения в виде верхнего органического слоя непрореагировавшего парафина (0-х неомыляемых), который через верхний переток подается в сборник неомыляемых (на схеме не показан) и далее возвращается на окисление. Нижний слой из Отстойника 14 (раствор едкого натра, солей карбоновых кислот, их эфиров и др.) подается насосом под давлением 1,5-2 МПа через теплообменник 15 (где нагревается вторыми неомыляемыми до 130-150С) в печь 17.
Сконденсировавшиеся в теплообменнике 15 вторые неомылявмые из сборника неомыляемых направляются на выделение спиртов или на повторное окисление.
В последние годы термическая печь подверглась реконструкции. В настоящее время в термической печи 17 имеются: вертикально расположенный змеевик 17' (оребренная длина 7 м), заключенный в огнеупорную кладку; отделитель 17" вместе с отпарной колонной, газовые горелки и два эксгаустера для циркуляции дымовых газов. ПО вертикали печь разделена на две секции, работающих изолированно друг от друга. В каждой секции установлено по шесть инжекционпых газовых горелок, расположенных друг под другом, а для лучшего теплообмена дымовые газы каждой секции постоянно рециркулируются эксгаустером с подсосом необходимого количества свежего воздуха.
Трубчатка термической печи условно разделена на три температурные зоны: подогрева (130-200 ОС); выдержки (230-250 ОС) и испарения (340-380 ОС).
В последнее время увеличение степени извлечения неомыляемых достигается за счет повышения температуры в автоклаве не выше 180-200 ОС, а в отделителе термолечи до 3800с. водноно-мыльная эмульсия из теплообменника 15 прокачивается через зону подогрева термопечи 17, где нагревается до 180-200С и поступает в автоклав 16 для отделения 1-ых неомыляемых. После отделения 1-ых неомыляемых реакциониая масса последовательно проходит зоны выдержки и испарения термической печи и поступает в отделитель с отпарной колонной.
В печи при температуре 340-380С и давлении 2-2,5 МПа происходит доомыление кетонов, лактонов и кетокислот.
Температура паро-мыльной смеси на выходе из печи составляет 340-380С; температура мыла в отделителе 320-380С и температура мыла, выходящего из отпарной колонны 300-375С. Перегретые в трубчатке печи пары воды и 2-х неомыляемых, поступая в отделитель и отпарную колонну испаряются.
Кроме того, по выходе из печи 17 давление понижается до 022 МПа и происходит дополнительное испарение воды и 2-х неомыляемых. Пары поступают в отстойник-разделитель 18 где при 13 МПа происходит отделение увлеченных натриевых солеи жирных кислот (мыла) от паров воды и 2-х неомыляемых.
Натриевые соли жирных кислот оседают в нижнеи части разделителя 18 и непрерывно транспортируются в емкость 19 для разбавления мыльного клея (расклеиватель), в который поступает также «мыльный плав» из отделителя печи.
В емкости 19 расплавленное мыло -мыльный плав - охлаждается до температуры 70-95 С сульфатной водой и разбавляется до концентрации 25-30 %.
Полученный 25%-ный paствоp натриевых солеи жирных кислот так называемый мыльный клей подается в нейтрализатор 20, где происходит разложение солей (выделение свободных кислот] 92-96 % -й серной кислотой при 80-90С, по реакции:
2RCOONa + H2S04 →2RCOOH + Na2S04
В последнее время предложено применение для разложения натриевых солей жирных кислот (мыла) диоксида углерода вместо серной кислоты.
При разложении мыла диоксидом углерода образуется кислое мыло и выделяется бикарбонат натрия:
2RCOONa + СО2 →[RCOOH + RCOONa] + NаНСОз
”кислое мыло"
Необходимый для разложения диоксид углерода получается на стадии омыления окисленного парафина кальцинированнои содой (карбонатом натрия). Образующиися при разложении мылa бикарбонат натрия превращается при нагревании до 95-105С в карбонат натрия (возвращаемыи на омыление окисленного парафина) с выделением дополнительного количества диоксида углерода. В результате расход кальцинированнои соды резко сокращается, а серная кислота требуется только для разложения солей, входящих в состав кислого мыла. При разложении мыла
диоксидом углерода даже на 60%, расход сернои кислоты снижается на 50 %, а кальцинрованной соды - на 75 %; примерно вдвое уменьшается также количество образующегося сульфата натрия.
Выделившаяся смесь жирных кислот и сульфатная вода (10- 15 % сульфата натрия, 0,3-0,5 % свободной серной кислоты, 0,6-0,8 % нелетучих органических соединений, 0,01-0,02 % марганца и 0,003-0,005 % железа) поступают в отстойник 21, где происходит расслоение. Жирные кислоты (верхний слой) направляются на водную промывку в колонну 22, заполненную кольцами Рашига, а сульфатная вода отводится на станцию нейтрализации. Сырые Жирные кислоты из КОлонны 22 направляются на ректификацию для разделения на товарные фракции.
Сырые синтетические жирные кислоты представляют собой смесь гомологов нормальных монокарбоновых кислот от С4 до С25 (60-70 %), монокарбоновых кислот изостроения (15-25 %), дикарбоновых кислот (4-5%) и небольшого количества непредельных кислот, кето- и оксикислот и неомьiляемых продуктов. Разделение сырых жирных кислот осуществляется в пяти колонной системе непрерывной ректификации. В первой колонне-осушителе 23 производится отгонка при небольшом разрежении воды и кислот С1 - С4• Обезвоженные жирные кислоты последовательно поступают в колонны 24, 25, 26 и 27, где нижний продукт предыдушей колонны является сырьем для последующей. С верха каждой колонны отбирают определенную товарную фракцию кислот, соответственно С5 – С6, С7 – C9, С1О - С16; С17 - С2О. Кубовый остаток выводят в виде нижнего продукта последней колонны 27. Колонны 23, 24, 26 и 27 - колпачковые, колонна 25 заполнена керамическими кольцами. Суммарный выход товарных кислот составляет 78-80% (масс.) на исх парафин.
66. Производство фенола и ацетона кумольным методом. Краткая историческая справка. Преимущества и стадии процесса. Стадия жидкофазного окисления ИПБ в ГП ИПБ. Разновидности технологий окисления. Требования к сырью, способы его подготовки. Ингибиторы, катализаторы (инициаторы). Химические реакции (основная и побочные), протекающие при окислении ИПБ. (по лекциям Никонова надо))
Широкое распространение получил кумольный метод синтеза фенола совместно с ацетоном, основанный на окислении изопропилбензола в гидропероксид и последующем его разложении.

Краткая историческая справка:
Технология этого процесса была разработана в Советском Союзе П. Г. Сергеевым, Б. Д. Кружаловым, Р. Ю. Удрисом и М. С. Немцовым. В 1949 г. в СССР впервые в мире было осуществлено многотоннажное производство фенола и ацетона по этому методу. За рубежом первые заводы по получению фенола и ацетона из кумола были пущены в Канаде и во Франции в 1953 г., а начиная с 1954 г. построен ряд заводов в США и ФРГ.
Мировое производство фенола составляет более 3 млн. т/год. Единичные мощности установок по производству фенола кумольным методом в настоящее время составляют 100—150 тыс. т/год фенола.
«+»: дешевое сырье, получение второго основного продукта – ацетона, наиболее экономичный процесс.
Процесс складывается из окисления ИПБ в гидропероксид, концентрирования ГП, кислотного разложения ГП и ректификации продуктов разложения.
Стадия жидкофазного окисления изопропилбензола. Процесс окисления ИПБ проводится в ЖФ температурах 110-130°С в присутствии инициатора — самого ГП ИПБ.
Требования к сырью:
Болышое влияние на обрыв цепи и, следовательно, на скорость протекания могут оказывать ингибиторы. Ингибиторами являются кислые продукты, например НСООН, фенол, сернистые и ненасыщеные соединения. Следовательно сырье не должно их содержать.
Кислые продукты сами по себе не ингибируют процесс окисления, но в их присутствии ГП ИПБ разлагается на фенол и ацетон, а фенол является ингибитором окисления.
Продукты распада диметилфенилкарбинол (ДМФК) и ацето-фенон (АФ) не тормозят процесс. Имеются данные, указывающие на то, что ДМФК даже несколько ускоряет процесс. Диметилфенилкарбинол и ацетофенон являются основными побочными продуктами, снижающими селективность процесса.
Окисление в присутствии щелочи
Окисление ИПБ кислородом воздуха проводят также в воднощелочной эмульсии (1 %-ный раствор соды) при интенсивном перемешивании в присутствии ПАВ. Процесс ведут при 110-130°С и 0,49—0,98 МПа; конечное содержание ГП 25%,рН среды 8,5—10,5. Скорость накопления ГП 5-7%.
В процессе окисления по мере накопления ГП начинается частичный его распад, который становится особенно заметным при содержании ГП в реакционной массе ~ 18% и более. Поскольку распаду гидропероксида способствует повышенная температура, очень важно, чтобы в конце зоны реакции температура не превышала 110—120°С. При высоких температурах может идти распад ГП со взрывом. Количество продуктов распада колеблется от 0,5 до 5 % (в зависимости от условий окисления и конечной концентрации гидропероксида).
Для окисления ИПБ применяют реакторы следующих типов: колонного, с перемешивающим устройством, эрлифтного.
Химические реакции (основная и побочные), протекающие при окислении ИПБ
Процесс идет по радикально-цепному механизму через следующие стадии:
1) Инициирование
Можно предположить тримолекулярное инициирование

2)Продолжение цепи
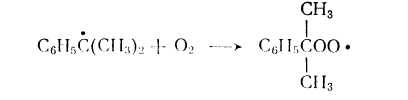
Гидропероксид(основной продукт) образуется в результате взаимодействия пероксирадикала с исходным изопропилбензолом

Пероксирадикал может параллельно распадаться с образованием ацетофенона(побочный)

Образующийся метоксирадикал взаимодействует с ИПБ
![]()
Метиловый спирт обычно окисляется дальше
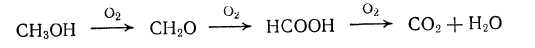
3)Вырожденное разветвление
Разветвление цепи происходит в результате термического распада гидроперекиси

Оразуется диметилфенилкарбинол —основной побочный продукт процесса.
![]()
Образовавшийся радикал может взаимодействовать с гидропероксидом
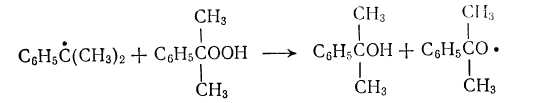
Эта реакция —один из основных маршрутов образования димефенилкарбинола.
Кроме того, возможна еще следующая реакция
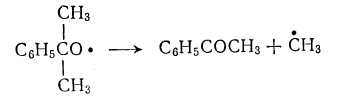
I) Обрыв цепи
67. Механизм окисления ИПБ в ГП ИПБ. Технология (в т. ч. типы реакторов и способы теплоотвода), условия и показатели стадии окисления ИПБ в ГП ИПБ. Способы разделения оксидата ИПБ. Технологическая схема стадии окисления. (см. лекции Никонова)
Процесс окисления ИПБ проводится в жидкой фазе при температурах 110-130 оС в присутствии инициатора – самого гидропероксида ИПБ.
Процесс идет по радикально – цепному механизму через следующие стадии:
