
- •I. Классические -обусловленные избыточной продукцией соляной кислоты в желудке):
- •II. Опосредованные (зависимые)- течение заболевания поддерживается повышенной продукцией кислоты в желудке):
- •III. Симптоматические расстройства желудочно-кишечного тракта:
- •1. Всасывающиеся антациды (резорбирующиеся, всасывающиеся, системные):
- •2. Невсасывающиеся антациды (несистемные, нерастворимые):
- •2.1. Монокомпонентные:
- •2.1. Комбинированные:
- •2.2. Смешанные:
- •Антацидный эффект
- •Предотвращение обратной диффузии ионов водорода
- •5.Цитопротективный эффект
- •6. Обволакивающее и/или вяжущее (для препаратов Bi) действие.
- •7. Слабое противовоспалительное действие.
- •Сравнительная характеристика действия катионов металлов, входящих в состав антацидных препаратов
- •Кислотонейтрализующая активность различных действующих веществ, входящих в состав антацидов
- •Кислотонейтрализующая активность некоторых коммерческих антацидных препаратов
- •Скорость наступления и продолжительность действия монокомпонентных антацидов
- •3. Терапия гэрб
- •4 .Антацидные препараты в терапии хронического дуоденита:
- •Блокаторы h-2 -рецепторов гистамина
- •1. Фармакокинетические
- •2. Фармакодинамические
- •Ингибиторы протонного насоса
- •Дальнейшие изменения структуры радикалов привели к созданию новых препаратов – пантопразола и рабепразола (рис.6).
- •1.Всасывание
- •2. Концентрирование в секреторных канальцах
- •4. Образование необратимой ковалентной связи с протонной помпой
- •Дозировки различных ипп
- •8.Эндокринные нарушения
- •Антибиотики для лечения нр-инфекции
- •Пилобакт am
- •Гастропротекторы
- •Классификация современных цитопротекторов в терапии заболеваний желудка
- •Механизм действия гастропротекторов
- •Схемы терапии цитопротекторами
- •Фармакокинетика
- •Показания
- •Фармакокинетика
- •Побочные действия
- •Противопоказания
- •Особые указания
- •Лекарственное взаимодействие
- •Фармакологическое действие
- •Фармакокинетика
- •Побочное действие
- •Противопоказания
- •Применение при беременности и кормлении грудью
- •Особые указания
- •Лекарственное взаимодействие
- •Стандарты Диагностика и терапия кислотозависимых заболеваний, в том числе и ассоциированных с Helicobacter pylori
- •Гастроэзофагеальная рефлюксная болезнь (гэрб)
- •Язвенная болезнь, ассоциированная с Helicobacter Pylori (нр)
- •Альтернативные варианты антихеликобактерной терапии язвенной болезни, ассоциированной с hp
- •Язвы желудка и двенадцатиперстной кишки, ассоциируемые с нестероидными противовоспалительными препаратами (нпвп)
- •Хронический панкреатит
- •Медикаментозная терапия гэрб
- •2. Антацидные препараты
- •4.Алгинаты
- •Использование антисекреторных препаратов при гэрб,
- •1.Ступенчатая терапия в двух вариантах:
- •Тактика ведения больных гэрб после стойкого устранения симптомов и эзофагита
- •Периодическая (курсовая) терапия:
- •Схемы эрадикационной терапии инфекции h. Pylori (по Маастрихтскому соглашению III, 2005)
Ингибиторы протонного насоса
Желудочный сок обладает сильнокислой реакцией -рН 0,8–1,5.
Процесс секреции соляной кислоты париетальными клетками основан на трансмембранном переносе протонов и непосредственно осуществляется специфическим ферментом - водоро́дно-ка́лиевой аденозинтрифосфата́зой(Н+/К+-АТФа́за, прото́нная по́мпа, прото́нный насо́с, прото́новый насо́с, или прото́новая по́мпа).
Секреция соляной кислоты регулируется нервной и гуморальной (эндокринной и паракринной) системами и происходит в обкладочных клетках дна и тела желудка. Основными внутриклеточными мессенджерами являются цАМФ для гистамина и ионы Са2+для гастрина и ацетилхолина, которые в конечном итоге активируют фермент Н+,K+-АТФазу. Н+,K+-АТФаза состоит из двух субъединиц белка (большой а и малой b), синтез которых происходит в эндоплазматическом ретикулуме париетальной клетки. Расчетное время полужизни Н+,K+-АТФазы составляет 15-30 ч.
При активизации молекулы Н+/К+-АТФаза транспортирует ион водорода Н+ из цитоплазмы париетальной клетки в полость желудка через апикальную мембрану в обмен на ион К+, который она переносит внутрь клетки. При этом оба катиона транспортируются против электрохимического градиента. Источником энергии для этого транспорта служит гидролиз молекулы АТФ. Одновременно с протонами водорода в просвет желудка путем активного транспорта против градиента переносятся ионы хлора Cl-. Входящие в клетку ионы К+ покидают ее по градиенту концентрации вместе с ионами Cl- через апикальную мембрану париетальных клеток. Протоны Н+ образуются в эквивалентных количествах с НСО3- при диссоциации угольной кислоты Н2СО3 при участии фермента карбоангидразы. Ионы НСО3- пассивно перемещаются в кровь по градиенту концентрации через базолатеральную мембрану в обмен на Cl-.
Реакция внутренней среды обкладочных клеток такая же, как и в других клетках,— рН 7,2, тогда как реакция в их секреторных канальцах резко кислая — рН 1,0. Содержание в желудочном соке ионов водорода и хлора составляет 150 ммоль/л, в плазме же уровень ионов водорода равен 0,00004 ммоль/л, а хлора — 105 ммоль/л. Таким образом, по обе стороны обкладочных клеток создается градиент концентрации Н+, составляющий примерно 1:1000000. Н+/К+-АТФаза создаёт значительный градиент ионов водорода, вследствие чего устанавливается значительная разница рН между цитоплазмой париетальной клетки (рН = 7,4) и просветом секреторного канальца (рН около 0,8-1). Ни одна из других клеток человеческого организма никогда не граничит со средой с такими низкими рН. (рис. 4).
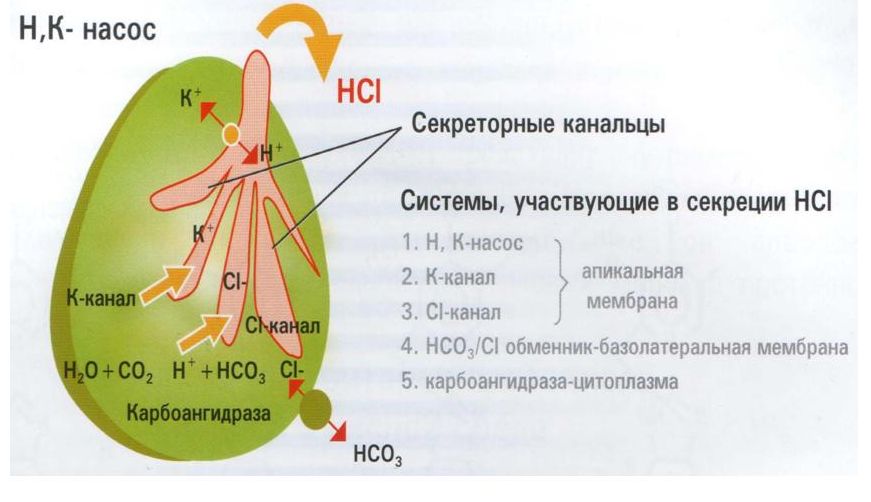
Рис.4. Механизм секреции соляной кислоты в париетальной клетке.
Таким образом в просвет желудка при с участием Н+/К+-АТФазы выделяется соляная кислота в виде ионов Н+ и Cl-, а ионы К+ возвратным образом перемещаются через мембрану.
Изучение молекулярных механизмов образования соляной кислоты желудочного сока позволило выявить его ключевое звено - активную секрецию протонов, сопряженную с транспортом К+, реализуемую специальным мембранным комплексом - протонной помпой. Это позволило разработать принципиально новый класс лекарственных средств, способных снижать активность АТФазы протонной помпы, эффективно подавляющий секрецию соляной кислоты на 100%.
Ингибиторы протонной помпы (ИПП)- химический класс антисекреторных препаратов, замещенных производных бензимидазола, образующих ковалентные связи с молекулой H+, K+-АТФазы (протонного насоса) париетальных клеток слизистой оболочки желудка, что вызывает прекращение переноса ионов водорода в просвет желудка
Химическая структура и свойства ИПП
Все ИПП представляют собой производные а-пиридилметил-сульфинилбензимидазола с различающимися заместителями в пиридиновом и бензимидазольном фрагментах.
Первый блокатор протонной помпы - тимопразол - был синтезирован в 1976 г. Однако из-за выраженных побочных эффектов, выявленных на стадии клинической апробации, препарат не был зарегистрирован.
Омепразол, синтезированный в 1978 г., первый вошел в клиническую практику и на долгое время стал «золотым» стандартом и препаратом № 1 для ингибирования протонной помпы (рис.1).
Вторым ИПП был ланзопразол (с 1992 года, Франция), третьим- пантопразол ( с 1994 года в Германии), далее в середине 90-х гг. рабепразол (Великобритания) и эзомепразол (Швеция).
Лансопразол отличается от омепразола только структурой радикалов на пиридиновом и бензимидазольном кольцах ( рис. 5).
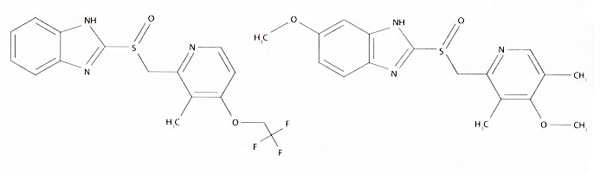
Рис. 5. Химическая структура лансопразола (слева) и омепразола (справа)
