- •Передмова.
- •1. Основні поняття та закони термодинаміКи
- •Задачі для самостійного вирішення
- •2. Термодинамічні політропні процеси з ідеальними газами
- •З урахуванням виразу :
- •Характеристики політропних процесів
- •Задачі для самостійного вирішення
- •Значення ізобарної, ізохорної теплоємностей та показника адіабати
- •3. Властивості і процеси реальних газів і парів
- •Задачі для самостійного вирішення
- •4. Цикли паросилових і холодильних установок
- •Задачі для самостійного вирішення
- •5. Основи теплообміну
- •Задача для самостійного вирішення
Характеристики політропних процесів
Групи |
Границі зміни показника політропи |
∆u |
q |
Теплоємність в процесі |
Схема енергобалансу |
|
І |
1 n |
∆u 0 |
q 0 |
сп 0
|
|
|
ІІ |
k n 1 |
∆u 0 |
q 0 |
сп 0
|
|
|
III |
+ n k |
∆u 0 |
q < 0 |
сп 0 |
|
|
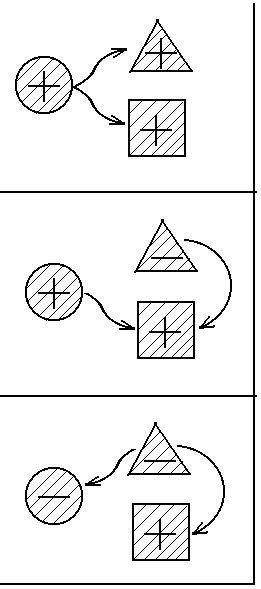
І група процесів характеризується тим, що зміна внутрішньої енергії становить частину теплоти, що підводиться в процесі, друга частина якої витрачається на виконання роботи.
ІІ
група процесів характеризується тим,
що робота здійснюється за зарахунок не
тільки теплоти, яка підводиться
![]() ,
але й зменшення внутрішньої енергії
,
але й зменшення внутрішньої енергії
![]() .
.
ІІІ
група процесів характеризується тим,
що теплота, яка відводиться
![]() ,
і робота виконується за рахунок зменшення
внутрішньої енергії
.
,
і робота виконується за рахунок зменшення
внутрішньої енергії
.
Теплоємність
в процесах ІІІ групи додатня
![]() ,
оскільки знаки теплоти і зміни температури
однакові.
,
оскільки знаки теплоти і зміни температури
однакові.
Аналогічно можна розбити на три групи всі політропні процеси стискання.
Задачі для самостійного вирішення
Задача
2.
Повітря
масою
![]() при початкових температурі
і тику
при початкових температурі
і тику
![]() стискається за політропою при
стискається за політропою при
![]() із
зменшенням об’єму в
із
зменшенням об’єму в
![]() разів. Визначити роботу і кількість
теплоти в процесі, а також зміну калоричних
параметрів. Показати для цього процесу
схему енергобалансу і графіки в
і
координатах.
Теплоємність повітря прийняти сталою.
Числові значення
і
прийняти за таблицею 2.2 відповідно до
номеру варіанту.
разів. Визначити роботу і кількість
теплоти в процесі, а також зміну калоричних
параметрів. Показати для цього процесу
схему енергобалансу і графіки в
і
координатах.
Теплоємність повітря прийняти сталою.
Числові значення
і
прийняти за таблицею 2.2 відповідно до
номеру варіанту.
Приклад
вирішення задачі при
![]() і
і
![]() .
Початкова
температутра:
.
Початкова
температутра:
![]() .
.
Газова
стала повітря:
![]() .
.
Початковий
об’єм повітря:
![]() .
.
Кінцевий
об’єм
![]() .
.
Тиск
в кінці стискання:
 .
.
Кінцева
температура:
![]() ;
;
![]() .
.
Робота, яка витрачається в процесі:
![]() .
.
Теплоємність повітря в політропному процесі:
![]() .
.
Тут
![]() – мольна теплоємність двохатомного
газу при постійному об’ємі (табл. 2.3).
– мольна теплоємність двохатомного
газу при постійному об’ємі (табл. 2.3).
Кількість теплоти, що витрачається в процесі:
![]() .
.
Зміна внутрішньої енергії повітря:
![]() .
.
Зміна ентальпії повітря:
![]()
Зміна
ентропії:
![]() .
.
Таким чином, в розглянутому політропному процесі робота, яка витрачається, йде на зростання внутрішньої енергії і на теплоту, яка відводитсья. Графік політропного процесу з і схема енергобалансу показані на рис.2.6.
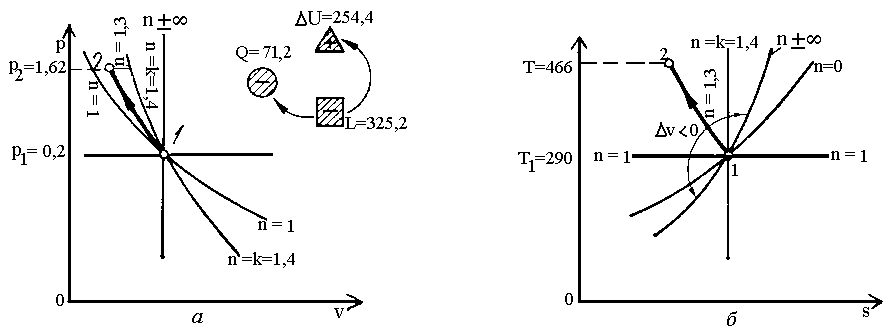
Рис.2.6. Графіки політропного процесу .
Таблиця 2.2.
Вихідні дані задач для самостійного вирішення
№ вар. |
|
|
№ вар. |
|
|
1 |
16 |
0,1 |
16 |
32 |
1,7 |
2 |
18 |
0,3 |
17 |
33 |
1,8 |
3 |
19 |
0,4 |
18 |
34 |
1,9 |
4 |
20 |
0,5 |
19 |
35 |
2,0 |
5 |
21 |
0,6 |
20 |
35 |
2,1 |
6 |
22 |
0,7 |
21 |
37 |
2,2 |
7 |
23 |
0,8 |
22 |
38 |
2,3 |
8 |
24 |
0,9 |
23 |
39 |
2,4 |
9 |
25 |
1,0 |
24 |
40 |
2,5 |
10 |
26 |
1,1 |
25 |
41 |
2,6 |
11 |
27 |
1,2 |
26 |
42 |
2,7 |
12 |
28 |
1,3 |
27 |
43 |
2,8 |
13 |
29 |
1,4 |
28 |
44 |
2,9 |
14 |
30 |
1,5 |
29 |
45 |
3,0 |
15 |
31 |
1,6 |
30 |
46 |
3,1 |
Таблиця 2.3.