- •Рациональный состав медного концентрата
- •Расчет количества и состава штейна и отвального шлака и расход флюсов
- •Состав и количество отвального шлака
- •Состав и количество отходящих газов на воздушном дутье с учетом подсосов
- •Расчет состава и количество газа для обогащенного дутья 68% кислорода
- •Состав и количество топочных газов
- •Состав отходящих газов с учётом подсосов и сгорания природного газа (т.Е. С учётом топочных газов)
МИНИСТЕРСТВО ОБЩЕГО И ПРОФЕССИОНАЛЬНО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
Национальный исследовательский технологический университет «МИСиС»
Кафедра ЦМиЗ
Домашнее задание по курсу:
«Металлургия меди и никеля»
Вариант 14
Студент: Черепов В.В.
Группа: МРМ-09-1
Преподаватель: Хабиев Р. П.
2012 год
1. Рассчитать рациональный состав медного концентрата следующего состава:
: Cu – 22%, Fe – 36%, Ni - 2%, S – 33,6%, SiO2 – 0,6%, Al2O3 – 1,2%, CaO – 0,3%, MgО – 0,3.
В концентрате присутствуют следующие минералы: халькопирит (CuFeS2), пирротин(Fe7S8), пентлантид (NiFeS2), известняк (CaCO3), магнезит (MgCO3). Вся медь присутствует в форе халькопирита.
Состав медного концентрата:
Cu |
Fe |
Ni |
S |
SiO2 |
Al2O3 |
CaO |
MgО |
Прочее |
22 |
36 |
2 |
33,6 |
0,6 |
1,2 |
0,3 |
0,3 |
4 |
2. Рассчитать количество и состав штейна и отвального шлака (на 100 кг сухой массы концентрата) и расход флюсов при плавке по способу окислительного восстановления (ПВ) при следующих условиях :
Извлечение Cu в штейн – 98,5%, Ni – 97,5%.
Содержание в штейне меди - 60%
Содержание в шлаке SiO2 -35%, CaO-6%, отношение FeO/Fe3O4 – 6:1
Химический состав кварцевого флюса: SiO2 – 95%, CaO – 1%;
Химический состав известняка: CaO – 49%, SiO2 – 0.5%, Al2O3 – 1,5%, MgO – 2%
3. Рассчитать количество и состав технологических и отходящих газов на обогащенном до 68 % (объемн.) O2 в дутье при плавке концентрата в полуавтогенном режиме из условий:
- 5% серы в газах окисляется до SO3 , а 95% до SO2 ;
- коэффициент использования кислорода в расплаве – 94%;
- содержание кислорода в техническом кислороде – 95,5%;
- влажность концентрата -6,5%, флюсов – 9,5%;
- расход природного газа на 100 кг сухой шихты 2,8 кг
- состав природного газа (% объёмн.) CH4 - 90%, C2H6 – 6%, N2 – 4%
-подсосы воздуха в печь составляют 45% от объема дутья;
4.Составить материальный баланс процесса плавки. Рассчитать степень десульфуризации при плавке.
Расчёт рационального состава медного концентрата
Найдем количество CuFeS2 и количество каждого компонента в нём:
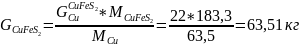

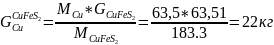

Найдем количество Fe в Fe7S8 :
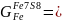 36 - 19,33 = 16,67
36 - 19,33 = 16,67
Найдем количество NiFeS2 и содержание S в нём:
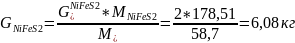
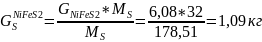
Найдём количество S в Fe7S8
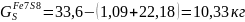
Найдем количество CaCO3 и содержание в нём CO2:
CaCO3 –> CaO + CO2


Найдем количество MgCO3 и содержание в нём CO2:


Найдем количество прочего в концентрате:

Рациональный состав медного концентрата
|
Cu |
Ni |
Fe |
S |
SiO2 |
Al2O3 |
CaO |
MgО |
CO2 |
Прочее |
Всего |
CuFeS2 |
22 |
|
19,33 |
22,18 |
|
|
|
|
|
|
63,51 |
Fe7S8 |
|
|
16,67 |
10,33 |
|
|
|
|
|
|
27 |
NiFeS2 |
|
2 |
|
1,09 |
|
|
|
|
|
|
3,09 |
CaCO3 |
|
|
|
|
|
|
0,3 |
|
0,24 |
|
0,54 |
MgCO3 |
|
|
|
|
|
|
|
0,3 |
|
|
0,63 |
SiO2 |
|
|
|
|
0,6 |
|
|
|
|
|
0,6 |
Al2O3 |
|
|
|
|
|
1,2 |
|
|
|
|
1,2 |
Прочее |
|
|
|
|
|
|
|
|
|
3,43 |
3,43 |
Всего |
22 |
2 |
36 |
33,6 |
0,6 |
1,2 |
0,3 |
0,3 |
0,57 |
3,43 |
100 |
Расчет количества и состава штейна и отвального шлака и расход флюсов
Расчет состава и количества штейна
Количество Cu в штейне:

Количество штейна:
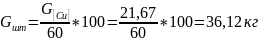
Количество Ni в штейне:

Содержание серы в штейне |
25% по правилу Мостовича: |
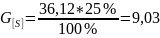 кг
кг
Содержание кислорода в штейне:


Содержание прочих в штейне
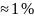

Количество Fe в штейне:
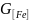 =
=
Количество и состав штейна
Компонент |
Масса ,кг |
Содержание,% |
Cu |
|
60,00 |
Fe |
|
7 |
Ni |
|
5,4 |
S |
|
25 |
O |
|
1,6 |
Пр |
|
1,00 |
Всего |
|
100 |
Расчет состава и количества самоплавкого шлака
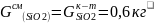

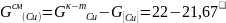
 0,33
0,33

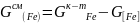
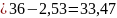
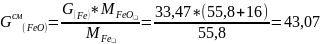
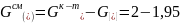

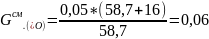
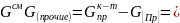 4 – 0,36 = 3,64
4 – 0,36 = 3,64
Количество и состав самоплавкого шлака
Оксиды |
Масса,кг |
Содержание,% |
FeO |
43,07 |
86,94 |
MgO |
0,3 |
0,61 |
Cu2O |
0,37 |
0,75 |
NiO |
0,06 |
0,12 |
Al2O3 |
1,2 |
2,42 |
SiO2 |
0,6 |
1,21 |
CaO |
0,3 |
0,61 |
Пр |
3,64 |
7,35 |
Всего |
49,54 |
100 |
Расчет флюсов
Кварцевый флюс – x кг
Известковый флюс – y кг
Составляем два балансовых уравнения и решаем их как систему
SiO2:
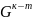 SiO2+0.95x+0.05y=0.35(Gсм.шл.+0,99x+0,62y)
SiO2+0.95x+0.05y=0.35(Gсм.шл.+0,99x+0,62y)
CaO: СаО+0.49y+0.01х=0.06(Gсм.шл.+ 0,99x+0,62y)
Получаем:
x=30,22 кг – кварцевый флюс
y=7,52 кг – известковый флюс
Составим пропорцию :
Кварцевый
флюс
CaCO3=»
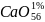 +
+

X1=0,79% CO2; Прочее 3,21%
Известковый
флюс: CaCO3=»
 +
+
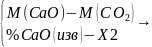
X2=38,5% CO2; Прочее 8,5%
Gфл=30,22 +7,52 =37,74 кг
Gотв.шлSiO2
=
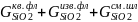 =30,22*0,95+7,52*0,005+0,6
= 29,35 кг
=30,22*0,95+7,52*0,005+0,6
= 29,35 кг
Gотв.шлCaO
=
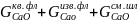 =30,22*0,01+7,52*0,49+0,3=
4,28 кг
=30,22*0,01+7,52*0,49+0,3=
4,28 кг
Gотв.шлMgO
=
 кг
кг
Gотв.шлAl2O3
=
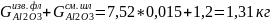
G
Пр =
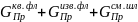 =
30,22*0,0321+7,52*0,085+3,64 = 5,25 кг
=
30,22*0,0321+7,52*0,085+3,64 = 5,25 кг