
- •Агрегатные состояния (лекция №1)
- •Газовые законы
- •Хроматография
- •Использование плазмы в медицине
- •Плазма используется в технике.
- •Термодинамика растворения
- •Структура воды
- •Роль воды в организме
- •Баланс воды в организме
- •Распределение воды в организме
- •Твердые тела
- •Кристаллические тела
- •Ионные решетки
- •Атомные решетки
- •Полиморфизм
- •Аллотропные модификации углерода
- •Металлическая решетка
- •Жидкие кристаллы
- •Фазовые переходы (Лекция №3)
- •Уравнение Клайперона – Клаузиса
- •Уравнение Трутона
- •Кипение
- •Плавление
- •Перекристаллизация из раствора
- •Экстракция
- •Ферменты. (Лекция №4)
- •Ферменты – это белковые катализаторы.
- •Участок фермента, непосредственно взаимодействующий с субстратами называется активным центром фермента.
- •Свойства активного центра
- •Основные свойства ферментов.
- •Зависимость скорости ферментативной реакции от концентрации субстрата
- •Способы регуляции активности ферментов.
- •Конкурентное ингибирование.
Использование плазмы в медицине
Плазменные разряды используются для получения озона, применяемого для обеззараживания воды.
Генерирующие плазму приборы также используют для дезинфекции хирургических инструментов для удаления фрагментов тканей и коагуляции крови. Поскольку плазма действует на атомном уровне и способна достигнуть любой точки поверхности, даже полость иглы. Дезинфицирующие свойства связаны с генерированием биологически активных бактерицидных агентов, таких как свободные радикалы.
Разработали устройство, позволяющее с помощью ионизированной плазмы в течение нескольких секунд безопасно дезинфицировать кожу человека, уничтожая все устойчивые к антибактериальным препаратам микроорганизмы. Новое плазменное устройство сокращает в 10 раз время обработки рук хирургам. С помощью плазмы можно лечить также незаживающие раны.
Обработанная плазмой вода долго хранится. Вода после обработки плазмой сохраняла свои антибактериальные свойства даже спустя неделю, когда содержание в ней пероксида водорода, а также нитратов и нитритов снижалось до нуля. Это указывает на существование других активных соединений, формируемые под действием разрядов плазмы и сохраняющихся в воде в течение продолжительного времени.
Плазма используется в технике.
Плазменная панель (телевизор, монитор)
Вещество внутри люминесцентных (в том числе компактных) и неоновых ламп
Плазменные ракетные двигатели
Исследования управляемого термоядерного синтеза
Электрическая дуга в дуговой лампе и в дуговой сварке
Управляемый термоядерный синтез — синтез более тяжёлых атомных ядер из более лёгких с целью получения энергии, который, в отличие от взрывного термоядерного синтеза (используемого в термоядерных взрывных устройствах), носит управляемый характер. Наиболее простая реакция – это получение дейтерия из атомов водорода. Н + Н = Д.
Жидкость (Лекция №2)
Жидкость — одно из агрегатных состояний вещества. Основным свойством жидкости, является способность неограниченно менять форму, практически сохраняя при этом объём. Поверхность жидких тел ведёт себя как упругая мембрана. Так, вода может собираться в капли. Жидкость способна течь. Однако жидкость не обладает полной свободой перемещений. Между молекулами существует притяжение, достаточно сильное, чтобы удержать их на близком расстоянии.
Как правило, вещество в жидком состоянии имеет только одну модификацию.
Текучесть. Основным свойством жидкостей является текучесть. Если к участку жидкости, находящейся в равновесии, приложить внешнюю силу, то возникает поток частиц жидкости. В отличие от пластичных твёрдых тел, жидкость не имеет предела текучести: достаточно приложить сколь угодно малую внешнюю силу, чтобы жидкость потекла.
Сохранение объёма. Давление, производимое на жидкость, заключенную в сосуд, передаётся без изменения в каждую точку объёма этой жидкости (закон Паскаля).
Жидкости обычно увеличивают объём при нагревании и уменьшают объём при охлаждении. Впрочем, встречаются и исключения, например, вода сжимается при нагревании, при нормальном давлении и температуре от 0 °C до приблизительно 4 °C.
Вязкость. Кроме того, жидкости характеризуются вязкостью. Она определяется, как способность оказывать сопротивление перемещению одной из части относительно другой — то есть как внутреннее трение. Вязкость тем больше, чем меньше текучесть. Вязкость можно измерять с помощью вискозиметра. Ниже приведена таблица вязкостей
Вещество Вязкость кг/(м*с)
Эфир этиловый 0,238
Ацетон 0,337
Бензол 0,673
Вода 1,05
Масло оливковое 90
Глицерин 1400
Масло машинное легкое 113
Смачивание — поверхностное явление, возникающее при контакте жидкости с твёрдой поверхностью в присутствии пара, то есть на границах раздела трёх фаз. Смачивание характеризует «прилипание» жидкости к поверхности и растекание по ней). Различают три случая: несмачивание, ограниченное смачивание и полное смачивание.
Смешиваемость — способность жидкостей растворяться друг в друге. Пример смешиваемых жидкостей: вода и этиловый спирт, пример несмешиваемых: вода и жидкое масло. Если при взаимодействии молекул разных жидкостей образуются водородные, электростатические связи, то жидкости смешиваются (полярные с полярными, неполярные с неполярными).
Диффузия. При нахождении в сосуде двух смешиваемых жидкостей молекулы в результате теплового движения начинают постепенно проходить через поверхность раздела, и таким образом жидкости постепенно смешиваются. Это явление называется диффузией.
Порядок Молекулы жидкости не имеют определённого положения, но в то же время им недоступна полная свобода перемещений. Между ними существует притяжение, достаточно сильное, чтобы удержать их на близком расстоянии.
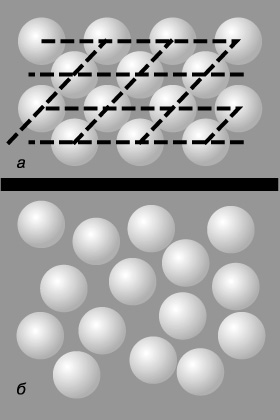
Ближний порядок.
Упорядоченность
в твердом теле (а) и в жидкости(б). Молекула
жидкости колеблется около положения
временного равновесия, сталкиваясь с
другими молекулами из ближайшего
окружения. Время от времени ей удается
совершить «прыжок», чтобы покинуть
своих соседей из ближайшего окружения
и продолжать совершать колебания уже
среди других соседей. Время оседлой
жизни молекулы воды, т. е. время
колебания Около одного положения
равновесия при комнатной температуре,
равно в среднем
10-11
сек.
Траектории движения молекул:
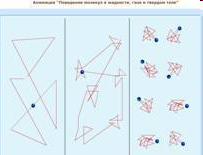
Газ Жидкость Твердое тело
В жидкости могут быть растворены газы, жидкости и твердые вещества.
Растворимость газов в жидкостях меняется в широких пределах и зависит от природы газа (в первую очередь от его полярности), природы растворителя, температуры и давления.
В таблице 3 приведена растворимость газа ( в литрах ) в 1 литре воды.
Растворимость газов в воде.
Газы V газа /V воды

Кислород 0,032
СО2 0,93
Аммиак 750,0

