
- •Агрегатные состояния (лекция №1)
- •Газовые законы
- •Хроматография
- •Использование плазмы в медицине
- •Плазма используется в технике.
- •Термодинамика растворения
- •Структура воды
- •Роль воды в организме
- •Баланс воды в организме
- •Распределение воды в организме
- •Твердые тела
- •Кристаллические тела
- •Ионные решетки
- •Атомные решетки
- •Полиморфизм
- •Аллотропные модификации углерода
- •Металлическая решетка
- •Жидкие кристаллы
- •Фазовые переходы (Лекция №3)
- •Уравнение Клайперона – Клаузиса
- •Уравнение Трутона
- •Кипение
- •Плавление
- •Перекристаллизация из раствора
- •Экстракция
- •Ферменты. (Лекция №4)
- •Ферменты – это белковые катализаторы.
- •Участок фермента, непосредственно взаимодействующий с субстратами называется активным центром фермента.
- •Свойства активного центра
- •Основные свойства ферментов.
- •Зависимость скорости ферментативной реакции от концентрации субстрата
- •Способы регуляции активности ферментов.
- •Конкурентное ингибирование.
Хроматография
Различают газо-твёрдофазную и газо-жидкостную хроматографию. В первом случае неподвижной фазой является твёрдый носитель (силикагель, уголь, оксид алюминия). Вещества разделяются по способности адсорбироваться на твердом носителе. Чем меньше способность к адсорбции, тем раньше вещество попадает в детектор.
Во втором случае неподвижной фазой является жидкость, нанесённая на поверхность инертного носителя. Вещества разделяются по растворимости в жидкой фазе.
Схема хроматографа

1 — источник газа-носителя (подвижной фазы) Обычно используется аргон, гелий, азот, водород, воздух. 2 — регулятор расхода газа носителя 3 — устройство ввода пробы (испаритель). 4 — хроматографическая колонка в термостате 5 — детектор 6 — электронный усилитель 7 — регистрирующий прибор (самописец, компьютер) 8 — расходомер
Неподвижная жидкая фаза должна быть термически стабильной, химически устойчивой, иметь небольшую вязкость.
Вещества, лучше растворимые в стационарной фазе, дольше удерживаются ею. Благодаря этому происходит разделение анализируемой смеси на отдельные компоненты, которые выходят из колонки отдельно и регистрируются на выходе.
Плазма
Плазма царит во Вселенной. Звезды, наше Солнце, огонь — все это вещество в состоянии плазмы. В мире на плазму приходится 99,9% всего вещества. От газа плазма отличается тем, что часть ее атомов и молекул ионизирована. Хотя общий заряд плазмы равен нулю, в ее состав наряду с нейтральными частицами входят и электрически заряженные — ионы и электроны. Присутствие свободных электрических зарядов делает плазму проводящей средой. Это обуславливает её заметно большее взаимодействие с магнитным и электрическим полями.
Плазма в магнитном поле, упорядоченно движется в плоскостях, перпендикулярных его силовым линиям. Последнее свойство позволило исследователям «укрощать» плазму. Два десятилетия физики стремятся осуществить в плазме звездную реакцию превращения водорода в гелий — управляемый термоядерный синтез.
Для получения
плазмы обычно используют плазматроны.
Большое распространение получили
плазмотроны электродуговые. В них
поступающий в рабочую камеру газ —
аргон, гелий, азот или водород —
превращается в плазму с помощью дугового
разряда, горящего между двумя электродами).
Один из этих электродов обычно выполняется
из тугоплавкого
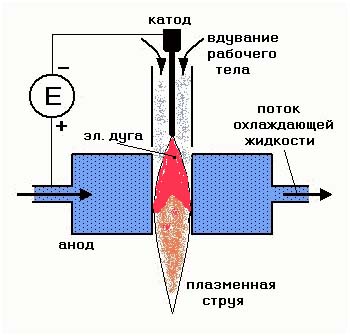 металла —
вольфрама, молибдена или специальных
сплавов, а второй, представляющий собой
узкое сопло с циркулирующей под рубашкой
охлаждающей водой.
металла —
вольфрама, молибдена или специальных
сплавов, а второй, представляющий собой
узкое сопло с циркулирующей под рубашкой
охлаждающей водой.
Низкотемпературной наз. плазму, у которой средняя энергия электронов меньше характерного потенциала ионизации атома ( Температура её обычно не превышает 105 К. Плазма с более высокой температурой называется. горячей или высокотемпературной плазмой. Обычно низкотемпературная плазма слабо ионизована, т. е. число нейтральных атомов и молекул значительно превышает число заряженных частиц - электронов и ионов. Отношение числа ионизированных атомов к полному их числу в единице объёма называется. степенью ионизации плазмы.
