
- •Глава 1. Товароведение как наука о потребительной стоимости товаров
- •1.1. Предмет и содержание товароведения
- •Связь товароведения с другими науками и научными дисциплинами
- •1.2. Товароведение как наука о потребительной стоимости
- •Структура потребительной стоимости
- •Качество и потребительские свойства
- •Структура потребительских свойств предметов потребления, их значимость
- •Глава 2. Систематизация, кодирование и информация о товаре
- •2.1. Значение и виды классификации товаров
- •2.2. Маркировка
- •1 См.: гост 9980.4-2002 Материалы лакокрасочные. Маркировка.
- •1 См.: гост 141.92 Транспортная маркировка.
- •2.3. Штриховое кодирование товаров
- •Флаг кода, присвоенный странам мира Международной ассоциацией ean
- •2.4. Кодирование ювелирных изделий пробированием й клеймением
- •2.5. Кодирование бытовой электротехнической продукции по классам — уровням а, б, с, д, е, f, g
- •2.6. Манипуляционные и предупредительные знаки и условные обозначения
- •Глава 3. Потребительские и основные свойства товаров
- •3.1. Потребительские свойства товаров
- •3.2. Основные свойства материалов и изделий
- •Износостойкость материалов и изделий
- •Глава 4. Факторы, обеспечивающие качество товаров
- •4.1. Строение материалов
- •Аморфная структура материалов
- •Стекло его состав и строение
- •Ориентировочные составы существующих стекол (в %)
- •Аморфно-кристаллическая структура материалов
- •Формирование структуры керамики методом прессования
- •Минеральный состав клинкера
- •4.2. Материалы на основе суспензий
- •4.3. Композиционные материалы
- •4.4. Некоторые особенности микро-и макроструктуры строительных материалов
- •Глава 5. Качество и контроль качества товаров
- •5.1. Показатели надежности продукции
- •Показатели надежности, записываемые в стандарты и технические условия
- •Восстанавливаемые детали машин и механизмов
- •Восстанавливаемые радиотехнические устройства, бытовые машины, аппараты и приборы
- •Восстанавливаемые узлы и агрегаты машин и механизмов
- •5.2. Показатели качества товаров
- •Неравномерность товара (материала) по различным признакам
- •5.3. Методы определения качества
- •Отборы проб
- •Приборы и стендовые испытания
- •Результаты испытаний
- •5.4. Контроль качества продукции
- •Организация производственного технического контроля
- •5.5. Физико-химические методы оценки состава, структуры материалов и изделий
- •Масс-спектральный анализ
- •Глава 6. Оценка качества товаров
- •Основные методы оценки уровня качества
- •Глава 7. Формирование и оценка ассортимента товаров
- •7.1. Структурная характеристика ассортимента товаров
- •7.2. Формирование ассортимента товаров
- •Глава 8. Факторы, сохраняющие качество товаров
- •8.1. Классификация и требования к упаковке
- •1 См.: Общероссийский классификатор видов грузов, упаковки и упаковочных материалов, ок 031-2002.
- •8.2. Условия и принципы хранения
- •8.3. Приемка товаров
- •8.4. Транспортировка
- •Глава 9. Конкурентоведение1 и конкурентоспособность товаров
- •1 См.: Магомедов ш.Ш. Конкурентоспособность товаров: Учебное пособие для вузов. — м.: итк "Дашков и к°", 2003.
- •9.1. Предмет и метод конкурентоведения товаров
- •Метод конкурентоведения товаров
- •1 См.: Магомедов ш.Ш. Конкурентоспособность товаров: Учебное пособие для вузов. — м.: итк "'Дашков и к°", 2003.
- •Связь конкурентоведения товаров с другими науками и дисциплинами
- •9.2. Конкурентоспособность и методы управления качеством
- •Функционально-стоимостной анализ
- •Распределение служебных функций изделия «а» по принципу abc
- •Сопоставление коэффициентов значимости функций и их стоимости
- •Глава 10. Управление качеством на стадиях жизненного цикла товаров
- •10.1. Маркетинговая деятельность в управлении качеством
- •10.2. Характеристика о производственной стадии
- •10.3. Управление качеством через оптимизацию уровня качества продукции
- •10.4. Управление качеством на стадии эксплуатации (потребления)
- •Глава 11. Экспертиза товаров
- •11.1. Понятие, цели, задачи и виды экспертизы
- •11.2. Экспертиза непродовольственных товаров Особенности экспертизы полимерных материалов
- •Особенности экспертизы нефтепродуктов и их характеристика
- •Технические требования к физико-химическим свойствам нефти, поставляемой для экспорта
- •Характеристика нефтяных растворителей по составу
- •Характеристики автобензина
- •Определение волокнистого состава бумаги
- •Особенности горения текстильных волокон
- •Особенности горения смешанной пряжи
4.1. Строение материалов
Данные о внешнем и внутреннем строении широко используются в товароведении при изучении и оценке свойств сырья, материалов и готовых изделий, при установлении происходящих изменений в материале при выработке, хранении товаров и их использовании в различных условиях.
Ввиду сложности строения вещества исследование строения однородного материала по степени глубины можно подразделить на несколько ступеней: исследование строения атомов вещества, строения молекулы вещества, расположения и связей молекул в веществе ("внутренней структуры"), исследования микроструктуры и макроструктуры вещества.
Строение атомов изучается в специальных научных целях и непосредственно в товароведной практике не применяется. Однако использование радиоактивных атомов, так называемых "меченых атомов", находит применение в товароведных исследованиях.
При изучении строения молекул веществ наряду с химическим составом выясняется наличие тех или иных групп ато
мов, нередко оказывающих решающее влияние на свойств! вещества (цвет, растворимость вещества и т. д.). 2
Порядок и характер химических связей отдельных ато; мов в молекуле, наличие двойных и тройных связей в моле^ куле, как известно, сильно влияют на устойчивость веще-i ства к различным воздействиям (окисление, действие света! различных химических реагентов и др.).
Расположение и связи молекул в веществе обычно назьй вают "внутренней структурой вещества".
При изучении химической природы материалов данные 4 внутренней структуре вещества обусловливают более глубо-кие представления о различных свойствах материалов и Щ отношении к физико-химическим воздействиям.
Особенности микро- и макроструктуры применяемых ма| териалов являются предметом непосредственных товаровед! ных исследований. Эти данные широко используются при характеристике материалов.
Кристаллические и аморфные вещества
Твердое тело — агрегатное состояние вещества, отличающееся стабильностью формы и характером теплового дви| жения атомов, которые совершают малые колебания вокру: положений равновесия. Различают кристаллические и аморф] ные твердые тела. В первых существует пространственна^ периодичность в расположении равновесных положений атси мов. В аморфных твердых телах атомы колеблются окол« хаотически расположенных точек. Устойчивым состояние^ твердых тел является кристаллическое. Различают твердый тела с ионной, ковалентной, металлической и др. типами связз; между атомами, что обусловливает разнообразие их физи-j ческих свойств. Электрические и некоторые другие свойства твердых тел в основном определяются характером движений внешних электронов его атомов. По электрическим свойствази твердые тела делятся на диэлектрики, полупроводники ц металлы, по магнитным— на диамагнетики, парамагнетик^ и тела с упорядоченной магнитной структурой. Исследования
свойств твердых тел объединились в большую область — физику твердого тела, развитие которой стимулируется потребностями техники.
Как сказано выше, твердые вещества подразделяются на кристаллические и аморфные, причем часто кристаллическая и аморфная структуры являются лишь различными состояниями одного и того же вещества, и при определенных условиях возможен переход из аморфного состояния в крис-, таллическое, всегда термодинамически более устойчивое. Так, например, соединение SiOa существует в виде кристаллического кварца и нескольких аморфных форм кремнезема.
Кристаллическая форма одного и того же вещества может иногда существовать в различных модификациях (например, алмаз и графит).
В металлографии римскими цифрами и греческими буквами обозначают различные модификации одного и того же кристаллического вещества. Так, форма, устойчивая при комнатной температуре, называется а-модификацией. Модификации, в которую переходит Р-модификация при повышении температуры, соответственно обозначаются буквами греческого алфавита (а, Р, у и т. д.), а при понижении температуры — римскими цифрами (I, II, III и т. д.).
Характерные признаки кристаллического состояния вещества — явление анизотропии, определенная и резко выраженная температура плавления и определенная геометрическая форма кристалла.
Анизотропное строение обусловливает различное проявление некоторых свойств кристалла в зависимости от направления измерения этих свойств. К таким свойствам, в частности, относятся: прочность, тепло- и электропроводность, коэффициенты преломления света, теплового расширения и др.
Анизотропия является наиболее общим признаком, характерным для всех кристаллических структур, тогда как другие признаки не всегда могут быть применимы для характеристики структуры твердого вещества. Так, некоторые кристаллические вещества не могут быть переведены непосредственно в жидкое состояние или не плавятся без разложения.
Хотя каждой данной кристаллической модификации веще-* ства свойственна определенная геометрическая форма кристаллов, однако она может подвергнуться изменениям а процессе образования кристаллов при наличии факторов; препятствующих их нормальному росту. <
Так как внешняя форма правильных кристаллов являете ~ отражением расположения составляющих их частиц, тс* классификация кристаллов по внешней форме обычно со| впадает с классификацией кристаллических решеток. Вс кристаллы по признакам геометрического строения (угль между ребрами и размеры ребер) делятся на семь систем: кубическую, тетрагональную, ромбическую, гексагональную^ ромбоэдрическую, моноклинную и триклинную.
Одним из характерных признаков кристаллов является и~ симметрия, которая проявляется во всех свойствах и в и" форме.
По признакам геометрической симметрии кристаллы разделяются на 32 макросимметрических класса и 230 макро-f симметрических групп.
Большое влияние на свойства кристаллического веществ"' оказывает характер связи отдельных частичек (атомов, моле| кул, ионов), составляющих кристаллы. 1
Если в кристалле все частички связаны ковалентной свя зью, то благодаря прочности этой связи, ее направленност (т. е. ориентировке связи в строго определенном направлении! и насыщенности вещество обладает высокой твердостью, высокой температурой плавления и малой летучестью (например, алмаз, карборунд).
Связь, образующаяся между разноименно заряженным, ионами, называется ионной. Такая связь характеризуется зна4 чительной прочностью, вещества с ионной решеткой облада- ют сравнительно высокими температурами плавления и ма,; лой летучестью (например, NaCl, KF и др.). f
Кристалл, образованный одноименно заряженными ионами, характеризуется металлической связью, типичной дл;г металлов. Эта связь большей частью очень прочна, что
обусловливает твердость металлов, их высокую температуру плавления и низкую летучесть.
Наличие при этой связи слабо связанных (подвижных) электронов обеспечивает металлам высокую электропроводность и теплопроводность. Ненаправленность металлической связи придает металлам присущую им пластичность (например, ковкость).
При межмолекулярной связи (обусловленной силами Ван-дер-Ваальса) в кристаллах связаны друг с другом молекулы вещества. Эта связь менее прочная, поэтому эти вещества обладают сравнительно низкими температурами плавления и большой летучестью (нафталин, бензол и др.).
Необходимо отметить, что, кроме перечисленных выше четырех основных типов связи, в кристаллах существуют и промежуточные формы связи, например полярная — средняя между ковалентной и ионной, а также и другие связи: водородная и ионодипольная. Кроме того, во многих кристаллах возможно наблюдать несколько типов связи. Так, например, в кристалле кальцита (СаСОз) кальций связан с ионами СОз — ионной связью, а сложный ион С0з внутри имеет ковалентные связи.
Сплавы металлов, как правило, состоят из кристалликов отдельных металлов, составляющих данный сплав. Однако бывают случаи, когда в кристалликах одного металла присутствуют атомы другого металла. Это возможно в случае образования химического соединения металлов, или, как его называют, интерметаллического соединения, а также в том случае, когда атомы одного металла располагаются в кристаллической решетке другого металла, образуя твердые растйбры. Эти факторы сложности связей и состава кристаллов необходимо учитывать при изучении свойств кристаллических веществ.
Структура и свойства металлов
Первое наиболее точное определение металлов дано великим русским ученым М.В. Ломоносовым. Он указывал, что
"металлы суть светлые тела, которые ковать можно". В этом определении М.В. Ломоносов подчеркнул два характерных свойства металлов: металлический блеск и пластичность. Впоследствии учеными были подмечены еще два характерных свойства металлов: их электро- и теплопроводность. Одним из главнейших свойств металлов является их способность; легко отдавать валентные электроны, находящиеся На на.4 ружной оболочке атомов. Эти электроны являются валентными и непрочно связаны с ядром. Атомы металла после отдачи валентных электронов переходят в положительно заряженные ионы. Способность металлов отдавать свои электроны во многом определяет их физические свойства.
Способность'к отдаче электронов проявляется у отдельных металлов неодинаково. Чем легче металл отдает свои электроны, тем он химически активнее.
Металлы являются кристаллическими телами. В узлах кристаллической решетки материала находятся ион-атомы, т.е. атомы металла, валентные электроны которого принадлежат не только данному атому, но благодаря свободному их перемещению также и другим ион-атомам металла.
Вследствие этого атомы соединены между собой так называемой металлической связью, характеризующейся наличием каркаса из положительно заряженных ионов и блуждающих между ними свободных электронов. Ион-атомы колеблются около своего среднего положения.
Наличие свободно перемещающихся в металле электронов определяет все типичные свойства металлов, их высокую электропроводность, а также высокую пластичность. Современная теория металлической связи дает возможность связать важнейшие свойства металлов с их атомно-кристал-лическим состоянием.
Кристаллические решетки металлов
Как уже отмечалось, металлы имеют кристаллическое состояние. Совокупность атомов металлов в твердом состоянии образует кристаллическую пространственную решетку.
Атомы в кристаллических телах расположены в пространстве в определенном порядке, закономерно и периодично.
Многие металлы, например альфа-железо, хром, тантал, молибден, ванадий и др., имеют кристаллическую решетку объемно-центрированного куба. Восемь атомов находятся в углах куба и один — в центре (всего девять атомов).
Еще большее число металлов обладает решеткой куба с центрированными гранями: восемь атомов расположены в углах куба и по одному атому — в центре каждой грани (всего 14 атомов). Гамма-железо, алюминий, медь, никель, свинец, серебро, золото, платина обладают решеткой гранецентри-рованного куба.
У некоторых металлов имеется гексагональная (в виде шестигранной призмы) решетка. Гексагональную плотно сложенную решетку имеют цинк, магний и бериллий. Углерод в виде графита также имеет гексагональную решетку.
Кристаллической решеткой металлы обладают в твердом состоянии; при расплавлении металла решетка разрушается, а при затвердевании снова образуется.
Размеры кристаллической решетки характеризуются ее параметрами.
В настоящее время различают структуру металлов внутреннюю (междуатомную) и кристаллическую (микро- и макроструктуру).
Междуатомная структура (внутренняя) обнаруживается рентгенографическими методами. Кристаллическая микроструктура исследуется при помощи металломикроскопа. При небольших увеличениях или при рассмотрении невооруженным глазом наблюдается макроструктура металлов.
Аллотропия металлов
Для ряда металлов характерна аллотропия. Аллотропией называется способность металла приобретать при различных температурах различные кристаллические решетки. Аллотропические превращения обычно сопровождаются выделением и поглощением тепла. Различные аллотропические пре
вращения обычно сопровождаются выделением или поглощением тепла. Различные кристаллические решетки. Аллот-s ропические превращения обычно сопровождаются выделе-? нием или поглощением тепла.
Анизотропия кристаллов
Анизотропией называется различие свойств кристаллов в разных направлениях. Она обусловлена неодинаковой плотностью атомов в решетке.
Прочность монокристалла меди в различных направление ях, колеблется от 14 до 35 кгс/мм2, а относительное удлинение — от 10 до 55%. В противоположность этому аморфные; тела изотропны: их свойства одинаковы в различных направ-: лениях.
При обычных условиях охлаждения образующиеся из расплава металлы и сплавы состоят из большого количества кри-^ сталлов, различным образом ориентированных. Такое строев ние металла называется поликристаллическим. Кристаллы на. своей поверхности обычно не успевают приобрести свойственную каждому металлу законченную кристаллическую структуру. Это происходит вследствие столкновения их с другими, одновременно растущими кристаллами. Такие неправильной формы зерна называются кристаллитами. Вследствие произвольной ориентации отдельных кристаллитов в металле его средние свойства в различных направлениях могут быть одинаковы. Такие металлы называются квазиизотропными. Если металл приобретает преимущественно ориентированное направление кристаллитов, то наблюдается анизотропия его свойств. Анизотропия кристаллов широко используется в технике. При применении особых методов кристаллизации можно получить монокристалл — кусок металла, состоящий из одного кристалла, свободного от трещин и посторонних включений.
Монокристаллы германия, кремния и некоторых металлических соединений теперь применяются в качестве полупроводников. Анизотропия кристаллов широко используется
также для выявления микроструктуры металлов при воздействии на их поверхность растворов кислот, щелочей, солей.
Высокочистые монокристаллы тугоплавких металлов и их сплавов и соединений позволяет получать метод, разработанный специалистами Института металлургии и материаловедения имени А.А. Байкова Российской академии наук, — зонная плазменно-дуговая плавка.
Для современных высоких технологий монокристаллы представляют особый интерес. Ведь свойства любого твердого тела зависят не только от состава, но и от структуры, которая у монокристаллов отличается наибольшей стабильностью. И потому монокристаллы обладают многими куда более качественными характеристиками, нежели те же технические чистые вещества, но с поликристаллической структурой. В частности, монокристаллы обладают более высокой эрозионной и коррозионной стойкостью, лучшей совместимостью с некоторыми агрессивными средами, малым газоотделением при нагревании, а также более высокой пластичностью при одновременной устойчивости формы.
Методом зонной плазменно-дуговой плавки можно получать высокочистые металлические монокристаллы из сырья с высоким содержанием примесей, и притом достаточно больших размеров. Например, кристалл вольфрама диаметром до 50 мм и длиной до 300 мм. Удается даже получать крупные монокристаллы заданной формы — скажем, в виде труб или пластин.
На основе высокочистых монокристаллов молибдена и вольфрама в институте разработаны сплавы для деталей применяемых в СВЧ-технике: анодов, спиралей, подогревателей, сеток и т.д. Пластичность этих материалов позволила обеспечить» необходимую точность геометрии деталей, а высокая устойчивость формы — долговечность работы приборов без изменения рабочих параметров. И наконец, при помощи разработанного в институте метода из расплава были впервые в мире выращены монокристаллы таких химических соединений (карбидов и боридов), которые оказались более тугоплавкими, чем вольфрам — самый тугоплавкий в мире металл. К созданным в институте новым материалам
проявляют интерес специалисты, работающие в области ядерной физики, физики твердого тела, а также занятые использованием материалов для работы в агрессивных средах.
Состав и структура металлических сплавов
Сплавы — металлические, макроскопические однородные системы, состоящие из двух или более металлов (реже металлов и неметаллов), с характерными металлическими свойствами. В широком смысле сплавами называют любые однородные системы, полученные сплавлением металлов, неметаллов, оксидов, органических веществ и т. д.
Сплавы представляют собой сложные тела, получаемые из более простых тел путем диффузии, т.е. взаимного проникновения их частиц. Исходные элементарные тела или химические соединения, из которых образован сплав, при этом в наименьшем числе называется компонетами.
Свойства сплавов определяются их составом и структурой. Компоненты сплавов в процессе кристаллизации могут образовывать механические смеси,, твердые растворы, химические соединения, как это упоминалось выше. Структуры металлических сплавов представляют собой механические смеси, твердые растворы, химические соединения или их различные комбинации.
Сплавы виде механических смесей образуются при полной нерастворимости компонентов друг в друге в твердом состоянии. Кроме того, компоненты не образуют между собой химических соединений. Структура такого сплава под микроскопом (или при рассмотрении невооруженным глазом) состоит из кристаллитов отдельных компонентов. В механические смеси могут входить не только кристаллы исходных элементов, но и кристаллы твердых растворов и химических соединений, образованных этими элементами. В сплаве состоящем из двух металлов, видны кристаллиты обоих металлов. Рентгенографическое исследование такого сплава показывает существование двух типов кристаллических решеток — решеток каждого компонента в сплаве.
По типу механических смесей кристаллизуются сплавы: свинец — сурьма, свинец — олово и др. Механические свойства смесей находятся обычно в пределах свойств исходных компонентов.
Сплавы в виде твердых растворов образуются элементами, которые способны растворяться один в другом не только в расплавленном состоянии, но также и в твердом. В отличии от механической смеси твердый раствор состоит из одного типа кристаллов, имеющих одинаковую кристаллическую решетку.
Твердые растворы — однородные твердые вещества, состоящие из нескольких компонентов, концентрации которых могут быть изменены в некоторых пределах при данных температуре, давлении и т. п. без нарушения однородности. Многие металлические сплавы (например, сталь, бронза), минералы (полевые шпаты, слюды и др.), стекла являются твердыми растворами.
Твердый раствор — это сплав, у которого атомы растворимого элемента рассеяны в кристаллической решетке растворителя. При исследовании структуры твердого раствора под микроскопом обнаруживается ее однородность: она состоит из однородных кристаллов, как и чистые металлы, химический же анализ показывает присутствие двух (или нескольких) элементов. В отличие от химических соединений твердый раствор существует не при строгом определенном соотношении компонентов, а в интервале их концентраций. С помощью рентгеновского анализа выяснилось, что атомы растворенного вещества могут замещать ион-атомы растворителя в .узлах его решетки (твердые растворы замещения) или внедряться в пространство между атомами растворителя (твердые растворы внедрения).
На рис. 4.1а показана кристаллическая решетка чистого металла А., Его ион-атомы отмечены белыми кружками.
В твердых растворах замещения (рис 4.1Ь) растворение компонента В в металле А происходит путем частичного замещения атомами В (черные кружки) ион-атомов А (белые кружки) в решетке металла растворителя А.
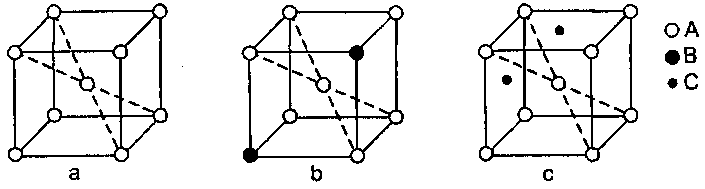
В твердых растворах внедрения (рис. 4.1с)
атомы компонента С
располагаются
между узлами атомов металла-растворителя
А.
В
этом случае диаметр атома компонета С
должен
быть небольшим, чтобы атомы С
поместились
между атомами А.
Поэтому
твердые растворы внедрения образуются
обычно между металлом-растворителем и
компонентом, имеющим небольшой атомный
объем. Они характерны для элементов с
малыми атомными диаметрами: углерода,
азота, бора, образующими твердые растворы
ограниченной растворимости.
твердых растворах внедрения (рис. 4.1с)
атомы компонента С
располагаются
между узлами атомов металла-растворителя
А.
В
этом случае диаметр атома компонета С
должен
быть небольшим, чтобы атомы С
поместились
между атомами А.
Поэтому
твердые растворы внедрения образуются
обычно между металлом-растворителем и
компонентом, имеющим небольшой атомный
объем. Они характерны для элементов с
малыми атомными диаметрами: углерода,
азота, бора, образующими твердые растворы
ограниченной растворимости.
Кроме растворов ограниченной растворимости, могут быть, твердые растворы неограниченной (непрерывной) растворимости.
Непрерывные растворы образуются тогда, когда металлы неограниченно растворяются друг в друге.
Неограниченные твердые растворы образуют железо с| никелем, медь с никелем, золото с серебром, железо с хромом и др.
Сплавы в виде химических соединений металлов или металлов с другими элементами характеризуются постоянством; состава.
Химические соединения имеют иную кристаллическую:; решетку, отличающуюся от кристаллических решеток компонентов, входящих в состав сплава. Микроструктура химических соединений аналогична структуре твердых растворов: (кристаллы имеют вид полиэдров — многогранников).
Химические соединения часто образуются также между* металлами и неметаллами. Некоторые из них1 отличаются высокой твердостью, например, карбиды вольфрама WC^I
W2C, карбид железа Fe3C (цементит), карбид хрома Сг3С, некоторые нитриды и др. Чем более в химических соединениях твердых и хрупких структурных составляющих, тем более повышается твердость сплава, но уменьшается пластичность.
Химические соединения двух и более металлов называют также интерметаллическими.
В настоящее время, в ходе научно-технического прогресса встречаются новые интересные сплавы, например пенометаллы, металлы или сплавы с ячеистой структурой. Они получаются при введении в расплавленный металл гидридов титана, циркония и др., выделяется водород, вспенивающий металл. Получены пенометаллы на основе ,А1, Mg и других металлов. Пенометаллы применяются в качестве наполнителей конструкций, а также как теплоизолирующие материалы и являются весьма перспективными материалами.
Различают также твердые сплавы — материалы с высокими твердостью, прочностью, режущими и др. свойствами, сохраняющимися при нагреве до высоких температур. Различают литые и спеченные (металлокерамические) твердые сплавы. Последние получают методами порошковой металлургии из твердых карбидов металлов, сцементированных пластичным металлом-связкой.
Порошковой металлургией называют производство порошков металлов и изделий из них, их смесей и композиций с неметаллами. Порошки вырабатываются механическим измельчением или распылением жидких исходных металлов, высокотемпературным восстановлением и термической диссоциацией летучих соединений, электролизом и другими методами. Изделия получают обычно прессованием с последующей или одновременно термической, термохимической обработкой без расплавления основного компонента. Методы порошковой металлургии позволяют изготавливать изделия из материалов, получение которых другими способами невозможно (например, из несплавляющихся металлов, композиций металлов с неметаллами) или экономически невы
годно. С помощью порошковой металлургии получают тугоплавкие и твердые материалы и сплавы, пористые, фрикционные и другие материалы и изделия из них.
