
- •Правила охраны труда и техники безопасности
- •Оказание первой помощи
- •Оформление результатов лабораторных работ.
- •Лабораторная работа 1 Анализ воды
- •Определение жёсткости воды
- •Оборудование и реактивы:
- •Экспериментальная часть
- •1. Определение общей щелочности и карбонатной жесткости воды.
- •2. Определение общей жесткости воды комплексонометрическим методом (при помощи трилона б).
- •4. Определение содержания ионов so42- в воде.
- •Лабораторная работа 2 Подготовка воды
- •Оборудование и реактивы:
- •Экспериментальная часть
- •Лабораторная работа 3 Определение скорости движения газа в трубе
- •Экспериментальная часть
- •Лабораторная работа 4 Адсорбционная очистка активированным углем в динамических условиях
- •Оборудование и реактивы
- •Экспериментальная часть
- •Лабораторная работа 5 Адсорбция на активированном угле в статических условиях
- •Оборудование и реактивы:
- •Экспериментальная часть
- •Лабораторная работа 6 Определение коэффициента распределения йода в системе бензин-вода.
- •Оборудование и реактивы
- •Экспериментальная часть
- •Лабораторная работа 7 Термопары
- •Оборудование
- •Экспериментальная часть
- •Вопросы к лабораторным работам.
- •1. Анализ Воды. Подготовка воды.
- •3. Определение скорости движения газа в трубе
- •6. Экстракция. Адсорбция.
- •7. Термопары.
- •Лабораторная работа 8 Ускоренный метод определения содержания серы в технической сере.
- •Оборудование и реактивы:
- •Лабораторная работа 9 Разложение фосфата серной кислотой
- •Расчет производят по формуле:
- •Лабораторная работа 10 Получение извести.
- •Оборудование и реактивы:
- •Экспериментальная часть
- •Лабораторная работа 11 Приготовление легкоплавких стекол
- •Оборудование и реактивы.
- •Экспериментальная часть
Лабораторная работа 4 Адсорбционная очистка активированным углем в динамических условиях
На химических заводах, как правило, проводят адсорбционный процесс непрерывно в динамических условиях. Эти процессы протекают в аппаратах различной конструкции. Сам процесс заканчивается после того как может наступить процесс проскока. Процессом проскока обычно называют процесс, когда концентрация раствора из которого производят процесс адсорбции адсорбируемого вещества, прекращается и концентрация раствора, выходящего из абсорбера , остаётся постоянной. Это же относится к тому случаю, когда процесс протекает в газовой фазе. Поэтому любой адсорбент характеризуется предельной адсорбцией, которая представляет собой массу адсорбированного вещества в кг/м3 адсорбента. Полная ёмкость адсорбента определяется по формуле:
M
W= --------- ,
V
где: W – полная динамическая ёмкость адсорбента, кг/м 3; M – масса адсорбированного вещества, кг; V – объём адсорбента, м3.
Оборудование и реактивы
1.Установка для адсорбции 2. Мензурка, 30мл 3. Колба коническая, 250 мл 4. Бюретка 5. Раствор йода водный 6. Раствор тиосульфата 7. Раствор крахмала 8. Уголь активированный (адсорбент)
Экспериментальная часть
Работу по определению предельной адсорбции проводят на установке,
приведенной на рис. 2.
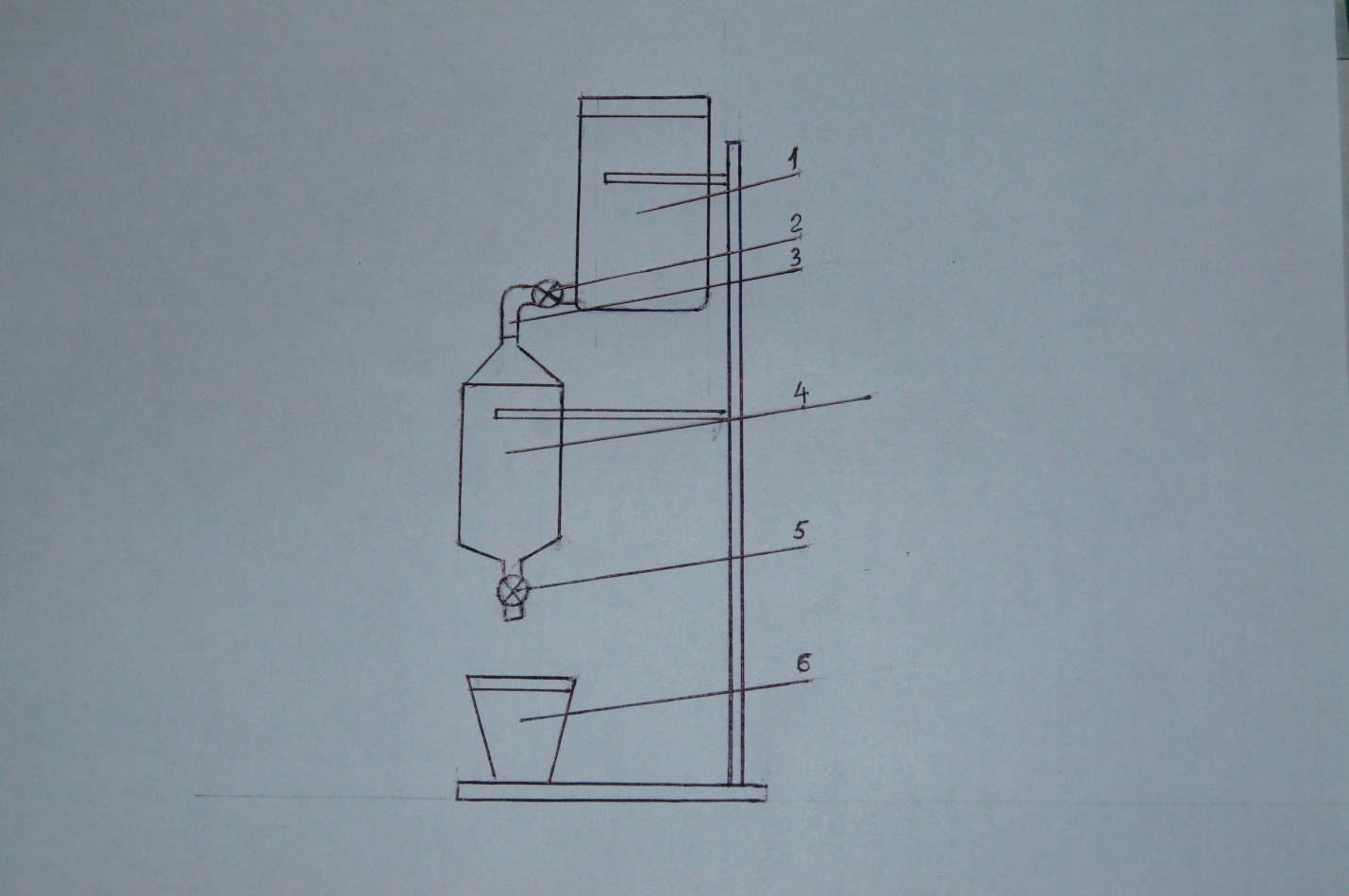 Рис.
2
Рис.
2
Установка состоит из ёмкости с йодом (1), крана (2), трубки (3) для подачи раствора йода в колонку (4) с краном (5) и мензурки (6), в которую отмеряют раствор после адсорбции. Раствор йода определённой концентрации пропускают через фильтр с загрузкой из активированного угля. Для этого открывают кран (2) ёмкости (1) и кран (5) на колонке. Регулируют скорость подачи раствора краном (2) таким образом, чтобы раствор не выливался из колонки. Раствор, проходящий через кран (5) собирают в мензурку ёмкостью 30 мл. Содержимое мензурки, количественно переносят в коническую колбу и титруют тиосульфатом натрия в присутствии раствора крахмала до полного обесцвечивания. Концентрацию йода в растворе, прошедшем через колонку определяют по формуле:
N 1V1 = N2V2 ,
где N1 - концентрация тиосульфата натрия;
V1 - объем раствора тиосульфата натрия;
V2 - объем исследуемого раствора;
N2 - концентрация йода после адсорбции. Эксперимент проводят до тех пор, пока концентрация йода в 3-х последних пробах не станет постоянной.
Полученные данные вносят в таблицу:
№ пробы |
Объём титруемого раствора V1 , мл |
Исходная концентрация йода N1 , гэкв/л |
Объём раствора тио- сульфата V2 , мл |
Концентрация йода, после титрования N2 , гэкв/л |
|
|||||
|
1 |
2 |
3 |
4 |
5 |
|||||
Количество йода, прошедшего через адсорбент, определяют по формуле: M Н = N1 ∙ VН ,
где: M Н – начальная масса йода, прошедшего через колонку, кг ; VН – полный объём раствора йода, прошедшего через колонку, (Σ V1 колонка 2 в таблице), м3. Количество йода в растворе после титрования определяют по формуле:
M К = Σ N2 ∙ V2 ,
где: M К – конечная масса йода, прошедшего через адсорбент, кг. Масса йода адсорбированного на угле составляет:
M = M Н - M К
Предельную ёмкость адсорбента (активированного угля) определяют по формуле: M
W= --------- .
V
