
- •Правила охраны труда и техники безопасности
- •Оказание первой помощи
- •Оформление результатов лабораторных работ.
- •Лабораторная работа 1 Анализ воды
- •Определение жёсткости воды
- •Оборудование и реактивы:
- •Экспериментальная часть
- •1. Определение общей щелочности и карбонатной жесткости воды.
- •2. Определение общей жесткости воды комплексонометрическим методом (при помощи трилона б).
- •4. Определение содержания ионов so42- в воде.
- •Лабораторная работа 2 Подготовка воды
- •Оборудование и реактивы:
- •Экспериментальная часть
- •Лабораторная работа 3 Определение скорости движения газа в трубе
- •Экспериментальная часть
- •Лабораторная работа 4 Адсорбционная очистка активированным углем в динамических условиях
- •Оборудование и реактивы
- •Экспериментальная часть
- •Лабораторная работа 5 Адсорбция на активированном угле в статических условиях
- •Оборудование и реактивы:
- •Экспериментальная часть
- •Лабораторная работа 6 Определение коэффициента распределения йода в системе бензин-вода.
- •Оборудование и реактивы
- •Экспериментальная часть
- •Лабораторная работа 7 Термопары
- •Оборудование
- •Экспериментальная часть
- •Вопросы к лабораторным работам.
- •1. Анализ Воды. Подготовка воды.
- •3. Определение скорости движения газа в трубе
- •6. Экстракция. Адсорбция.
- •7. Термопары.
- •Лабораторная работа 8 Ускоренный метод определения содержания серы в технической сере.
- •Оборудование и реактивы:
- •Лабораторная работа 9 Разложение фосфата серной кислотой
- •Расчет производят по формуле:
- •Лабораторная работа 10 Получение извести.
- •Оборудование и реактивы:
- •Экспериментальная часть
- •Лабораторная работа 11 Приготовление легкоплавких стекол
- •Оборудование и реактивы.
- •Экспериментальная часть
Оборудование и реактивы:
Муфельная печь
Аналитические весы
Фарфоровые тигли
Стакан химический – 200 мл
Колба мерная – 250 мл
Колба коническая – 250 мл
Микробюретка
Стекло часовое
Калия гидроксид
Спирт этиловый
Фенолфталеин
Для определения содержания серы в образце ускоренным методом достаточно провести анализ ее на содержание золы (х3) и кислот (хК).
Содержание серы (в %) хs вычисляют по формуле

Порядок выполнения работы. Определение содержания золы.
20 г серы взвешивают с погрешностью не более 0,001 и помещают в фарфоровый, низкий тигель № 5, предварительно прокаленный и взвешенный с погрешностью не более 0,001 г. Затем серу медленно сжигают.
Содержание (в %) золы х3 вычисляют по формуле
 ,
,
где: g и g1 - массы навесок серы и остатка после прокаливания, г.
За результат анализа принимают среднее арифметическое из двух параллельных определений, допускаемые расхождения между которыми не должны превышать 0,005 %.
Определение содержания кислот в пересчете на серную кислоту.
2 г серы взвешивают с погрешностью не более 0,01 г, помещают в коническую колбу, смачивают 2 мл этилового спирта и добавляют 20 мл воды. Смесь перемешивают, колбу накрывают часовым стеклом и кипятят в течение 15-20 мин, периодически перемешивая. После охлаждения содержимое колбы фильтруют через складчатый бумажный фильтр в мерную колбу (100 мл), доводят объем раствора до метки водой, не содержащей диоксида углерода и тщательно перемешивают, переносят раствор в коническую колбу ( 250 мл) и титруют из микробюретки 0,01 н. раствором гидроксида натрия в присутствии фенолфталеина до светло-розовой окраски.
Содержание
(в %) кислот
 в пересчете на серную кислоту вычисляют
по формуле:
в пересчете на серную кислоту вычисляют
по формуле:
V ∙ 0,00049∙100
= ------------------------ ∙ 100 ,
g
где: V - объем 0,01 н. растворов NaOH, пошедшие на титрование анализируемого раствора, мл;
0,00049 - масса серной кислоты, эквивалентная массе NaOH , содержащейся в 1 мл 0,01 н. раствора NaOH , г;
g - масса навески серы, г.
За результат анализа принимают среднее арифметическое двух параллельных определений, допускаемые расхождения между которыми не должны превышать 0,001 %.
Лабораторная работа 9 Разложение фосфата серной кислотой
Удобрения применяются для повышения урожайности. По своему характеру они подразделяются на органические и неорганические. Неорганические удобрения можно подразделить исходя из:
- простые, содержащие только один активный элемент;
- смешанные, содержащие два или более активных элементов, полученные смешиванием простых удобрений;
- сложные, содержащие два или более активных элементов в химически связанной форме;
- в зависимости от содержания элемента или элементов (азотные, фосфорные, калийные).
Исходным сырьём для получения фосфорных удобрений является фосфорит или апатит, содержащие различные количества активного оксида фосфора, (Р2О5).

Для анализа берут навеску фосфата 1-1,5 г, помещают в фарфоровый стакан, смачивают водой, добавляют рассчитанное согласно уравнению реакции количество концентрированной серной кислоты и ставят на водяную баню на 40 минут. Затем осадок отфильтровывают через плотный фильтр в мерную колбу на 200 мл. Осадок промывают на фильтре дистиллированной водой, в фильтрате определяют трилонометрически ионы кальция. Поэтому способу определяется водорастворимая форма Р2О5 , связанная с ионами кальция в виде Са(Н2РО4)2 . Свободная фосфорная кислота определяется в той же водной вытяжке титрованием 0,1н раствором гидроксида натрия в присутствии метилового оранжевого.
Анализируемый раствор наливают в бюретку и титруют 0,1 н раствором трилона Б. Для этого 10 мл титрованного раствора трилона Б (точно из бюретки) наливают в коническую колбу, добавляют 70-80 мл дистиллированной воды, 5 мл аммиачного буферного раствора, несколько кристалликов индикатора эриохрома черного и медленно титруют анализируемым раствором, энергично встряхивая последний, добавлением каждой капли до перехода синей окраски в малиновую. Для каждого анализа титруют три параллельные пробы, причем первое титрование является ориентировочным, при котором грубо определяется объем анализируемого раствора, требуемый для изменения окраски индикатора.
Содержание СаО в растворе (вес.%) рассчитывают по формуле:
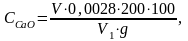
где V - объем 0,1 н раствора трилона Б;
V1 - объем анализируемого раствора, израсходованный на титрование;
g - навеска фосфата;
0,0028 - количество СаО, эквивалентное содержанию трилона Б в 1 мл
0,1 н раствора, г.
Полученные результаты, пересчитывают на содержание в растворе Р2О5 (вес.%), связанной с СаО по формуле:

где СCаО - содержание СаО в растворе, вес.%.
Определение содержания свободной фосфорной кислоты производят титрованием 10 мл той же водной вытяжки из фосфата, что и для определения СаО, 0,1 н раствором гидроксида натрия в присутствии метилового оранжевого.
