
- •Предмет и задачи биофизики. История развития биофизики. Разделы биофизики.
- •Особенности кинетики биологических процессов. Параметры и переменные. Влияние концентраций на скорость реакций. Понятие «узкого места».
- •Механизмы первичных реакций в организме при размене физической энергии на химическую (теория мишени, теория непрямого действия, теория цепных процессов).
- •Влияние температуры на скорость реакций в биологических системах.
- •Перекисное окисление липидов в мембранах. Биологические последствия пероксидации липидов.
- •Кинетика ферментативных реакций (уравнения Михаэлиса-Ментен).
- •Чувствительность различных биологических объектов к радиации. Действие ионизирующего облучения на живые системы.
- •Аллостерическое и конкурентное ингибирование ферментативных реакций. Субстратное торможение. Индукция и репрессия синтеза ферментов (по Жакобу и Моно).
- •Статистический характер организации биополимеров (на примере двумерной свободно сочлененной полимерной цепи).
- •Раздел III. Пространственная организация биополимеров
- •Глава VII. Пространственные конфигурации полимерных молекул (стр. 167 - 182)
- •§1. Статистический характер организации полимеров
- •Множественность стационарных состояний. Модели триггерного типа. Силовое и параметрическое переключение триггера. Гистерезисные явления.
- •Транспорт электролитов (электрохимический потенциал, электродиффузионное уравнение Нернста-Планка , гидратация ионов).
- •Классификация термодинамических систем. Первый закон термодинамики и его применимость в биологии. Закон Гесса.
- •Транспорт электролитов (ионное равновесие на границе мембрана-раствор, равновесие Доннана).
- •Второй закон термодинамики. Понятие градиента. Энтропия, свободная и связанная энергия.
- •Пространственная конформация биополимеров (стереоспецифичность аминокислот, первичная, вторичная, третичная, четверичная структура белка).
- •Вида ионизирующих излучений. Единицы измерения дозы ионизирующего излучения.
- •Изменение энтропии в открытых системах. Стационарные состояния и состояния термодинамического равновесия. Принцип Ле-Шателье.
- •Механно-химические процессы в полимерах.
- •Активный транспорт (участие атф-аз вм активном транспорте ионов через биологические мембраны).
- •Переносчики и каналы.
- •Устойчивость и неустойчивость стационарного состояния (на примере гидродинамической модели).
- •1. Кинетические уравнения Лотки (a.J. Lotka. Elements of Physical Biology, 1925)
- •2. Модель Вольтерра
- •(По к. Вилли, в. Детье, 1974)
- •Активный транспорт (электрогенный транспорт ионов – опыт Уссинга и ).
- •Понятие обобщенных сил и потоков. Соотношение взаимности Онзагера. Теорема Пригожина.
- •Простая и облегченная диффузия.
- •Кооперативные свойства макромолекул (механизм кооперативного связывания кислорода гемоглобином и миоглобином).
- •Потенциал покоя и его происхождение.
- •[Править]История открытия
- •[Править]Общие положения
- •[Править]Формирование потенциала покоя
- •Поверхностный заряд мембранных систем (происхождение дзета-потенциалов – представление Гельмгольца, Гуи, Штерна; определение дзета-потенциалов).
- •Состояние воды и гидрофобные взаимодействия.
- •Потенциал действия (изменение электропроводной мембраны, потоки ионов натрия и калия, схема функционирования натриевого канала при возбуждении). Распространение возбуждения.
- •Роль гидрофобных взаимодействий в формировании структуры белков. Переход спираль-клубок. Переход глобула-клубок.
- •Переход клубок—глобула
- •Транспорт неэлектролитов (проницаемость мембран для воды, роль коллоидно-осмотического давления плазмы в переносе воды).
- •Электропроводность биосистем (закономерности происхождения постоянного тока через биологические объекты; явления поляризации).
- •Сокращение мышцы (схема взаимодействия актина и миозина по а.Хаксли).
- •Электропроводность биосистем (закономерности происхождения переменного тока через биологические объекты; дисперсия электропроводности).
- •5. Живая ткань как проводник переменного электрического тока. Дисперсия
- •Химия и физика мышцы (схема взаимодействия актина с миозином по Хаксли, кривая зависимости скорости изотонического сокращения от величины нагрузки по Хиллу).
- •Структура биомембран: развитие представление о структуре, модельные мембранные системы.
- •Ковалентные и слабые связи.
- •21. Слабые связи.
- •Динамические модели биологических систем. Понятие фазовой плоскости. Фазовой портрет системы.
- •12. Понятие фазовой плоскости. Фазовый портрет системы.
- •Свободные радикалы. Методы изучения. Классификация свободных радикалов.
- •Классификация свободных радикалов, образующихся в нашем организме
- •Первичные радикалы (радикалы кислорода, окись азота, радикал коэнзима q). Первичные радикалы
- •Активные формы кислорода
- •Окись азота
- •Радикал коэнзима q
- •Клеточные системы антирадикальной защиты.
- •Динамика мембран. Фазовые переходы в липидном бислое.
- •Слабые взаимодействия (ион-ионное взаимодействие, диполь-дипольное взаимодействие, наведенные диполи, лондоновские или дисперсные силы).
- •Свойства
- •Слабый распад
- •Дисперсионное взаимодействие
- •Характеристика ковалентной связи.
1. Кинетические уравнения Лотки (a.J. Lotka. Elements of Physical Biology, 1925)
Лоткой была исследована гипотетическая химическая реакция:
![]()
Модель очень простая и служит хорошей иллюстрацией применения исследования устойчивости стационарного состояния системы методом линеаризации.
Пусть
в некотором объеме находится в избытке
вещество А. Молекулы А с
некоторой постоянной скоростью ![]() превращаются
в молекулы вещества X (реакция
нулевого порядка). Вещество Xможет
превращаться в вещество Y, причем
скорость этой реакции тем больше, чем
больше концентрация вещества Y –
реакция второго порядка. В схеме это
отражено обратной стрелкой над символом Y.
Молекулы Y в
свою очередь необратимо распадаются,
в результате образуется вещество B (реакция
первого порядка).
превращаются
в молекулы вещества X (реакция
нулевого порядка). Вещество Xможет
превращаться в вещество Y, причем
скорость этой реакции тем больше, чем
больше концентрация вещества Y –
реакция второго порядка. В схеме это
отражено обратной стрелкой над символом Y.
Молекулы Y в
свою очередь необратимо распадаются,
в результате образуется вещество B (реакция
первого порядка).
Запишем систему уравнений, описывающих реакцию:
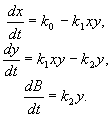 (5.13)
(5.13)
Здесь x, y, B - концентрации химических компонентов. Первые два уравнения этой системы не зависят от B, поэтому их можно рассматривать отдельно. Рассмотрим стационарное решение системы:
![]()
Из этих
условий получим систему алгебраических
уравнений, связывающих равновесные
концентрации![]() :
:
![]() (5.14)
(5.14)
Координаты особой точки:
![]() .
.
Исследуем устойчивость этого стационарного состояния методом Ляпунова. Введем новые переменные , , характеризующие отклонения переменных от равновесных концентраций :
![]() .
.
Линеаризованная система в новых переменных имеет вид:
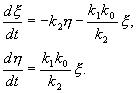 (5.15)
(5.15)
Отметим, что величины отклонений от стационарных значений переменных , могут менять знак, в то время как исходные переменные x, y, являющиеся концентрациями, могут быть только положительными.
Запишем характеристическое уравнение системы (4.3):
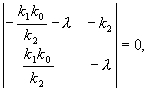
или
![]() .
.
Корни характеристического уравнения:
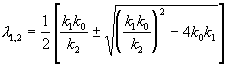 .
.
Фазовый портрет системы (5.13) изображен на рис. 5.1.
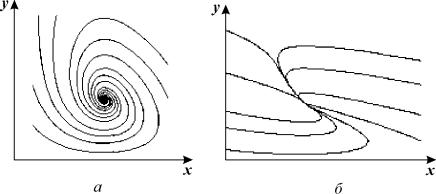
Рис. 5.1. Фазовый портрет системы 5.13.
а
– устойчивый
фокус, ![]()
б
– устойчивый
узел. ![]()
При ![]() подкоренное
выражение отрицательно, и особая точка
– фокус, при обратном соотношении –
узел. И в том и в другом случае особая
точка устойчива, так как действительная
часть обоих корней характеристического
уравнения отрицательна.
подкоренное
выражение отрицательно, и особая точка
– фокус, при обратном соотношении –
узел. И в том и в другом случае особая
точка устойчива, так как действительная
часть обоих корней характеристического
уравнения отрицательна.
Таким
образом, в описанной выше химической
реакции возможны разные режимы изменения
переменных в зависимости от соотношения
величин констант скоростей. Если ![]() ,
имеют место затухающие колебания
концентраций компонентов, при
–
бесколебательное приближение концентраций
к стационарным.
,
имеют место затухающие колебания
концентраций компонентов, при
–
бесколебательное приближение концентраций
к стационарным.
-
Рис. 5.2 Плоскость параметров для системы 5.14.
а – область устойчивого фокуса; б– область устойчивого узла
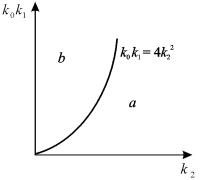
Соотношение параметров соответствует изменению типа особой точки системы уравнений (5.13).
Рассмотрим плоскость параметров, где по оси абсцисс отложены значения константы k2, а по оси ординат – произведение k0 k1. Парабола k0 k1 = 4 k22 делит изображенную на рис. 5.2 плоскость параметров на две области – устойчивых узлов и устойчивых фокусов. Задавая те или иные значения параметров, можно получить колебательный и бесколебательный режимы изменения концентраций веществ x и y, и фазовый портрет системы, соответственно, будет собой представлять фокус (а) или узел (б), изображенные соответственно на рис 5.1а, и 5.1б.
Если в системе установятся стационарные концентрации веществ x и y, это приведет к установлению постоянной скорости прироста концентрации вещества В в третьем уравнении системы (5.13):
![]() .
.
Ясно, что в действительности такая система реализоваться не может, так как в ней при t концентрация вещества В стремится к бесконечности. Однако система, подобная системе реакций Лотки, может представлять собой фрагмент более сложной химической системы. Исследованные нами уравнения правильно описывают поведение компонентов x и y, если приток вещества x (скорость его постоянна и равна k0) осуществляется из большого «резервуара», а отток вещества y – в большой «резервуар» (значение В очень велико). При этих предположениях на малых промежутках времени (по сравнению с временем существенного изменения заполненности емкости B) наше рассмотрение является вполне правомерным.
