
- •Введение
- •Лабораторная работа № 1 исследование зависимости между структурой и механическими свойствами чугунов
- •1.1. Цели работы
- •1.2. Теоретическая часть
- •1.3. Оборудование, инструмент и материалы
- •1.4. Методика выполнения работы
- •1.5. Содержание отчета
- •1.6. Контрольные вопросы
- •Лабораторная работа № 2 исследование роста кристаллов для системы Fe-Ni
- •2.1. Цели работы
- •2.2. Теоретическая часть
- •2.3. Оборудование, инструмент и материалы
- •2.4. Методика выполнения работы
- •2.5. Содержание отчета
- •2.6. Контрольные вопросы
- •Диаграмма состояния Fe-Ni
- •Составители: деменок Олег Борисович
- •4 50000, Уфа-центр, ул. К. Маркса,12
Лабораторная работа № 2 исследование роста кристаллов для системы Fe-Ni
2.1. Цели работы
2.1.1. Изучение основных закономерностей процесса зарождения и роста кристаллов металлической системы Fe - Ni.
2.1.2. Приобретение умения и навыков моделирования влияния величины переохлаждения на радиус зародыша кристалла с помощью программы "Кристалл" и величины переохлаждения на скорость возникновения центров кристаллизации.
2.1.3. Исследование влияния величины переохлаждения на скорость роста кристаллов.
2.1.4. Овладение методиками выполнения работы, обработки и анализа полученных экспериментальных данных результатов исследования.
Работа рассчитана на 4 часа.
2.2. Теоретическая часть
Под кристаллизацией в теории литейных процессов понимается формирование структуры отливок при переходе металла из жидкого состояния в твёрдое.
Значение химического состава зародыша в процессе формирования химической неоднородности практически не изучено. Форма зародышей не очень ясна. В общем виде новая фаза для обеспечения минимальной энергии должна иметь шаровидную форму. Однако в силу анизотропии свойств кристаллов шаровидная форма, вероятно, не является оптимальной для свободно растущего кристалла. Даже если форма зародыша напоминает шар, то она имеет вид куба с усеченными вершинами (кандодегаэдрон), ограниченного соответственно шестью квадратными (100) и гексагональными (111) плоскостями. Такой зародыш (рисунок 2.1) может расти с помощью присоединения целых слоев по граням. При присоединении слоя атомов на плоскость (111) одновременно увеличиваются и размеры плоскости (100).
Согласно молекулярно-кинетической теории кристаллизации М. Фольмера, Я. И. Френкеля и В. И. Данилова, самопроизвольное возникновение центров кристаллизации происходит при наличии в жидкости гетерофазных флуктуации – небольших участков, имеющих такое же расположение молекул, как в кристалле. На образование поверхности раздела кристаллика в переохлаждённой жидкости должна быть затрачена некоторая энергия.
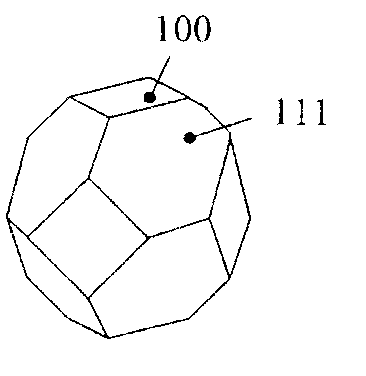
Рис.2.1. Возможная структура критического зародыша
Если кристалл
меньше некоторой определенной величины,
эта затрата энергии превышает выигрыш
в энергии, связанный с переходом в более
устойчивое состояние, и кристалл будет
плавиться. Если кристалл больше
критической величины, его рост будет
энергетически выгоднее, чем плавление.
Чем больше переохлаждение, тем меньше
размер критического зародыша и больше
вероятность возникновения кристаллов.
Вероятность зарождения центров
кристаллизации в переохлаждённом
металле будет пропорциональна
![]() ,
где Ак
– работа образования критического
зародыша, выражаемая при определенных
допущениях формулой
,
где Ак
– работа образования критического
зародыша, выражаемая при определенных
допущениях формулой
Ак
=![]() , (2.1)
, (2.1)
где В
– постоянная для данного вещества
величина, связанная с его молекулярным
весом, теплотой кристаллизации, плотностью
и теплотой плавления;
![]() – поверхностное натяжение па границе
фаз; ΔT
– переохлаждение.
– поверхностное натяжение па границе
фаз; ΔT
– переохлаждение.
Скорость возникновения центров кристаллизации описывается формулой
![]() , (2.2)
, (2.2)
где k – постоянная Больцмана; М1 – величина, определяющая скорость обмена атомами между зародышем и окружающей средой, равная
![]() ,
(2.3)
,
(2.3)
где С1 – множитель, который должен иметь тот же порядок, что и количество атомов в данном объёме жидкости, т.е. С1≈1023; U – энергия активации атомов в расплаве.
Подставляя все коэффициенты в уравнение (2.2) получим
![]() , (2.4)
, (2.4)
Равновесный зародыш
кристаллизации должен иметь огранку.
Его дальнейший рост уже как кристалла
может происходить различными способами.
Одна из вероятных систем роста
представляется в форме образования на
грани кристалла двумерных зародышей.
Увеличение этих зародышей по периметру,
более вероятно, чем по высоте. Такой
двумерный рост приведет к зарастанию
всей грани новым слоем (рисунок 2.2). Далее
картина будет последовательно повторяться.
С этой точки зрения скорость кристаллизации
![]() можно описать уравнением, похожим на
равенство, описывающее скорость
возникновения центров кристаллизации
можно описать уравнением, похожим на
равенство, описывающее скорость
возникновения центров кристаллизации
![]() (2.5)
(2.5)
где С2
– множитель, который должен иметь
порядок величины, соответствующей числу
атомов на грани кристалла (принимается,
что для 1 моля С2
= 1016);
L
– энергия активации, определяющая
скорость обмена атомами между зародышем
и расплавом (принимается, что L≈0,25
U);
![]() – граничная энергия на периферии
двумерного зародыша, D
– постоянная для данного вещества
величина.
– граничная энергия на периферии
двумерного зародыша, D
– постоянная для данного вещества
величина.
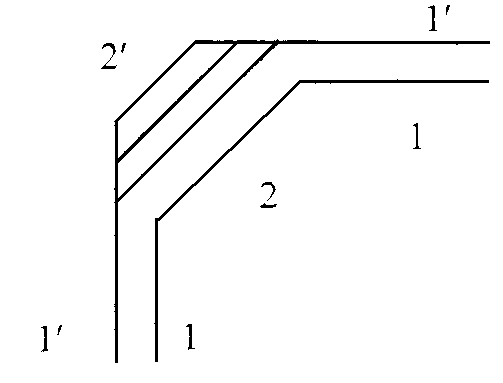
Рис.2.2. Влияние скорости роста на форму кристалла
Радиус зародыша можно определить по формуле
![]() (2.6)
(2.6)
где rk – радиус сферы, вписанной в куб; М – молекулярная масса; ρ – плотность зародыша; σ – поверхностное натяжение между твёрдой и жидкой фазами; Т0 – температура равновесия кристалл - жидкость; Т – температура, до которой жидкий металл переохлаждён;
q – теплота плавления металла. Для вычисления критического радиуса зародыша необходимо знать величину σ. В ряде работ величину σ жидких металлов вычисляют, исходя из потенциальной энергии наружных атомов. Впервые такую трактовку предложил в 1947 году Я.И. Френкель. Он исходил из того, что величина σ определяется электростатической энергией двойного электрического слоя, существующего на поверхности жидкого металла. Впоследствии эта теория была уточнена путем учёта влияния кинетической энергии электронов, однако окончательного выражения для определения величины о чистых металлов расчетным путем еще не получено. В связи с этим имеется большое число эмпирических и полуэмпирических формул, связывающих величину поверхностного натяжения металлов с другими физическими характеристиками. Прямые методы определения величины σ затруднительны, поэтому можно сделать оценку этой величины, исходя из предположения о том, что максимальная величина переохлаждения соответствует случаю гомогенного зарождения.
Для железа и никеля переохлаждение составляет соответственно 295 и 319°С. Весьма близко для этих металлов и значение отношения свободной поверхностной энергии к атомной скрытой теплоте плавления σ/q ≈ 0,45. Оценка размера зародыша, исходя из этих положений, дает величину порядка 200 – 400 атомов.
