
- •Вопрос 1 Сырье для производства синтетического аммиака. Способы получения водорода и азота
- •Двухступенчатая организация конверсии природного газа.
- •Вопрос 2 Паровая конверсия природного газа: реакции и равновесие процесса.
- •Вопрос 3 Паровая конверсия природного газа: катализаторы.
- •Паровая конверсия природного газа: кинетика.
- •Параметры первой ступени конверсии природного газа.
- •Оборудование конверсии природного газа 1 ступени. Многорядная трубчатая печь.
- •Вопрос 4 Методика расчета материального баланса радиантной зоны трубчатой печи
- •Вопрос 5 Методика расчета теплового баланса радиантной зоны трубчатой печи
- •Вопрос 6 Двухступенчатая организация процесса конверсии природного газа.
- •Особенности второй ступени конверсии.
- •Реакции и равновесие процесса
- •Вопрос 7 Паровоздушная конверсия метана: кинетика, катализаторы и параметры процесса.
- •Вопрос 8 Оборудование стадии паровоздушной конверсии природного газа
- •9. 10. Двухступенчатая организация конверсии монооксида углерода. Конверсия монооксида углерода: реакции и равновесие процесса.
- •Методика расчета материального баланса процесса конверсии со.
- •Методика расчета теплового баланса конвертора со .
- •Очистка конвертированного газа от диоксида углерода. Требования, предъявляемые к хемосорбенту и массообменной аппаратуре.
- •Моноэтаноламиновая очистка: реакции, равновесие, кинетика и параметры процесса.
- •15. Оборудование стадии очистки конвертированного газа от диоксида углерода и регенерации раствора
- •Технологическая схема мэа-очистки.
- •Очистка конвертерного газа от со2 по методу «карсол».
- •18.Физико-химические свойства nн3.Требования к качеству nн3.Синтез nн3 :реакция,равновесие процесса
- •Требования к качеству продукционного nн3 по гост 6221 – 90.
- •19.Синтез аммиака: кинетика, механизм реакции, катализаторы и параметры процесса.
- •20. Оборудование стадии синтеза nн3.Технологические особенности производств
- •23.Производство нак. Сырье. Требования к качеству продукционной кислоты. Стадии производства.Балансовая реакция получения hno3 и расчет расходных коэффициентов. Стадия контактного окисления аммиака…
- •25.Гомогенное окисление монооксида азота: реакции, равновесие, кинетика и параметры процесса.
- •27. Переработка оксидов азота в азотную кислоту: реакции, равновесие, кинетика и параметры процесса.
- •28. Оборудование стадии абсорбции нитрозных газов.
- •30.Методика расчета материального баланса первой тарелки абсорбционной колонны в производстве азотной кислоты.
- •31. Методика расчета теплового баланса первой тарелки абсорбционной колонны в производстве азотной кислоты.
- •33. Сырье и требования к качеству продукционного карбамида. Физико-химические свойства карбамида. Синтез карбамида: реакции и равновесие процесса.
- •34. Синтез карбамида: кинетика и параметры процесса. Диаграмма состояния системы.
- •35. Оборудование стадии синтеза карбамида. Расходные коэффициенты на 1 т карбамида. Технологические особенности производства карбамида.
- •36. Технологические схемы получения карбамида.
- •Вопрсо№39: Методика расчета материального баланса аппарата итн
- •Способы получения элементарной серы. Добыча серы. Требования к качеству серы.
- •Сырье для производства h2so4. Серный колчедан и др. Сернистые соединения металлов, газы цветной металлургии, сульфаты Ca, k, Fe.
- •Газы цветной металлургии
- •Физико-химические основы процесса горения серы. Печи для сжигания жидкой серы. Утилизация теплоты горения серы.
- •Методика расчета материального баланса циклонной печи.
- •Методика расчета теплового баланса циклонной печи.
- •47. Равновесие и кинетика процесса окисления диоксида серы
- •48. Катализаторы для окисления диоксида серы. Контактные аппараты для окисления диоксида серы.
- •49. Методика расчета материального баланса контактного аппарата
- •50. Методика расчета теплового баланса контактного аппарата
- •51.Равновесие и кинетика процесса абсорбции триоксида серы.
- •Аппаратурное оформление стадии абсорбции. Моногидратный абсорбер. Олеумный абсорбер, сушильная башня.
- •53.Методика расчета материального баланса моногидратного абсорбера.
- •55. Технологическая схема печного отделения.
- •56. Технологическая схема контактно-компрессорного отделения.
- •57. Технологическая схема сушильно-абсорбционного отделения.
- •58.Способы производства и применение фосфорной кислоты. Сырье и требования к качеству продукционной фосфорной кислоты. Стадии технологического процесса.
- •Разложение апатитового концентрата смесью серной и фосфорной кислот
- •Фильтрация фосфополугидрата на вакуумных фильтрах, гидроудаление
- •Упаривание (концентрирование) фосфорной кислоты
- •Абсорбция газов
- •59.Химизм процесса взаимодействия фосфатов с кислотами. Кинетика процесса разложения фосфатов.
- •Скорость процесса разложения фосфатов (Кинетика)
- •60.Кристаллизация сульфата кальция и условия образования крупнокристаллического осадка.
- •61.Режимы экстракции фосфорной кислоты. Оборудование для экстракции фосфорной кислоты.
- •62.Выделение и улавливание фтора при получении и переработке эфк. Оборудование стадии.
- •63.Методика расчета материального баланса отделения экстракции в производстве дигидратной эфк.
- •64.Методика расчета теплового баланса отделения экстракции в производстве дигидратной эфк.
- •65. Производство сложных удобрений на основе эфк. Свойства фосфатов аммония. Физико-химические особенности производства аммофоса и фосфатов аммония.
- •Физико-химические особенности н а рисунке показаны изотермы растворимости в системе аммиак – фосфорная кислота – вода при 25 и 75 ºС. Взаимодействие эфк с nh3 происходит по реак-ям (1)-(3).
- •66 Вопрос. Основное оборудование стадий нейтрализации, гранулирования и сушки при получении фосфатов аммония: струйный реактор, саи, аг, сб, бгс.
- •68. Производство диаммонийфосфата, особенности технологии. Требования на даф
- •1. Привести расчет величин δн и δg для I ступени паровой конверсии природного газа.
- •8. Дать полную характеристику колонне синтеза, как реактору для получения карбамида. Материал колонны синтеза.
- •9. Основные стадии процесса окисления аммиака до оксида азота(2), как гетерогенно-каталитического хтп.
- •12 Дать полную характеристику абсорбционной колонне , как реактору получения нак. Материал абсорбционноц колонны.
- •13. Уравнение адиабаты. Зависимость степени превращения оксидов азота в азот для необратимой экзотерм. Реакции (графическая и аналитическая зависимости)
- •14. Дать полную характеристику аппарата типа “кипящий слой”, рассчитать критическую скорость псевдоожижения.
- •15. Интенсификация работы оборудования и пути ее увеличения.
- •17.Охт. Дать полную характеристику экстрактору, как реактру для получения эфк.
Газы цветной металлургии
При обжиге руд цветных металлов (медных, цинковых, свинцовых) или их концентратов образуются газы, содержащие SO2. При получении, например, 1 т меди можно получить сернистого ангидрида в количестве, эквивалентном 10 т серной кислоты. При этом сырье для серной кислоты получается без затрат на строительство и эксплуатацию печного отделения сернокислотного цеха, отбросные сернистые газы утилизируются, что оздоровляет среду на металлургических заводах и в близлежащих районах. В металлургической промышленности отходящие газы называются по названию печей, из которых они выходят: обжиговые, ватержакетные, конвертерные, газы отражательных печей. Состав этих газов приведен в табл. 5.
Состав газов зависит от сырья, состояния аппаратуры, условий процесса обжига, поэтому он значительно колеблется. Для улучшения качества огарка, получаемого при обжиге руд цветных металлов и используемого в цветной металлургии, а также для интенсификации обжига применяют кислородное дутье или ведут обжиг в атмосфере технологического кислорода. При этом концентрация SO2 в отходящих газах увеличивается.

Физико-химические основы процесса горения серы. Печи для сжигания жидкой серы. Утилизация теплоты горения серы.
Физико-химические основы процесса горения серы.
Сжигание S происходит с выделением большого количества теплоты: 0,5S2г + О2г = SО2г, ΔН = -362,43 кДж
Горение – комплекс химических и физических явлений. В устройстве для сжигания приходится иметь дело со сложными полями скоростей, концентраций и температур, которые трудно поддаются математическому описанию.
Горение расплавленной S зависит от условий взаимодействия и сгорания отдельных капель. Эффективность процесса горения определяется временем полного сгорания каждой частички серы. Горению серы, которое происходит только в газовой фазе, предшествует испарение S, смешение её паров с воздухом и прогрев смеси до t, обеспечивающей необходимую скорость реакции. Поскольку интенсивнее испарение с поверхности капли начинается лишь при определенной t – каждая капля жидкой серы должна быть нагрета до этой t. Чем выше t, тем больше времени потребуется для прогрева капли. Когда над поверхностью капли образуется горючая смесь паров S и воздуха предельной концентрации и t, происходит воспламенение. Процесс горения капли S зависит от условий горения: t и относительной скорости газового потока, и физико-хим-х свойств жидкой S (например, наличие в S твердых примесей золы), и состоит из стадий: 1-смешение капель жидкой S с воздухом; 2-прогрев этих капель и испарение; 3-термическое расщепление паров S; 4-образование газовой фазы и её воспламенение; 5-горение газовой фазы.
Эти стадии протекают почти одновременно.
В результате прогрева капля жидкой S начинает испаряться, пары S диффундируют к зоне горения, где при высокой t начинают активно реагировать с О2 воздуха, происходит процесс диффузионного горения S с образованием SО2.
При высоких t скорость реакции окисления S больше скорости физических процессов, поэтому общая скорость процесса горения определяется процессами массо- и теплоотдачи.
Молекулярная диффузия определяет спокойный, сравнительно медленный процесс горения, а турбулентная ускоряет его. С уменьшением размера капель сокращается время их испарения. Мелкое распыление частиц серы и равномерное распределение их в воздушном потоке увеличивает поверхность контакта, облегчает нагрев и испарение частиц. При горении каждой единичной капли S в составе факела следует различать 3 периода: I-инкубационный; II-интенсивного горения; III-период догорания.
При горении капли с ее поверхности происходят выбросы пламени, напоминающие собой солнечные вспышки. В отличие от обычного диффузионного горения с выбросом языков пламени с поверхности горящей капли получило название «взрывного горения».

Горение
капли S в диффузионном
режиме осуществляется путем испарения
молекул с поверхности капли. Скорость
испарения зависит от физических свойств
жидкости и t окружающей
среды, а определяется характеристикой
скорости испарения. В дифференциальном
режиме S горит в I
и III периодах. Взрывное
горение капли наблюдается только в
периоде интенсивного горения во II
периоде. Продолжительность периода
интенсивного горения пропорциональна
кубу начального диаметра капли. Это
вызвано тем, что взрывное горение
является следованием процессов,
протекающих в объеме капли. Характеристика
скорости горения вычисл. по ф-ле: К=
 /τсг;
/τсг;
dн – начальный диаметр капли, мм; τ – время полного сгорания капли, с.
Характеристика скорости горения капли равна сумме характеристик диффузионного и взрывного горения: К = Квз + Кдиф; Квз = 0,78∙ехр(-(1,59∙р)2,58); Кдиф = 1,21∙р +0,23; КТ2 = КТ1∙ехр(Еа/R∙(1/Т1 – 1/Т2)); КТ1 – константа скорости горения при t1 = 1073 К. КТ2 – конст. скорости грения при t отличной от t1. Еа – энергия активации (7850 кДж/моль).
Т.О. основными условиями эффективного горения жидкой S являются: подвод всего необходимого количества воздуха к устью факела, мелкое и равномерное распыление жидкой S, турбулентность потока и высокая t.
Общая зависимость интенсивности испарения жидкой S от скорости газа и t: К1 = a∙V/(b+V); a, b – константы, зависящие от t. V – скор. газа, м/с. При более высоких t зависимость интенсивности испарения S от скорости газа им вид: К1 = Ко ∙ Vn;
t,оС |
lgКо |
n |
300 |
4,975 |
0,58 |
400 |
5,610 |
0,545 |
440 |
6,332 |
0,8 |
При увеличении t от 120 до 180оС интенсивность испарения S возрастает в 5-10 раз, а т 180 до 440оС в 300-500 раз.
Интенсивность
испарения при скорости газа 0,104 м/с
определяется:
 = 8,745 – 2600/Т (при 120-140 оС);
=
7,346 – 2025/Т (при 140-200 оС);
=
10,415 – 3480/Т (при 200-440 оС).
= 8,745 – 2600/Т (при 120-140 оС);
=
7,346 – 2025/Т (при 140-200 оС);
=
10,415 – 3480/Т (при 200-440 оС).
Чтобы определить интенсивность испарения S при любой t от 140 до 440оС и скорости газа в пределах 0,026-0,26 м/с, её сначала находят для скорости газа 0,104 м/с и пересчитывают на другую скорость: lg = lg + n ∙ lgV``/V`; Сравнение значения интенсивности испарения жидкой серы и скорости горения говорит о том, что интенсивность горения не может превысить интенсивность испарения при температуре кипения серы. Это подтверждает правильность механизма горения, по которому сера сгорает только в парообразном состоянии. Константа скорости окисления паров серы (реакция протекает по уравнению второго порядка) определяется кинетическим уравнением: -dСS/d = К∙СS∙СО2; СS – концентрация паров S; СО2 – конц-я паров О2; К – константа скорости реакции. Общую концентрацию паров S и О2 оп-ют: СS = а(1-х); СО2 = b – 2ах; а – начальная концентрация паров S; b – начальная конц-я паров О2; х – степень окисления паров S. Тогда:
К∙τ = (2,3 /(b – 2a)) ∙ (lg(b – ax/b(1 - x)));
Константа скорости реакции окисления S до SО2: lgK = В – А/Т;
оС |
650 - 850 |
850 - 1100 |
В |
3,49 |
2,92 |
А |
2510 |
1875 |
Капли серы d < 100мкм сгорают в диффузионном режиме; d>100мкм во взрывном, на участке 100-160 мкм время горения капель не увеличивается.
Т.о. для интенсификации пр-са горения целесообразно распыливать серу на капли d=130-200имкм, что требует затрат дополнительной энергии. При сжигании одного и того же кол-ва S получ. SО2 тем концентрированней, чем меньше объем печного газа и чем выше его t.
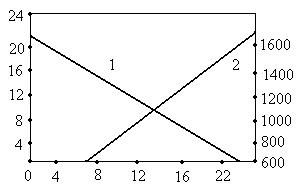 1
– СО2; 2 – СSО2
1
– СО2; 2 – СSО2
На рис.показана приближенная зависимость между t и концентрацией SO2 в печном газе, образовавшемся при адиабатическом сжигании серы в воздухе. На практике получают высококонцентрированную SO2 ограниченную тем, что при t > 1300 быстро разрушается футеровка печи и газоходов. Кроме того в этих условиях могут происходить побочные реакции между O2 и N2 воздуха с образованием оксидов азота, который является нежелательной примесью в SO2, поэтому обычно в серных печах поддерживается t=1000-1200. А печные газы содержат 12-14 об% SO2. Из одного объема O2 образуется один объем SO2, поэтому максимальное теоретическое содержание SO2 в обжиговом газе при сжигании S в воздухе 21%. При сжигании S в воздухе обжиг. O2 содержание SO2 в газовой смеси может возрастать в зависимости от концентрации O2. Теоретическое содержание SO2 при сжигании S в чистом O2 может достигнуть 100%. Возможный состав обжиговых газа, полученного при сжигании S в воздухе и в различных кислородо-азотных смесях представлена на рисунке:

Печи для сжигания серы.
Сжигание S в сернокислотном произ-ве осущ-т в печах в распыленном или тв сост-ии. Для сжигания расплавл-ой S исп-т форсуночные, циклонные и вибрацион-е печи. Наиболее широко примен-ся циклонные и форсуночные. Эти печи классиф-ют по признакам: - по типу установленных форсунок (механич-е, пневматич-е, гидравлич-е) и их располож-ю в печи (радиальное, тангенсальное); - по наличие экранов внутри топочных камер; - по исполнению (гориз-ые, вертик-е); - по располож-ю вход-х отверстий для подачи воздуха; - по устройствам для перемеш-я потоков возд-а с парами S; - по оборуд-ю для испльз-я тепла горения S; - по кол-ву камер.
Форсуночная печь (рис)

1 — стальной цилиндр, 2 — футеровка. 3 — асбест, 4 — перегородки. 5 —форсунка для распыления топлива, 6—форсунки для распыления серы,
7 — короб для подвода воздуха в печь.
Имеет достаточно простую конструкцию, просто в обслуж-ии, в ней образ-ся газ, постоян-й концен-ии SO2. К серьезным недост-м относят: постепен-е разруш-е перегородок из-за выс-х t; низкое теплонапряж-е камеры горения; трудность получ-я газа высокой концен-ии, т.к. исп-ся большой избыток возд-а; зависимость проц-а проведения сжигания от кач-ва распыления S; значит-ый расход топлива при пуске и разогреве печи; сравнит-но большие габариты и масса, и как следствие значит-е капиталовлож-я, производ-ные площади, эксплуатационные расходы и большие потери тепла в окр-ю среду.
Более совершен-ми явл-ся циклонные печи.

1 — форкамера, 2 — воздушный короб, 3, 5 — камеры дожигания, 4. 6—пережимные кольца, 7, 9 — сопла для подачи воздуха, 8, 10 — форсунки для подачи серы.
Дост-ва: тангенциальный ввод возд-а
и S; обеспечивает равномерное сжигание
S в печи за счет лучшей турбулизации
потоков; возмож-ть получения концен-го
технологич-го газа до 18об% SO2;
высокое тепловое напряж-е топочного
простр-ва (4,6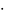 106Вт/м3);
объем апп-та уменьш-ся в 30-40раз по сравн-ю
с объемом форсуночной печи той же
производительности; постоян-ая концен-я
SO2; простое регулиров-я проц-а
горения S и его автоматизация; малые
затраты времени и горючего материала
на разогрев и пуск печи после длит-ой
остан-ки; меньшее содержание оксидов
азота после печи. Основные нед-ки
связаны с высок t в проц-е горения;
возможно растрескивание футеровки и
сварных швов; неудовлет-е распыление S
приводит к проскоку ее паров в т/обмен-м
оборуд-ии после печи, а след-но к коррозии
оборуд-я и непостоянству t
на входе в т/обмен-е оборуд.
106Вт/м3);
объем апп-та уменьш-ся в 30-40раз по сравн-ю
с объемом форсуночной печи той же
производительности; постоян-ая концен-я
SO2; простое регулиров-я проц-а
горения S и его автоматизация; малые
затраты времени и горючего материала
на разогрев и пуск печи после длит-ой
остан-ки; меньшее содержание оксидов
азота после печи. Основные нед-ки
связаны с высок t в проц-е горения;
возможно растрескивание футеровки и
сварных швов; неудовлет-е распыление S
приводит к проскоку ее паров в т/обмен-м
оборуд-ии после печи, а след-но к коррозии
оборуд-я и непостоянству t
на входе в т/обмен-е оборуд.
Расплавлен-я S может поступать в печь через форсунки с тангенсальным или осевым располож-ем. При осевом располож-ии форсунок зона горения нах-ся ближе к периферии. При танген-м – ближе к центру, благодаря чему уменьш-ся действие высоких t на футеровку. (рис) Скорость газового потока сост-ет 100-120м/с – это создает благоприят-е условие для массо- и теплообмена, и возраст-т скорость горения S.
Вибрацион-е печи (рис).
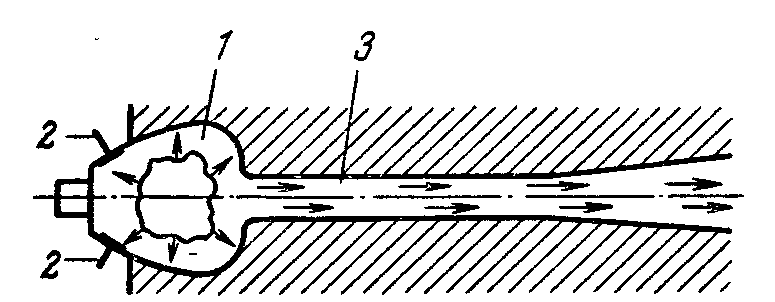
1 – головка печи горелки; 2 – возвратные клапаны; 3 – вибрационный канал.
При вибрац-м горении периодически измен-ся все парам-ры проц-а (давл в камере, скорость и состав газовой смеси, t). Устр-во для вибрац. горения S наз-ся печь-горелка. Перед печью происходит смешение S и возд-а, и они под-ся через обратные клапаны (2) в головку печи-горелки, где происх-т сжигание смеси. Подача сырья осущ-ся порциями (проц-с циклический). В этом варианте печи существенно увелич-ся теплонапряж-е и скорость горения, но перед зажиганием смеси необ-мо хорошее смешение распыленной S с возд-м, чтобы проц-с пошел мгновенно. В этом случае продукты горения хорошо перемеш-ся, газовая пленка SO2, окружающая частицы S разруш-ся и облегчает доступ новых порций О2 в зоне горения. В такой печи образующийся SO2 не сод-т не сгоревших частиц, его концен-я на вых высока.
Для циклон-й печи в сравнении с форсуночной харак-но в 40-65раз большее тепловое напряж-е, возм-ть получения более концен-ного газа и большая паропроизводит-ть.
Важнейшим оборуд-м для печей сжигания жид S явл форсунки, кот должны обеспечить тонкое и равномерное распыление жид S, хорошее смешение ее с возд-м в самой форсунке и за ней, быстрое регулиров-е расхода жид S с сохран-ем необх-го соотнош-я ее с возд-м, устойчивость определ-ой формы, длины факела, а так же иметь прочную конструкцию, надежную и удобную в эксплуатации. Для бесперебойной работы форсунок важно, чтобы S была хорошо очищена от золы и битумов. Форсунки бывают механич-го (жид под собствен давл) и пневматич-го (в распылении еще участвует воздух) действия.
Утилизация теплоты горения серы.
Реакция сильно экзотермическая, в результате происходит выделение большого количества тепла и тем-ра газа на выходе из печей составляет 1100-1300 0С. Для контактного окисления SO2 тем-ра газа на входе в 1-ый слой кат-ра не должна превышать 420 - 450 0С. Поэтому перед стадией окисления SO2 необходимо охлаждение газового потока и утилизации избыточного тепла. В серно-кислотных системах работающих на сере для утилизации теплоты наибольшее распостронение получили водотрубные котлы утилизаторы с естественной циркуляцией тепла. СЭТА – Ц (25 - 24); РКС 95/4,0 – 440.
Энерготехнологический котел РКС 95/4,0 – 440 водотрубный, с естественной циркуляцией, газоплотный котел, рассчитан на работу с наддувом. Котел состоит из испарительных устройств 1-ой 2-ой ступени, вынесенных экономайзеров 1,2 ступени, вынесенных пароперегревателей 1,2 ступени, барабана, топок для сжигания серы. Топка предназначена для сжигания до 650 т жид. Серы в сутки. Топка состоит из двух циклонов , соед-ых относительно др. друга под углом 110 0 и переходной камеры.

Внутренний корпус диаметром 2,6 м, свободно опирается на опоры. Внешний корпус диаметром 3 м. Кольцевое пространство обр-ое внутренним и внешним корпусом вводится воздух, который затем через сопла поступает в камеру сгорания . Сера подается в топку при помощи 8 серных форсунок по 4 на каждом циклоне. Сжигание серы происходит в закрученном газовоздушном потоке. Завихрение потока достигается тангинсиальным вводом воздуха в топочный циклон через воздушные сопла по 3 в каждом циклоне. Количество воздуха регулируется заслонками с электроприводом на каждом воздушном сопле. Переходная камера предназначена для направления газового потока из горизонтальных циклонов в вертикальный газоход испарительного устройства. Внутренняя поверхность топки футирована мулито-корундовым кирпичем марки МКС – 72, толщиной 250 мм.

1 – циклоны
2 - переходная камера
– испарительные устройства
– барабан
