
- •Теми лабораторних занять
- •Загальні правила виконання лабораторного практикуму.
- •Хімічні реактиви, їх зберігання та робота з ними
- •Хімічний посуд
- •Посуд загального призначення
- •Посуд спеціального призначення
- •Мірний посуд
- •Нескляний посуд
- •Лабораторна робота № 2. Основні закони хімії. Визначення еквівалентної маси цинку
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •Обробка результату
- •Контрольні питання та завдання
- •Хід виконання роботи.
- •Обробка результатів
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •Обробка результатів
- •Дослід 2. Вивчення впливу каталізатора (інгібітору) на швидкість реакції
- •Хід виконання роботи.
- •1. Каталітична дія іонів купруму на швидкість окиснення калій йодиду пероксидом водню в кислому середовищі
- •2. Уповільнення взаємодії нітратної кислоти з міддю за допомогою тіосечовини.
- •Контрольні питання та завдання
- •Лабораторна робота № 4. Визначення теплового ефекту реакції нейтралізації
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •2. Розрахуйте кількість речовини (кислоти) в молях, що знаходиться у заданому об’ємі розчину:
- •Обробка результатів
- •Контрольні питання та завдання
- •Лабораторна робота № 5 Приготування розчинів певної концентрації.
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •Контрольні питання та завдання
- •Лабораторна робота № 6.
- •Слабкої кислоти
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •Обробка результатів
- •Контрольні питання та завдання
- •Лабораторна робота № 7. Гідроліз солей
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •Контрольні питання та завдання
- •Лабораторна робота № 8. Окисно – відновні реакції.
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •Контрольні питання та завдання
- •Лабораторна робота № 9. Вивчення методів добування неорганічних сполук різних класів та їх властивостей
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •Контрольні питання та завдання
- •Лабораторна робота № 10. Хімія елементів та їх сполуки. Елементи I та II групи, головної підгрупи.
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •Контрольні питання та завдання
- •Лабораторна робота № 11. Твердість води. Визначення зальної твердості води комплексонометричним методом.
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •Обробка результатів
- •Контрольні питання та завдання
- •Лабораторна робота № 12. Хімія елементів та їх сполуки. Дослідження властивостей нітрогенвмісних сполук
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •Контрольні питання та завдання
- •Лабораторна робота № 13. Хімія елементів та їх сполуки. Дослідження властивостей сульфурвмісних сполук
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •Контрольні питання та завдання
- •Лабораторна робота № 14. Хімія елементів та їх сполуки. Дослідження властивостей сполук мангану та хрому.
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •Контрольні питання та завдання
- •Лабораторна робота № 15. Вивчення властивостей елементів підгрупи феруму. Синтез сполук феруму, кобальту, нікелю.
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •Контрольні питання та завдання
- •Лабораторна робота № 16. Комплексні сполуки. Методи отримання та їх хімічні властивості
- •Теоретичний мінімум.
- •Хід виконання роботи.
- •Контрольні питання та завдання
- •Додаток
- •Рекомендована література.
Хід виконання роботи.
Зважте ошурки металу (приблизно 0,05 г) на технічних терезах із точністю 0,01 г, загорніть їх у маленький шматочок фільтрувального паперу.
У колбу – реактор об’ємом 100…250 мл – через лійку! налийте розбавлену 1:1 хлоридну кислоту. Об’єм кислоти має бути таким, щоб при її горизонтальному положенні кислота не переливалася у горло колби. Кількість кислоти беруть з 80 % -м надлишком.
Колбу з кислотою закріпіть у лапках штатива в горизонтальному положенні і в горло колби обережно покладіть згорточок із наважки металу. Закрийте колбу пробкою з газовідвідною трубкою і перевірте герметичність приладу. Для цього занурте кінчик газовідвідної трубки у пневматичну ванну з водою і зігрійте колбу долонею. Повітря у колбі при нагріванні розширюється і за наявності герметичності з трубки витискуватиметься вода.
Потім зберіть прилад за схемою, що зображена на рис. 31.
Кінчик газовідвідної трубки підведіть під циліндр, заповнений водою, і обережно опустіть його, злегка притиснувши трубочку до дна пневматичної ванни. Відмітьте рівень води у циліндрі (V1) Реакційну колбу переведіть у вертикальне положення. Метал падає у кислоту, взаємодіє з нею й витискує водень. Коли виділення водня припиниться, запишіть рівень води у циліндрі (V2), розгерметизуйте прилад, відкривши реакційну колбу, і дайте системі охолонути до кімнатної температури. Дані досліду запишіть у робочий журнал: об’єм водню, висоту стовпчика води в циліндрі, вимірявши її лінійкою від поверхні води у ванні до поверхні води в циліндрі, атмосферний тиск за барометром і температуру повітря в лабораторії. Користуючись таблицею 2.1, визначте пружність водяної пари, що насичує простір у циліндрі при температурі досліду.
Таблиця. 2.1 Тиск насиченої водяної пари при різних температурах
-
T,К
р(H2O), кПа
Т,К
р(H2O), кПа
Т, К
р(H2O), кПа
288
1,693
293
2,319
298
3,132
289
1,799
294
2,452
299
3,332
290
1,919
295
2,612
300
3,532
291
2,039
296
2,786
301
3,745
292
2,173
297
2,959
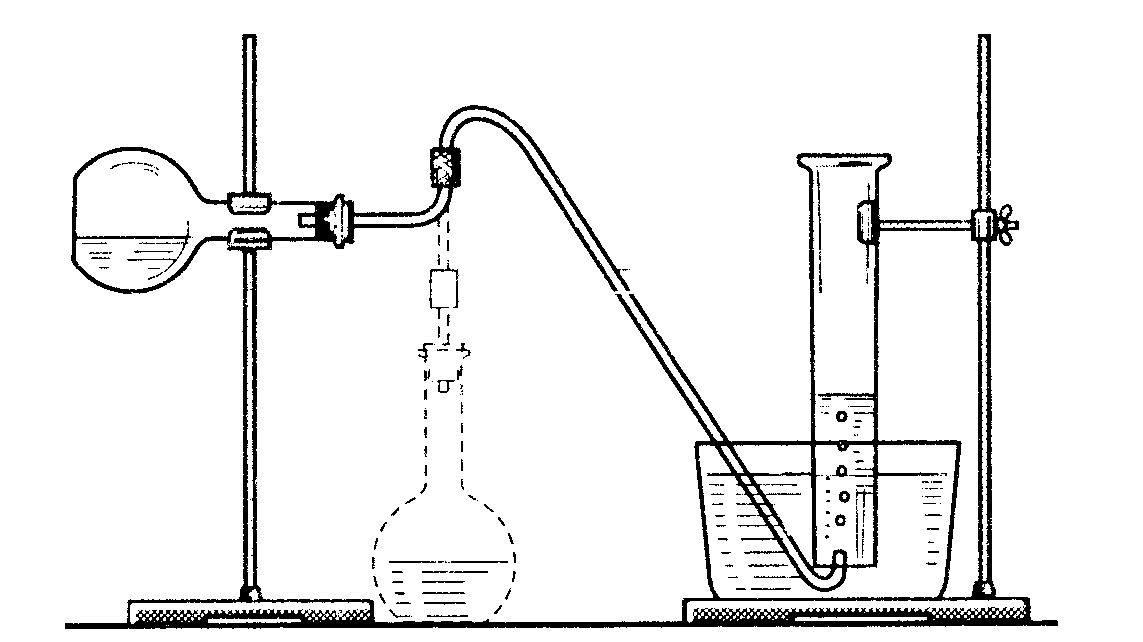
Рис. 31. Прилад для визначення еквівалента металу об’ємним методом
Дані досліду:
- наважка металу m, мг;
- об’єм утвореного водню V, мл; V = V2 - V1
- атмосферний тиск Ратм, мм рт.ст;
- температура повітря t, 0С;
- абсолютна температура Т, К (Т = t + 273);
- тиск водяної пари рН2О, мм (брати з таблиці);
- парціальний тиск водню: Рн2 = Р – Рн2о , мм рт.ст.
